- Home /
- Publicaciones de patentes /
- Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas
Patente nacional por "Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas"
Este registro ha sido solicitado por
Persona física
a través del representanteÁNGEL PONS ARIÑO
Contacto
- Estado: Vigente
- País:
- España
- Fecha solicitud:
- 25/08/2022
- Número solicitud:
-
P202230765
- Número publicación:
-
ES2963238
- Fecha de concesión:
-
- Inventores:
-
Persona física
- Datos del titular:
-
Persona física
- Datos del representante:
-
Ángel Pons Ariño
- Clasificación Internacional de Patentes:
- C07D 401/12,A61K 31/444,A61P 25/28
- Clasificación Internacional de Patentes de la publicación:
- C07D 401/12,A61K 31/444,A61P 25/28
- Fecha de vencimiento:
Quiero registrar una patente
Reivindicaciones:
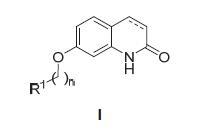
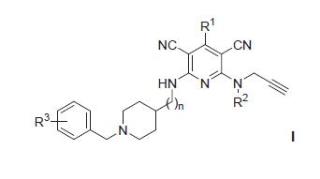
+ ES-2963238_A11. Un compuesto de fórmula I: o una sal farmacéutica del mismo, en donde: R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o más R4; R2 representa H o alquilo C1-C5; cada R3 y R4 representa independientemente alquilo C1-C5, -O-alquilo C1-C5, -NO2 o halógeno; y n es un número entero seleccionado de 0 a 4. 2. El compuesto de fórmula I de acuerdo con la reivindicación 1, en donde R2 representa H o -CH3. 3. El compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 o 2, en donde, en donde R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o dos R4. 4. El compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 3, en donde R4 representa alquilo C1-C5. 5. El compuesto de fórmula I de acuerdo con la reivindicación 1, seleccionado de: Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-1) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-2) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5 dicarbonitrilo (I-3) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-4) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-5) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-6) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-7) ; Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3.5- dicarbonitrilo (I-8) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-9) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-10) ; 2- ( ( (1-Bencilpiperidin-4-il) metil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3.5- dicarbonitrilo (I-11) ; Clorhidrato de 2- ( (3- (1-bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3, 5-dicarbonitrilo (I-12) . 6. Una composición farmacéutica que comprende un compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 5, y uno o más excipientes farmacéuticamente aceptables. 7. Un compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 5 o una composición farmacéutica de acuerdo con la reivindicación 6, para su uso como medicamento. 8. Un compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 5 o una composición farmacéutica de acuerdo con la reivindicación 6, para su uso en el tratamiento de una enfermedad neurológica. 9. El compuesto de fórmula I para su uso de acuerdo con la reivindicación 8, en donde la enfermedad neurológica se selecciona de la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica.
Los productos y servicios protegidos por este registro son:
C07D 401/12 - A61K 31/444 - A61P 25/28
Descripciones:
+ ES-2963238_A1 Derivados de piridina 3.5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas La invención se refiere a derivados de piridina 2, 5-dicarbonitrilo de fórmula I. La invención también se refiere a su uso para el tratamiento y/o prevención de enfermedades neurodegenerativas, particularmente, la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica. ESTADO DE LA TÉCNICA La enfermedad de Alzheimer (EA) es una enfermedad neurodegenerativa caracterizada por el deterioro progresivo de la memoria y la capacidad de aprendizaje debido a una variedad de cambios patológicos en el sistema nervioso central (SNC) (Scheltens, P. et al. The Lancet 2021, 397, 1577) . La revisión bibliográfica muestra que la inhibición de colinesterasas (ChEs) , en concreto, acetilcolinesterasa (AChE) y butirilcolinesterasa (BChE) , monoaminooxidasas (MAO-A/B) y p-secretasa, además de la modulación de los receptores monoaminérgicos, sigue siendo el foco del diseño de fármacos de molécula pequeña relacionados con la EA (do Carmo Carreiras, M. et al. Bioorg. Med. Chem. Lett. 2020, 30, 126880) . La pérdida selectiva de neuronas colinérgicas conduce a una disminución de los niveles de acetilcolina (ACh) en regiones específicas del cerebro que median la cognición (Hampel, H. et al. Brain 2018, 141, 1917) . Por lo tanto, la inhibición de AChE o BChE aumenta los niveles de ACh en la hendidura sináptica y restaura la neurotransmisión colinérgica (Wang, H.; Zhang, H. ACS Chem. Neurosci. 2019, 10, 852) . Por otro lado, las MAO catalizan la oxidación de aminas que actúan como neurotransmisores, liberando H2O2 y, en consecuencia, especies reactivas de oxígeno y nitrógeno (Jones, D.N.; Raghanti, M. A. J. Chem. Neuroanat. 2021, 114, 101957) . La inhibición de la MAO confiere potentes efectos neuroprotectores al disminuir el estrés oxidativo y restaura la plasticidad sináptica deteriorada, la memoria y el aprendizaje en un modelo de ratón de AD a través del control de los niveles tónicos de GABA (Manzoor, S.; Hoda, N. Eur. J. Med. Chem. 2020, 206, 112787) . La enfermedad de Parkinson (EP) es una enfermedad neurodegenerativa crónica que afecta al 1 % de las personas mayores de 60 años. La EP se caracteriza por la muerte progresiva de las neuronas dopaminérgicas en la substantia nigra, y la formación de uerpos de Lewy que contienen agregados de a-sinucleína (Bloem, BR et al. The Lancet 2021, 397, 2284) . El déficit en la neurotransmisión dopaminérgica es la base de los conocidos síntomas asociados a la patología de la EP, en concreto, temblor, rigidez, bradicinesia e inestabilidad postural. Las terapias aprobadas para la EP aumentan los niveles de dopamina en el cuerpo estriado a través de la inhibición selectiva de la MAO-B, por ejemplo, la rasagilina se prescribe como monoterapia en las primeras etapas de la EP y como terapia adicional a la levodopa en las etapas avanzadas de la EP (Armstrong, M.J.; Okun, M. S. JAMA 2020, 323, 548) . La inhibición de la MAO-B es, por lo tanto, un enfoque validado en la enfermedad de Parkinson, mientras que un inhibidor reversible de la MAO-B desarrollado recientemente también rescató el deterioro de la memoria y el aprendizaje en el modelo de EA en ratones APP/PS1 (Park, J.-H. et al. Sci. Adv. 5, eaav0316) . Los receptores de histamina H3 (H3R) se expresan principalmente en el cerebro en el área relacionada con la cognición y la memoria (Panula, P. et al. Pharmacol Rev. 2015, 67, 601) y desde su descubrimiento en los años 80 del siglo pasado todavía están en el centro de atención de los científicos. La utilidad terapéutica muestra que los ligandos anti-H3R, antagonistas o agonistas inversos, podrían ser útiles en el tratamiento de diversas enfermedades humanas, p. ej., EA, EP, narcolepsia, epilepsia, dolor, trastornos alimentarios y metabólicos o alergia. También se sugirió su aplicación en el tratamiento de la esclerosis múltiple, síndrome de Tourette, depresión, enfermedad de Huntington y autismo. Los trabajos intensivos realizados por investigadores académicos y de compañías farmacéuticas han dado lugar a muchos antagonistas/agonistas inversos de H3R potentes y selectivos. Por último, el primero de ellos, pitolisant (Wakix®) , ha entrado en el mercado como medicamento huérfano para la narcolepsia. En los últimos años, los ligandos H3R también se diseñaron para interactuar con al menos un objetivo biológico adicional, tal como, p. ej., AChE, transportador de serotonina, DA D2 y D3 o receptores de histamina H1 (Khanfar, M.A. et al. Front Neurosci. 2016, 10, 1) . Por consiguiente, sería deseable disponer de nuevos fármacos para el tratamiento de enfermedades neurodegenerativas, especialmente para la enfermedad de Alzheimer, la enfermedad de Parkinson y/o la esclerosis lateral amiotrófica, con una eficacia mejorada y sin efectos secundarios, al inhibir la ChE, las enzimas MAO, el receptor sigma 1/2, ya sea en solitario o en combinación con otras actividades beneficiosas, tales como propiedades antioxidantes. DESCRIPCIÓN DE LA INVENCIÓN Un primer aspecto de la presente invención se refiere a un compuesto de fórmula general I: o una sal farmacéutica del mismo, en donde: R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o más R4; R2 representa H o alquilo C1-C5; cada R3 y R4 representa independientemente alquilo C1-C5, -O-alquilo C1-C5, -NO2 o halógeno; y n es un número entero seleccionado de 0 a 4. En otra realización, la invención se refiere al compuesto de fórmula I, en donde R2 representa H o -CH3; y En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, en donde R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o dos R4, y preferiblemente con un R4. En otra realización, la invención se refiere al compuesto de fórmula I, en donde cada R3 y R4 representa independientemente alquilo C 1-C5 y, preferiblemente, -CH3. En otra realización, la invención se refiere al compuesto de fórmula I, en donde R4 representa alquilo C1-C5 y, preferiblemente, -CH3. En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, en donde R1 representa H o -Ph. En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, en donde: R1 representa H o -Ph; R2 representa H o -CH3; y n es un número entero seleccionado de 0 a 4. En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, seleccionado de: Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-1) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-2) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-3) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-4) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-5) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-6) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-7) ; Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-8) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-9) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-10) ; 2- ( ( (1-Bencilpiperidin-4-il) metil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3, 5-dicarbonitrilo (I-11) ; Clorhidrato de 2- ( (3- (1-bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3, 5-dicarbonitrilo (I-12) . La invención se refiere así pues a una sal farmacéuticamente aceptable, profármaco, polimorfo o hidrato de la misma, de un compuesto de fórmula I. Otro aspecto de la invención se refiere a una composición farmacéutica que comprende un compuesto de fórmula I como se ha definido anteriormente y uno o más excipientes farmacéuticamente aceptables. Como se ha indicado anteriormente, la composición farmacéutica comprende el compuesto de fórmula I como se ha definido anteriormente y uno o más excipientes farmacéuticamente aceptables. El excipiente debe ser "aceptable" en el sentido de ser compatible con los otros ingredientes de la composición y no perjudicial para los destinatarios de la misma. Otro aspecto de la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente o a una composición farmacéutica del mismo, para su uso como medicamento. Otro aspecto de la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente o a una composición farmacéutica del mismo, para su uso para el tratamiento de una enfermedad neurológica y, preferiblemente, para el tratamiento de una enfermedad neurológica seleccionada de la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica. Otro aspecto de la invención se refiere al uso del compuesto de fórmula I como se ha definido anteriormente o al uso de la composición farmacéutica como se ha definido anteriormente, para la fabricación de un medicamento. Otro aspecto de la presente invención se refiere a un método de tratamiento o prevención de una enfermedad en un sujeto que lo necesite, especialmente un animal o un ser humano, que comprende administrar a dicho sujeto el compuesto de fórmula I como se ha definido anteriormente o la composición farmacéutica del mismo como se ha definido anteriormente. La composición de la presente invención se puede administrar en forma de cualquier formulación farmacéutica, cuya naturaleza, como se sabe bien, dependerá de la naturaleza del compuesto activo y su vía de administración. Puede usarse cualquier vía de administración, por ejemplo, administración oral, parenteral, nasal, ocular, rectal y tópica. La dosificación y la frecuencia de las dosis dependerán de la naturaleza y gravedad de la enfermedad a tratar, la edad, el estado general y el peso corporal del paciente, así como de la composición administrada y la vía de administración, entre otros factores. Los compuestos de fórmula I como se han definido anteriormente, se puede administrar por separado o en combinación, particularmente como terapia adyuvante administrada simultáneamente, alternativa o sucesivamente con respecto a una terapia de primera línea adecuada para el tratamiento de una enfermedad neurológica, tal como la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica. Otro aspecto de la invención se refiere al uso de un compuesto de fórmula I o una composición farmacéutica del mismo como se ha definido anteriormente, para identificar y evaluar de forma robótica otros compuestos con alto poder neuroprotector que puedan ser útiles como medicamento, preferiblemente para el tratamiento de una enfermedad neurológica, y más preferiblemente para el tratamiento de la enfermedad de Alzheimer, la enfermedad de Parkinson o la esclerosis lateral amiotrófica. En las definiciones anteriores, el término alquilo C1-C5, como un grupo o parte de un grupo, significa una cadena de alquilo lineal o ramificada que contiene de 1 a 5 átomos de carbono e incluye, entre otros, los grupos metilo, etilo, propilo, isopropilo, butilo, isobutilo, sec-butilo, tere-butilo, pentilo e isopentilo. Cuando en las definiciones utilizadas a lo largo de la presente memoria descriptiva para grupos cíclicos Cy1 los ejemplos dados se refieren a un radical de un anillo en términos generales, tal como por ejemplo morfolina o azepina, se incluyen todas las posibles posiciones de fijación. A menos que se defina de otro modo, todos los términos técnicos y científicos utilizados en el presente documento tienen el mismo significado que el que entiende normalmente un experto en la materia a la que pertenece la presente invención. En la puesta en práctica de la presente invención pueden usarse métodos y materiales similares o equivalentes a los que se describen en el presente documento. A lo largo de la descripción y las reivindicaciones, la palabra "comprender" y sus variaciones no pretenden excluir otras características técnicas, aditivos, componentes o etapas. Objetos adicionales, ventajas y características de la invención serán evidentes para los xpertos en la materia tras examinar la descripción o pueden aprenderse poniendo en práctica la invención. Los siguientes ejemplos se proporcionan a modo de ilustración y no tienen por objeto ser limitantes de la presente invención. EJEMPLOS Métodos de síntesis general. Las reacciones se controlaron por TLC utilizando placas de aluminio con gel de sílice prerrevestidas que contenían un indicador fluorescente (Merck, 5539) . La detección se realizó por UV (254 nm) seguida de carbonización con pulverización de ácido sulfúrico-acético, solución acuosa de permanganato de potasio al 1 % o ácido fosfomolíbdico al 0, 5 % en EtOH al 95 %. Se utilizó Na2SO4 anhidro para las secar soluciones orgánicas durante los procesos de elaboración y la eliminación de disolventes se llevó a cabo al vacío con un evaporador rotatorio. La cromatografía en columna ultrarrápida se realizó usando gel de sílice 60 (malla de 230-400) . Los puntos de fusión se determinaron en un bloque Kofler y no están corregidos. Los espectros IR se obtuvieron en un espectrofotómetro Perkin-Elmer Spectrum One. Los espectros de RMN de 1H se registraron con un espectrómetro Varian VXR-200S, utilizando tetrametilsilano como patrón interno y los espectros de RMN de 13C se registraron con un Bruker WP-200-SY. Todas las asignaciones de protones y carbonos estaban de acuerdo con los espectros 2D COSY, HSQC, HMBC y 1D NOESY. Los valores con (*) se pueden intercambiar. La pureza de los compuestos se comprobó mediante análisis elementales, realizados en un aparato Carlo Erba EA 1108, y confirmados para ser >95 %. La síntesis de compuestos de fórmula I se ha llevado a cabo tal como se informa en: (a) Criado, M.; Mulet, J.; Sala, F.; Sala, S.; Colmena, I.; Gandia, L.; Bautista-Aguilera, O. M.; Samadi, A.; Chioua, M.; Marco-Contelles, J. N-Benzylpiperidine Derivatives as a7 Nicotinic Receptor Antagonists ACS Chem. Neurosci.2016, 7, 1157-1165. (b) Samadi, A.; Chioua, M.; Bolea, I.; de los Rios, C.; Iriepa, I.; Moraleda, I.; Bastida, A.; Esteban, G.; Unzeta, M.; Galvez, E.; Marco-Contelles, J. Synthesis, biological assessment and molecular modeling of new multipotent MAO and cholinesterase inhibitors as potential drugs for the treatment of Alzheimer's disease. Eur. J. Med. Chem. 2011, 46, 4665-4668. (c) Bautista-Aguilera, O. M; Esteban, G.; Chioua, M.; Katarina Nikolic, K.; Agbaba, D.; Moraleda; I.; Iriepa; I.; Soriano; E.; Samadi, A.; Unzeta, M.; Marco-Contelles; J. Multipotent cholinesterase/monoamine oxidase inhibitors for the treatment of Alzheimers disease: design, synthesis, biochemical evaluation, ADMET, molecular modeling, and QSARanalysis of novel donepezil-pyridyl hybrids. Drug Des. Dev. Ther. 2014, 81893-1910. La evaluación biológica de compuestos seleccionados de fórmula I se ha llevado a cabo de la siguiente manera: Para estimar el potencial de unión de los compuestos de ensayo hacia el a receptor 1, se realizaron ensayos de desplazamiento de radioligando usando radioligandos adecuados y preparaciones diana. Las constantes de inhibición Ki hacia el receptor a 1 humano se enumeran en la Tabla 1. Para evaluar la aafinidad por 1, se co-incubaron concentraciones crecientes del compuesto de ensayo respectivo (10-11 M - 10-5 M) con el ligando selectivo del areceptor 1, (+) -[3H]pentazocina (PerkinElmer LAS GmbH, Rodgau-Juegesheim, Alemania; AM = 995 GBq/mmol) en una sola concentración (~ 5 nM) y homogeneizados de membrana celular obtenidos a partir de células HEK293 transfectadas de manera estable con el receptor humano a 1 (proporcionado por Olivier Soriani, Instituto de Biología Valrose, Niza, Francia) en tampón de unión (TRIS-HCl 50 mM, pH 7, 4, NaCl 120 mM, KCl 5 mM, CaCl22 mM, MgCh 1 mM) a temperatura ambiente durante 2 h. La unión no específica de ambos radioligandos se determinó mediante incubación conjunta con haloperidol 10 ^M. Las incubaciones se terminaron por filtración a través de filtros de fibra de vidrio GF/B (recolector semiautomático de 48 muestras; Brandel, Gaithersburg, MD, EE. UU.) y la radiactividad unida al filtro se cuantificó mediante recuento de centelleo líquido (Hidex 600 SL; Turku, Finlandia) . Los datos de unión de inhibición se expresaron como % de unión específica del radioligando frente a una concentración molar logarítmica del compuesto de ensayo, y la curva de inhibición se generó mediante regresión no lineal utilizando la ecuación de "competencia en un sitio" en GraphPad Prism (Prism 3.0; Software GraphPad, San Diego, CA, EE. UU.) . A partir de los valores de CI50, las constantes de inhibición Ki se calcularon utilizando la ecuación de Cheng-Prusoff implementada en GraphPad Prism (KD, (+) -[3H]pentazocina, a 1 = 33 M) . La evaluación biológica de compuestos seleccionados de fórmula I ha proporcionado la afinidad de unión de sigma1R que se muestra en la Tabla 1 (análisis de unión de Sigma 1/2R para múltiples objetivos dirigidos a ligandos de fórmula I y análisis de viabilidad celular para ligandos I-1/12 y compuestos patrón NE-10/P28) Tabla 1. Análisis de unión Sigma 1/2R para múltiples dianas dirigidas a ligandos de fórmula I y análisis de viabilidad celular para ligandos I-1/12 y compuestos patrón NE-10/P28. Los valores a K¡ del receptor sigmal humano se midieron en preparaciones de membrana de células HEK-293 transfectadas de manera estable con el receptor sigmal humano usando (+) -[3H]pentazocina como radioligando. La unión no específica del radioligando se ha determinado con haloperidol 10 pM. En cada experimento, los compuestos se ensayaron por triplicado en el intervalo de 10-11-10-5 M. b Maier y Wünsch, JMedChem 2002, 45, 4923-4930: El ensayo de unión a a l se realizó usando una preparación de membrana de cerebro de cobaya como material receptor y [3H]- (+) -pentazocina como radioligando. La unión no específica se determinó con haloperidol 10 pM. c Maier y Wünsch, JMedChem 2002, 45, 4923-4930: La afinidad por el receptor a2 se determinó utilizando preparaciones de membrana de hígado de rata con el radioligando [3H]ditolilguanidina n presencia de (+) -pentazocina 100 nM para enmascarar los sitios de unión de o1. La unión no específica se determinó con ditolilguanidina 10 pM. b c Los valores de Ki se calcularon de acuerdo con Cheng y Prusoff y representan datos de al menos tres experimentos independientes, cada uno realizado por triplicado. Los resultados se dan como media (error típico de la media (SEM) d La viabilidad se ha determinado mediante un ensayo MTT realizado después de la incubación de células SH-SY5Y con compuesto de ensayo a 50 pM o vehículo (DMSO al 0, 5 %) durante 72 h. e nd (no determinado) .
Publicaciones:
ES2963238 (25/03/2024) - A1 Solicitud de patente con informe sobre el estado de la técnica
Eventos:
En fecha 25/08/2022 se realizó Registro Instancia de Solicitud
En fecha 26/08/2022 se realizó Admisión a Trámite
En fecha 26/08/2022 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 20/09/2022 se realizó Superado examen de oficio
En fecha 21/06/2023 se realizó Realizado IET
En fecha 26/06/2023 se realizó 1109P_Comunicación Traslado del IET
En fecha 25/03/2024 se realizó Publicación Solicitud
En fecha 25/03/2024 se realizó Publicación Folleto Solicitud con IET (A1)
Pagos:
25/08/2022 - Pago Tasas IET
+ ES-2963238_A11. Un compuesto de fórmula I: o una sal farmacéutica del mismo, en donde: R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o más R4; R2 representa H o alquilo C1-C5; cada R3 y R4 representa independientemente alquilo C1-C5, -O-alquilo C1-C5, -NO2 o halógeno; y n es un número entero seleccionado de 0 a 4. 2. El compuesto de fórmula I de acuerdo con la reivindicación 1, en donde R2 representa H o -CH3. 3. El compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 o 2, en donde, en donde R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o dos R4. 4. El compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 3, en donde R4 representa alquilo C1-C5. 5. El compuesto de fórmula I de acuerdo con la reivindicación 1, seleccionado de: Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-1) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-2) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5 dicarbonitrilo (I-3) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-4) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-5) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-6) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-7) ; Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3.5- dicarbonitrilo (I-8) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-9) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-10) ; 2- ( ( (1-Bencilpiperidin-4-il) metil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3.5- dicarbonitrilo (I-11) ; Clorhidrato de 2- ( (3- (1-bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3, 5-dicarbonitrilo (I-12) . 6. Una composición farmacéutica que comprende un compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 5, y uno o más excipientes farmacéuticamente aceptables. 7. Un compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 5 o una composición farmacéutica de acuerdo con la reivindicación 6, para su uso como medicamento. 8. Un compuesto de fórmula I de acuerdo con cualquiera de las reivindicaciones 1 a 5 o una composición farmacéutica de acuerdo con la reivindicación 6, para su uso en el tratamiento de una enfermedad neurológica. 9. El compuesto de fórmula I para su uso de acuerdo con la reivindicación 8, en donde la enfermedad neurológica se selecciona de la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica.
Los productos y servicios protegidos por este registro son:
C07D 401/12 - A61K 31/444 - A61P 25/28
Descripciones:
+ ES-2963238_A1 Derivados de piridina 3.5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas La invención se refiere a derivados de piridina 2, 5-dicarbonitrilo de fórmula I. La invención también se refiere a su uso para el tratamiento y/o prevención de enfermedades neurodegenerativas, particularmente, la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica. ESTADO DE LA TÉCNICA La enfermedad de Alzheimer (EA) es una enfermedad neurodegenerativa caracterizada por el deterioro progresivo de la memoria y la capacidad de aprendizaje debido a una variedad de cambios patológicos en el sistema nervioso central (SNC) (Scheltens, P. et al. The Lancet 2021, 397, 1577) . La revisión bibliográfica muestra que la inhibición de colinesterasas (ChEs) , en concreto, acetilcolinesterasa (AChE) y butirilcolinesterasa (BChE) , monoaminooxidasas (MAO-A/B) y p-secretasa, además de la modulación de los receptores monoaminérgicos, sigue siendo el foco del diseño de fármacos de molécula pequeña relacionados con la EA (do Carmo Carreiras, M. et al. Bioorg. Med. Chem. Lett. 2020, 30, 126880) . La pérdida selectiva de neuronas colinérgicas conduce a una disminución de los niveles de acetilcolina (ACh) en regiones específicas del cerebro que median la cognición (Hampel, H. et al. Brain 2018, 141, 1917) . Por lo tanto, la inhibición de AChE o BChE aumenta los niveles de ACh en la hendidura sináptica y restaura la neurotransmisión colinérgica (Wang, H.; Zhang, H. ACS Chem. Neurosci. 2019, 10, 852) . Por otro lado, las MAO catalizan la oxidación de aminas que actúan como neurotransmisores, liberando H2O2 y, en consecuencia, especies reactivas de oxígeno y nitrógeno (Jones, D.N.; Raghanti, M. A. J. Chem. Neuroanat. 2021, 114, 101957) . La inhibición de la MAO confiere potentes efectos neuroprotectores al disminuir el estrés oxidativo y restaura la plasticidad sináptica deteriorada, la memoria y el aprendizaje en un modelo de ratón de AD a través del control de los niveles tónicos de GABA (Manzoor, S.; Hoda, N. Eur. J. Med. Chem. 2020, 206, 112787) . La enfermedad de Parkinson (EP) es una enfermedad neurodegenerativa crónica que afecta al 1 % de las personas mayores de 60 años. La EP se caracteriza por la muerte progresiva de las neuronas dopaminérgicas en la substantia nigra, y la formación de uerpos de Lewy que contienen agregados de a-sinucleína (Bloem, BR et al. The Lancet 2021, 397, 2284) . El déficit en la neurotransmisión dopaminérgica es la base de los conocidos síntomas asociados a la patología de la EP, en concreto, temblor, rigidez, bradicinesia e inestabilidad postural. Las terapias aprobadas para la EP aumentan los niveles de dopamina en el cuerpo estriado a través de la inhibición selectiva de la MAO-B, por ejemplo, la rasagilina se prescribe como monoterapia en las primeras etapas de la EP y como terapia adicional a la levodopa en las etapas avanzadas de la EP (Armstrong, M.J.; Okun, M. S. JAMA 2020, 323, 548) . La inhibición de la MAO-B es, por lo tanto, un enfoque validado en la enfermedad de Parkinson, mientras que un inhibidor reversible de la MAO-B desarrollado recientemente también rescató el deterioro de la memoria y el aprendizaje en el modelo de EA en ratones APP/PS1 (Park, J.-H. et al. Sci. Adv. 5, eaav0316) . Los receptores de histamina H3 (H3R) se expresan principalmente en el cerebro en el área relacionada con la cognición y la memoria (Panula, P. et al. Pharmacol Rev. 2015, 67, 601) y desde su descubrimiento en los años 80 del siglo pasado todavía están en el centro de atención de los científicos. La utilidad terapéutica muestra que los ligandos anti-H3R, antagonistas o agonistas inversos, podrían ser útiles en el tratamiento de diversas enfermedades humanas, p. ej., EA, EP, narcolepsia, epilepsia, dolor, trastornos alimentarios y metabólicos o alergia. También se sugirió su aplicación en el tratamiento de la esclerosis múltiple, síndrome de Tourette, depresión, enfermedad de Huntington y autismo. Los trabajos intensivos realizados por investigadores académicos y de compañías farmacéuticas han dado lugar a muchos antagonistas/agonistas inversos de H3R potentes y selectivos. Por último, el primero de ellos, pitolisant (Wakix®) , ha entrado en el mercado como medicamento huérfano para la narcolepsia. En los últimos años, los ligandos H3R también se diseñaron para interactuar con al menos un objetivo biológico adicional, tal como, p. ej., AChE, transportador de serotonina, DA D2 y D3 o receptores de histamina H1 (Khanfar, M.A. et al. Front Neurosci. 2016, 10, 1) . Por consiguiente, sería deseable disponer de nuevos fármacos para el tratamiento de enfermedades neurodegenerativas, especialmente para la enfermedad de Alzheimer, la enfermedad de Parkinson y/o la esclerosis lateral amiotrófica, con una eficacia mejorada y sin efectos secundarios, al inhibir la ChE, las enzimas MAO, el receptor sigma 1/2, ya sea en solitario o en combinación con otras actividades beneficiosas, tales como propiedades antioxidantes. DESCRIPCIÓN DE LA INVENCIÓN Un primer aspecto de la presente invención se refiere a un compuesto de fórmula general I: o una sal farmacéutica del mismo, en donde: R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o más R4; R2 representa H o alquilo C1-C5; cada R3 y R4 representa independientemente alquilo C1-C5, -O-alquilo C1-C5, -NO2 o halógeno; y n es un número entero seleccionado de 0 a 4. En otra realización, la invención se refiere al compuesto de fórmula I, en donde R2 representa H o -CH3; y En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, en donde R1 representa H o -Ph, en donde -Ph está opcionalmente sustituido con uno o dos R4, y preferiblemente con un R4. En otra realización, la invención se refiere al compuesto de fórmula I, en donde cada R3 y R4 representa independientemente alquilo C 1-C5 y, preferiblemente, -CH3. En otra realización, la invención se refiere al compuesto de fórmula I, en donde R4 representa alquilo C1-C5 y, preferiblemente, -CH3. En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, en donde R1 representa H o -Ph. En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, en donde: R1 representa H o -Ph; R2 representa H o -CH3; y n es un número entero seleccionado de 0 a 4. En otra realización, la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente, seleccionado de: Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-1) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-2) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-3) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-4) ; Clorhidrato de 2- ( (2- (1-bencilpiperidin-4-il) etil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-5) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-6) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -6- (metil (prop-2-in-1-il) amino) piridin-3, 5-dicarbonitrilo (I-7) ; Clorhidrato de 2- ( (1-bencilpiperidin-4-il) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-8) ; 2- ( (3- (1-Bencilpiperidin-4-il) propil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-9) ; 2- ( (4- (1-Bencilpiperidin-4-il) butil) amino) -4-fenil-6- (prop-2-in-1-ilamino) piridin-3, 5-dicarbonitrilo (I-10) ; 2- ( ( (1-Bencilpiperidin-4-il) metil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3, 5-dicarbonitrilo (I-11) ; Clorhidrato de 2- ( (3- (1-bencilpiperidin-4-il) propil) amino) -6- (metil (prop-2-in-1-il) amino) -4-fenilpiridin-3, 5-dicarbonitrilo (I-12) . La invención se refiere así pues a una sal farmacéuticamente aceptable, profármaco, polimorfo o hidrato de la misma, de un compuesto de fórmula I. Otro aspecto de la invención se refiere a una composición farmacéutica que comprende un compuesto de fórmula I como se ha definido anteriormente y uno o más excipientes farmacéuticamente aceptables. Como se ha indicado anteriormente, la composición farmacéutica comprende el compuesto de fórmula I como se ha definido anteriormente y uno o más excipientes farmacéuticamente aceptables. El excipiente debe ser "aceptable" en el sentido de ser compatible con los otros ingredientes de la composición y no perjudicial para los destinatarios de la misma. Otro aspecto de la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente o a una composición farmacéutica del mismo, para su uso como medicamento. Otro aspecto de la invención se refiere a un compuesto de fórmula I como se ha definido anteriormente o a una composición farmacéutica del mismo, para su uso para el tratamiento de una enfermedad neurológica y, preferiblemente, para el tratamiento de una enfermedad neurológica seleccionada de la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica. Otro aspecto de la invención se refiere al uso del compuesto de fórmula I como se ha definido anteriormente o al uso de la composición farmacéutica como se ha definido anteriormente, para la fabricación de un medicamento. Otro aspecto de la presente invención se refiere a un método de tratamiento o prevención de una enfermedad en un sujeto que lo necesite, especialmente un animal o un ser humano, que comprende administrar a dicho sujeto el compuesto de fórmula I como se ha definido anteriormente o la composición farmacéutica del mismo como se ha definido anteriormente. La composición de la presente invención se puede administrar en forma de cualquier formulación farmacéutica, cuya naturaleza, como se sabe bien, dependerá de la naturaleza del compuesto activo y su vía de administración. Puede usarse cualquier vía de administración, por ejemplo, administración oral, parenteral, nasal, ocular, rectal y tópica. La dosificación y la frecuencia de las dosis dependerán de la naturaleza y gravedad de la enfermedad a tratar, la edad, el estado general y el peso corporal del paciente, así como de la composición administrada y la vía de administración, entre otros factores. Los compuestos de fórmula I como se han definido anteriormente, se puede administrar por separado o en combinación, particularmente como terapia adyuvante administrada simultáneamente, alternativa o sucesivamente con respecto a una terapia de primera línea adecuada para el tratamiento de una enfermedad neurológica, tal como la enfermedad de Alzheimer, la enfermedad de Parkinson y la esclerosis lateral amiotrófica. Otro aspecto de la invención se refiere al uso de un compuesto de fórmula I o una composición farmacéutica del mismo como se ha definido anteriormente, para identificar y evaluar de forma robótica otros compuestos con alto poder neuroprotector que puedan ser útiles como medicamento, preferiblemente para el tratamiento de una enfermedad neurológica, y más preferiblemente para el tratamiento de la enfermedad de Alzheimer, la enfermedad de Parkinson o la esclerosis lateral amiotrófica. En las definiciones anteriores, el término alquilo C1-C5, como un grupo o parte de un grupo, significa una cadena de alquilo lineal o ramificada que contiene de 1 a 5 átomos de carbono e incluye, entre otros, los grupos metilo, etilo, propilo, isopropilo, butilo, isobutilo, sec-butilo, tere-butilo, pentilo e isopentilo. Cuando en las definiciones utilizadas a lo largo de la presente memoria descriptiva para grupos cíclicos Cy1 los ejemplos dados se refieren a un radical de un anillo en términos generales, tal como por ejemplo morfolina o azepina, se incluyen todas las posibles posiciones de fijación. A menos que se defina de otro modo, todos los términos técnicos y científicos utilizados en el presente documento tienen el mismo significado que el que entiende normalmente un experto en la materia a la que pertenece la presente invención. En la puesta en práctica de la presente invención pueden usarse métodos y materiales similares o equivalentes a los que se describen en el presente documento. A lo largo de la descripción y las reivindicaciones, la palabra "comprender" y sus variaciones no pretenden excluir otras características técnicas, aditivos, componentes o etapas. Objetos adicionales, ventajas y características de la invención serán evidentes para los xpertos en la materia tras examinar la descripción o pueden aprenderse poniendo en práctica la invención. Los siguientes ejemplos se proporcionan a modo de ilustración y no tienen por objeto ser limitantes de la presente invención. EJEMPLOS Métodos de síntesis general. Las reacciones se controlaron por TLC utilizando placas de aluminio con gel de sílice prerrevestidas que contenían un indicador fluorescente (Merck, 5539) . La detección se realizó por UV (254 nm) seguida de carbonización con pulverización de ácido sulfúrico-acético, solución acuosa de permanganato de potasio al 1 % o ácido fosfomolíbdico al 0, 5 % en EtOH al 95 %. Se utilizó Na2SO4 anhidro para las secar soluciones orgánicas durante los procesos de elaboración y la eliminación de disolventes se llevó a cabo al vacío con un evaporador rotatorio. La cromatografía en columna ultrarrápida se realizó usando gel de sílice 60 (malla de 230-400) . Los puntos de fusión se determinaron en un bloque Kofler y no están corregidos. Los espectros IR se obtuvieron en un espectrofotómetro Perkin-Elmer Spectrum One. Los espectros de RMN de 1H se registraron con un espectrómetro Varian VXR-200S, utilizando tetrametilsilano como patrón interno y los espectros de RMN de 13C se registraron con un Bruker WP-200-SY. Todas las asignaciones de protones y carbonos estaban de acuerdo con los espectros 2D COSY, HSQC, HMBC y 1D NOESY. Los valores con (*) se pueden intercambiar. La pureza de los compuestos se comprobó mediante análisis elementales, realizados en un aparato Carlo Erba EA 1108, y confirmados para ser >95 %. La síntesis de compuestos de fórmula I se ha llevado a cabo tal como se informa en: (a) Criado, M.; Mulet, J.; Sala, F.; Sala, S.; Colmena, I.; Gandia, L.; Bautista-Aguilera, O. M.; Samadi, A.; Chioua, M.; Marco-Contelles, J. N-Benzylpiperidine Derivatives as a7 Nicotinic Receptor Antagonists ACS Chem. Neurosci.2016, 7, 1157-1165. (b) Samadi, A.; Chioua, M.; Bolea, I.; de los Rios, C.; Iriepa, I.; Moraleda, I.; Bastida, A.; Esteban, G.; Unzeta, M.; Galvez, E.; Marco-Contelles, J. Synthesis, biological assessment and molecular modeling of new multipotent MAO and cholinesterase inhibitors as potential drugs for the treatment of Alzheimer's disease. Eur. J. Med. Chem. 2011, 46, 4665-4668. (c) Bautista-Aguilera, O. M; Esteban, G.; Chioua, M.; Katarina Nikolic, K.; Agbaba, D.; Moraleda; I.; Iriepa; I.; Soriano; E.; Samadi, A.; Unzeta, M.; Marco-Contelles; J. Multipotent cholinesterase/monoamine oxidase inhibitors for the treatment of Alzheimers disease: design, synthesis, biochemical evaluation, ADMET, molecular modeling, and QSARanalysis of novel donepezil-pyridyl hybrids. Drug Des. Dev. Ther. 2014, 81893-1910. La evaluación biológica de compuestos seleccionados de fórmula I se ha llevado a cabo de la siguiente manera: Para estimar el potencial de unión de los compuestos de ensayo hacia el a receptor 1, se realizaron ensayos de desplazamiento de radioligando usando radioligandos adecuados y preparaciones diana. Las constantes de inhibición Ki hacia el receptor a 1 humano se enumeran en la Tabla 1. Para evaluar la aafinidad por 1, se co-incubaron concentraciones crecientes del compuesto de ensayo respectivo (10-11 M - 10-5 M) con el ligando selectivo del areceptor 1, (+) -[3H]pentazocina (PerkinElmer LAS GmbH, Rodgau-Juegesheim, Alemania; AM = 995 GBq/mmol) en una sola concentración (~ 5 nM) y homogeneizados de membrana celular obtenidos a partir de células HEK293 transfectadas de manera estable con el receptor humano a 1 (proporcionado por Olivier Soriani, Instituto de Biología Valrose, Niza, Francia) en tampón de unión (TRIS-HCl 50 mM, pH 7, 4, NaCl 120 mM, KCl 5 mM, CaCl22 mM, MgCh 1 mM) a temperatura ambiente durante 2 h. La unión no específica de ambos radioligandos se determinó mediante incubación conjunta con haloperidol 10 ^M. Las incubaciones se terminaron por filtración a través de filtros de fibra de vidrio GF/B (recolector semiautomático de 48 muestras; Brandel, Gaithersburg, MD, EE. UU.) y la radiactividad unida al filtro se cuantificó mediante recuento de centelleo líquido (Hidex 600 SL; Turku, Finlandia) . Los datos de unión de inhibición se expresaron como % de unión específica del radioligando frente a una concentración molar logarítmica del compuesto de ensayo, y la curva de inhibición se generó mediante regresión no lineal utilizando la ecuación de "competencia en un sitio" en GraphPad Prism (Prism 3.0; Software GraphPad, San Diego, CA, EE. UU.) . A partir de los valores de CI50, las constantes de inhibición Ki se calcularon utilizando la ecuación de Cheng-Prusoff implementada en GraphPad Prism (KD, (+) -[3H]pentazocina, a 1 = 33 M) . La evaluación biológica de compuestos seleccionados de fórmula I ha proporcionado la afinidad de unión de sigma1R que se muestra en la Tabla 1 (análisis de unión de Sigma 1/2R para múltiples objetivos dirigidos a ligandos de fórmula I y análisis de viabilidad celular para ligandos I-1/12 y compuestos patrón NE-10/P28) Tabla 1. Análisis de unión Sigma 1/2R para múltiples dianas dirigidas a ligandos de fórmula I y análisis de viabilidad celular para ligandos I-1/12 y compuestos patrón NE-10/P28. Los valores a K¡ del receptor sigmal humano se midieron en preparaciones de membrana de células HEK-293 transfectadas de manera estable con el receptor sigmal humano usando (+) -[3H]pentazocina como radioligando. La unión no específica del radioligando se ha determinado con haloperidol 10 pM. En cada experimento, los compuestos se ensayaron por triplicado en el intervalo de 10-11-10-5 M. b Maier y Wünsch, JMedChem 2002, 45, 4923-4930: El ensayo de unión a a l se realizó usando una preparación de membrana de cerebro de cobaya como material receptor y [3H]- (+) -pentazocina como radioligando. La unión no específica se determinó con haloperidol 10 pM. c Maier y Wünsch, JMedChem 2002, 45, 4923-4930: La afinidad por el receptor a2 se determinó utilizando preparaciones de membrana de hígado de rata con el radioligando [3H]ditolilguanidina n presencia de (+) -pentazocina 100 nM para enmascarar los sitios de unión de o1. La unión no específica se determinó con ditolilguanidina 10 pM. b c Los valores de Ki se calcularon de acuerdo con Cheng y Prusoff y representan datos de al menos tres experimentos independientes, cada uno realizado por triplicado. Los resultados se dan como media (error típico de la media (SEM) d La viabilidad se ha determinado mediante un ensayo MTT realizado después de la incubación de células SH-SY5Y con compuesto de ensayo a 50 pM o vehículo (DMSO al 0, 5 %) durante 72 h. e nd (no determinado) .
Publicaciones:
ES2963238 (25/03/2024) - A1 Solicitud de patente con informe sobre el estado de la técnica
Eventos:
En fecha 25/08/2022 se realizó Registro Instancia de Solicitud
En fecha 26/08/2022 se realizó Admisión a Trámite
En fecha 26/08/2022 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 20/09/2022 se realizó Superado examen de oficio
En fecha 21/06/2023 se realizó Realizado IET
En fecha 26/06/2023 se realizó 1109P_Comunicación Traslado del IET
En fecha 25/03/2024 se realizó Publicación Solicitud
En fecha 25/03/2024 se realizó Publicación Folleto Solicitud con IET (A1)
Pagos:
25/08/2022 - Pago Tasas IET
Fuente de la información
Parte de la información aquí publicada es pública puesto que ha sido obtenida de la Oficina de Propiedad Industrial de los diferentes países el 29/04/2024 y por lo tanto puede ser que la información no esté actualizada.Parte de la información aquí mostrada ha sido calculada por nuestro sistema informático y puede no ser veraz.
Privacidad
Si considera que al información aquí publicada afecta a su privacidad y desea que eliminemos la información aquí publicada envíe un email a info@patentes-y-marcas.com o rellene el formulario que encontrará aquí.Información sobre el registro de patente nacional por Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765
El registro de patente nacional por Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765 fue solicitada el 25/08/2022. Se trata de un registro en España por lo que este registro no ofrece protección en el resto de países. El registro Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765 fue solicitada por CONSEJO SUPERIOR DE INVESTIGACIONES CIENTÍFICAS mediante los servicios del agente Ángel Pons Ariño. El registro [modality] por Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765 está clasificado como C07D 401/12,A61K 31/444,A61P 25/28 según la clasificación internacional de patentes.
Otras invenciones solicitadas en la clasificación internacional de patentes C07D 401/12,A61K 31/444,A61P 25/28.
Es posible conocer invenciones similares al campo de la técnica se refiere. El registro de patente nacional por Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765 está clasificado con la clasificación C07D 401/12,A61K 31/444,A61P 25/28 por lo que si se desea conocer más registros con la clasificación C07D 401/12,A61K 31/444,A61P 25/28 clicar aquí.Otras invenciones solicitadas a través del representante ÁNGEL PONS ARIÑO
Es posible conocer todas las invenciones solicitadas a través del agente ÁNGEL PONS ARIÑO entre las que se encuentra el registro patente nacional por Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Si se desean conocer más invenciones solicitadas a través del agente ÁNGEL PONS ARIÑO clicar aquí.Patentes en España
Es posible conocer todas las invenciones publicadas en España entre las que se encuentra el registro patente nacional por Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas. Nuestro portal www.patentes-y-marcas.com ofrece acceso a las publicaciones de patentes en España. Conocer las patentes registradas en un país es importante para saber las posibilidades de fabricar, vender o explotar una invención en España.Patentes registradas en la clase C
Es posible conocer todas las patentes registradas en la clase C (QUIMICA; METALURGIA) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C07
Es posible conocer todas las patentes registradas en la clase C07 (QUIMICA ORGANICA) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C07D
Es posible conocer todas las patentes registradas en la clase C07D (COMPUESTOS HETEROCICLICOS) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A
Es posible conocer todas las patentes registradas en la clase A (NECESIDADES CORRIENTES DE LA VIDA) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61
Es posible conocer todas las patentes registradas en la clase A61 (CIENCIAS MEDICAS O VETERINARIAS; HIGIENE) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61K
Es posible conocer todas las patentes registradas en la clase A61K (PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO ) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61P
Es posible conocer todas las patentes registradas en la clase A61P (ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES) entre las que se encuentra la patente Derivados de piridina 3,5-dicarbonitrilo para el tratamiento y prevención de enfermedades neurodegenerativas con el número P202230765. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.
¿Tienes alguna duda?
Escribe tu consulta y te responderemos rápida y gratuitamente.


 P202230763
P202230763