- Home /
- Publicaciones de patentes /
- Nuevo tratamiento del cáncer colorrectal
Patente nacional por "Nuevo tratamiento del cáncer colorrectal"
Este registro ha sido solicitado por
FUNDACION UNIVERSITARIA SAN ANTONIO
a través del representanteMARIA DESAMPARADOS DIAZ PACHECO
Contacto
- Estado: Vigente
- País:
- España
- Fecha solicitud:
- 27/01/2021
- Número solicitud:
-
P202130064
- Número publicación:
-
ES2919898
- Fecha de concesión:
-
05/10/2023
- Inventores:
-
Persona física
- Datos del titular:
-
FUNDACION UNIVERSITARIA SAN ANTONIO
- Datos del representante:
-
MARIA DESAMPARADOS DIAZ PACHECO
- Clasificación Internacional de Patentes:
- A61K 31/496,A61P 35/00
- Clasificación Internacional de Patentes de la publicación:
- A61K 31/496,A61P 35/00
- Fecha de vencimiento:
Quiero registrar una patente
Reivindicaciones:
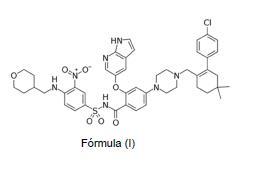
+ ES-2919898_A11. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer gastrointestinal en un individuo. Fórmula (I) 2. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según la reivindicación anterior, donde el cáncer gastrointestinal es el cáncer colorrectal. 3. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según la reivindicación anterior, donde el cáncer colorrectal es el cáncer colorrectal metastásico. 4. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según cualquiera de las reivindicaciones 1-3, donde el individuo presenta los niveles de hepsina elevados con respecto a los niveles normales. 5. Una composición que comprende el compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según cualquiera de las reivindicaciones 1-4. 6. La composición según la reivindicación 5, que es una composición farmacéutica. 7. La composición según cualquiera de las reivindicaciones 5-6, donde la composición además comprende excipientes y/o un vehículo farmacéuticamente aceptable. 8. La composición según cualquiera de las reivindicaciones 5-7, donde la composición además comprende otro principio activo.
+ ES-2919898_B21. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso en la prevención, mejora, alivio y/o tratamiento del cáncer colorrectal en un individuo donde dicho individuo presenta los niveles de hepsina elevados con respecto a los niveles normales. Fórmula (I) 2. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según la reivindicación anterior, donde el cáncer colorrectal es el cáncer colorrectal metastásico.345 3. Una composición que comprende el compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según cualquiera de las reivindicaciones 1-2. 4. La composición según la reivindicación 3, que es una composición farmacéutica. 5. La composición según cualquiera de las reivindicaciones 3-4, donde la composición además comprende excipientes y/o un vehículo farmacéuticamente aceptable. 6. La composición según cualquiera de las reivindicaciones 3-5, donde la composición además comprende otro principio activo.
Los productos y servicios protegidos por este registro son:
A61K 31/496 - A61P 35/00
Descripciones:
+ ES-2919898_A1 Nuevo tratamiento del cáncer colorrectal CAMPO DE LA INVENCIÓN La presente invención pertenece al campo de la biomedicina, y más concretamente se refiere a un nuevo tratamiento para el cáncer gastrointestinal, y más preferiblemente para el tratamiento del cáncer gástrico y el cáncer colorrectal. ESTADO DE LA TÉCNICA ANTERIOR El cáncer colorrectal es el tercer cáncer más común diagnosticado tanto en hombres como en mujeres. Tiene lugar en el colon y recto y se desarrolla lentamente a partir de pólipos adenomatosos. El crecimiento excesivo de la mucosa del colon genera estos pólipos que tienen una morfología pedunculada o sésil. El desarrollo de cáncer colorrectal puede tener lugar por diferentes vías. Entre ellas se encuentra la aparición de lesiones serradas con apariencia del epitelio en dientes de sierra y que ocurre en el colon proximal. Esta vía se detecta en un tercio de todos los cánceres colorrectales. Con respecto a la secuencia adenoma-carcinoma, se ha propuesto que la progresión desde adenomas pequeños a grandes adenomas o adenocarcinomas avanzados está mediada por múltiples rutas moleculares que incluyen la inestabilidad de microsatélites, la inestabilidad cromosómica y rutas epigenéticas. Es posible hacer una prevención precoz puesto que se ha estimado que al menos lleva 10 años que un pólipo se transforme en célula tumoral (PMID: 28842051 0ines et al. Best Pract Res Clin Gastroenterol. 2017 Aug;31 (4) :419-424) . El diagnóstico precoz mediante colonoscopia y detección de sangre oculta en heces, así como la mejora en los tratamientos ha contribuido a prolongar la supervivencia de los tumores colorrectales en la fase de curación, Sin embargo, la metástasis está presente en aproximadamente el 25% de los pacientes durante el diagnóstico y en total, el 50% de los pacientes con cáncer colorrectal desarrollará metástasis (PMID: 27672422 Ohhara et al. World J Gastrointest Oncol. 2016 Sep 15;8 (9) :642-55) . Debido a la heterogeneidad y naturaleza multifactorial del cáncer colorrectal han aumentado considerablemente en los últimos años estudios para identificar predictores clínicos y moleculares, así como factores pronósticos con potencial para mejorar el manejo de los pacientes (PMID: 26964802 Aran et al. Clin Colorectal Cáncer. 2016 Sep;15 (3) :195-203; PMID: 29139091 Bermejo et al. Drugs. 2018 Jan;78 (1) :1-18) . Tanto la incidencia como la mortalidad del cáncer colorrectal ha disminuido tanto para hombres como para mujeres desde 1970 debido a la detección precoz (PMID: 29313949 Siegel et al. CA Cáncer J Clin. 2018 Jan;68 (1) :7-30) . Sin embargo, aunque diferentes terapias estás disponibles para el cáncer colorrectal metastásico, los resultados no son óptimos debido a la heterogeneidad entre pacientes debido a características moleculares, respuesta a la terapia y presentación clínica (PMID: 25593032 Linnekamp et al. Cáncer Res. 2015 Jan 15;75 (2) :245-9) . Los tratamientos más comunes de estos tumores se basan en la cirugía, la quimioterapia, terapias dirigidas y el tratamiento hormonal sustitutivo. Al menos el 50% de los pacientes con cáncer colorrectal recaen tras la resección quirúrgica y finalmente mueren de enfermedad metastásica. A pesar de la quimioterapia adyuvante postoperatoria en estos pacientes para disminuir el riesgo de recurrencia, el tratamiento adyuvante no da beneficios en supervivencia, especialmente en pacientes diagnosticados con estadío I. La terapia dirigida está basada en anticuerpos monoclonales y pequeños inhibidores moleculares, que selectivamente bloquean la proliferación celular mediante la intervención con ciertas moléculas y proteínas sobreexpresadas requeridas para la expansión del tumor. De acuerdo a la clasificación Mesh, el cáncer colorrectal se encuentra incluido en los cánceres gastrointestinales. La clasificación es la siguiente: Neoplasms [C04] Neoplasms by Site [C04.588] o Digestive System Neoplasms [C04.588.274] Gastrointestinal Neoplasms [C04.588.274.476] Esophageal Neoplasms [C04.588.274.476.205]_ Esophageal Squamous Cell Carcinoma [C04.588.274.476.205.500] Intestinal Neoplasms [C04.588.274.476.411] Cecal Neoplasms [C04.588.274.476.411.184], Appendiceal Neoplasms [C04.588.274.476.411.184.290] Colorectal Neoplasms [C04.588.274.476.411.307] Adenomatous Polyposis Coli [C04.588.274.476.411.307.089] Colonic Neoplasms [C04.588.274.476.411.307.180] Colitis-Associated Neoplasms [C04.588.274.476.411.307.180.400 ] Sigmoid Neoplasms [C04.588.274.476.411.307.180.800 ] Colorectal Neoplasms, Hereditar y Nonpolyposis [C04.588.274.476.411.307.190] Rectal Neoplasms [C04.588.274.476.411.307.790] Anus Neoplasms [C04.588.274.476.411.307.790.040 ] Anal Gland Neoplasms [C04.588.274.476.411.307. 790.040.040] Por tanto, es necesario desarrollar nuevos tratamientos para el cáncer colorrectal DESCRIPCIÓN DE LAS FIGURAS Fig. 1. Pose resultante del docking molecular entre Venetoclax y hepsina. Fig. 2. Cálculo del valor de IC50 de Venetoclax sobre la actividad de Hepsina. Velocidad máxima de la actividad de Hepsina en presencia de dosis crecientes de Venetoclax. Fig.3 . Efecto de Venetoclax en la migración de células de cáncer colorrectal. Porcentaje de migración celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 4. Efecto de Venetoclax en la degración de gelatina de células de cáncer colorrectal. Porcentaje de degradación celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 5. Efecto de Venetoclax en la generación de trombina. Valores del tiempo hasta el inicio del pico (Lagtime) y el tiempo en alcanzar el pico máximo (ttPeak) en las células Caco-2-HPN en presencia o ausencia de Venetoclax. Fig .6. Efecto de Venetoclax en el ciclo celular de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN en las diferentes fases del ciclo celular (G0/G1, S, G2/M) en presencia o ausencia de venetoclax. Fig. 7. Efecto de Venetoclax en la proliferación de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN que están proliferando (EdU+) en presencia o ausencia de Venetoclax. DESCRIPCIÓN DE LA INVENCIÓN La presente invención se refiere al Venetoclax y a cualquiera de sus sales, formas en estado sólido y solvatos para su uso en el tratamiento del cáncer cáncer colorrectal, y aún más preferiblemente del cáncer colorrectal metastásico. USO MÉDICO DEL COMPUESTO DE LA INVENCIÓN Por tanto, un primer aspecto de la invención se al Venetoclax, de ahora en adelante compuesto de la invención, o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer gastrointestinal. Venetoclax, es una molécula de nombre IUPAC 4- (4 - {[2- (4-clorofenil) -4, 4-dimetilciclohex-1-en-l- il] metil} piperazin-1 -il) -N - ({3 -nitro-4- [ (tetrahidro-2H-piran-4-ilmetil) amino] fenil} sulfonil) -2- (1H-pirrolo [2, 3-b] piridin-5-iloxi) benzamida, de fórmula (I) y número CAS 1257044-40-8 Fórmula (I) En esta memoria Venetoclax también incluye cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus ombinaciones, así como todas las formas en estado sólido de Venetoclax conocidas y composiciones farmacéuticas de las mismas. Venetoclax se describe en varios documentos de patentes, donde se indica que la sobreexpresión de proteínas Bcl-2 se correlaciona con la resistencia a la quimioterapia, el resultado clínico, la progresión de la enfermedad, el pronóstico general o una combinación de los mismos en varios cánceres y trastornos del sistema inmunológico. Por tanto, es necesario el desarrollo de compuestos que inhiban la actividad de las proteínas Bcl-2 antiapoptóticas, como el Venetoclax, aprobado para el tratamiento de la leucemia linfocítica crónica cuyos tumores tienen una alteración genética específica. Sin embargo, una disminución progresiva en su expresión durante la progresión del tumor indica un papel menor en la supervivencia y resistencia al CCR (Maurer CA et al., 1998. Dig Dis Sci 43 (12) :2641-2648; Flohil CC et al., 1996. J Pathol 178 (4) :393-397; Hawkins N et al., 1997. Tumour Biol 18 (3) :146-156; Kaklamanis L et al., 1996. J Pathol 179 (1) :1014; Kikuchi Y et al., 1997. Virchows Arch 431 (2) :111-117; Nakamura T et al., 1995. Pathol Int 45 (10) :721-728; Watson AJ et al., 1996. Br J Cáncer 73 (8) :889-895; van der Heijden M et al., 2016. Nat Commun 7:10916; Ofner D et al., 1995. Br J Cancer 72 (4) :981-985) , y un metaanálisis reciente (Huang Q et al., 2017. World J Gastroenterol.23 (27) :5018-5033, que es el tipo de estudio que aporta el mayor grado de evidencia, concluye que la alta expresión de la proteína antiapoptótica Bcl-2 es un factor de buen pronóstico en el cáncer colorrectal. Además, hasta el momento, de los 344 ensayos clínicos localizados en distintas bases de datos a fecha de enero de 2021, no hay ninguno en el que se emplee el Venetoclax para el tratamiento del cáncer gastrointestinal o colorrectal. Ningún experto en la materia se vería proclive a emplear Venetoclax en este tipo de cánceres. Las proteasas pericelulares han sido ampliamente implicadas en carcinogénesis, no solo porque actúan como enzimas capaces de degradar la matriz extracelulares, permitiendo así a las células tumorales romper la membrana basal e invadir el tejido circundante, sino que son capaces de actuar como modificadores proteolíticos de factores de crecimiento y receptores activados por proteasas que son críticos para la activación de rutas de señalización tumoral (PMID: 27870503 Tanabe et al. FEBS J. 2017 May;284 (10) :1421-1436) . Entre estas proteasas se encuentra hepsina, que pertenece a la super familia de serín proteasas transmembrana de tipo II (TTSP) . Hepsina se encuentra sobreexpresada en cáncer de próstata y sus niveles elevados son indicativos de mal pronóstico y recaida tras prostatectomía radical (PMID: 18927246 Sardana et al. Clin Chem. 2008 Dec;54 (12) :1951-60) . También se ha demostrado su obreexpresión en cáncer de ovario (PMID: 18726901 Miao et al. Int J Cáncer. 2008 Nov 1;123 (9) :2041-7) y cáncer de mama (PMID: 21383634) . Recientemente se ha descrito que la hepsina se encuentra elevada en suero de pacientes con cáncer colorrectal metastásico con respecto a pacientes con tumor primario. Aunque aún no existen datos que relacionen su expresión con metástasis en cáncer colorrectal. El desarrollo de eventos tromboembólicos venosos (ETEV) es un problema común en los tumores digestivos. La incidencia acumulada de ETEV en series modernas varía entre 12-20% (PMID: 26738412 Posch et al. Thromb Haemost. 2016 Apr;115 (4) :817-26) , dependiendo de las disparidades en las características de los pacientes en cada estudio y el contexto en el que la evaluación es llevada a cabo. La trombogénesis se atribuye a una combinación de factores clínicos y biológicos, que incluyen la activación del sistema hemostático por parte del tumor y la toxicidad vascular de la quimioterapia. La trombosis se asocia con una mayor morbilidad y mortalidad en estos pacientes (PMID: 28267709 Carmona-Bayonas et al. Br J Cáncer. 2017 Apr 11;116 (8) :994-1001, PMID: 22475313 Kline et al. Thromb Res. 2012 May;129 (5) :e194-9) y es uno de los eventos adversos más importantes en los ensayos clínicos de terapia anti-neoplásica. Tal como se muestra en los ejemplos de la invención, sorprendentemente, los inventores han demostrado mediante un ensayo fluorogénico la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina, así como la capacidad de Veneoclax de reducir la migración y la invasión de células de cáncer colorrectal. También han demostrado que reduce la generación de trombina en plasma procedente de sujetos sanos tras la incubación con células de cáncer colorrectal, y que reduce la generación de trombina en plasma de pacientes con cáncer colorrectal. Por tanto, otro aspecto de la invención se refiere al Venetoclax (compuesto de fórmula I) o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer colorrectal en un individuo. Más preferiblemente el cáncer colorrectal es el cáncer colorrectal metastásico. Aún más preferiblemente el individuo muestra los niveles de hepsina elevados con respecto a los valores normales. Los métodos para examinar los niveles de expresión de la proteína hepsina en muestras biológicas, y en particular en muestras de tejidos, son ampliamente conocidos en el stado de la técnica, por ejemplo, mediante métodos inmunohistoquímicos y/o el western blot. Los compuestos de la presente invención representados por la fórmula (I) pueden incluir isómeros, dependiendo de la presencia de enlaces múltiples, incluyendo isómeros ópticos o enantiómeros, dependiendo de la presencia de centros quirales. Los isómeros, enantiómeros o diastereoisómeros individuales y las mezclas de los mismos caen dentro del alcance de la presente invención, es decir, el término isómero también se refiere a cualquier mezcla de isómeros, como diastereómeros, racémicos, etc., incluso a sus isómeros ópticamente activos o las mezclas en distintas proporciones de los mismos. Los enantiómeros o diastereoisómeros individuales, así como sus mezclas, pueden separarse mediante técnicas convencionales. Asimismo, dentro del alcance de esta invención se encuentran los profármacos de los compuestos de fórmula (I) . El término "prodroga" o "profármaco" tal como aquí se utiliza incluye cualquier derivado de un compuesto de fórmula (I) -por ejemplo y no limitativamente: ésteres (incluyendo ésteres de ácidos carboxílicos, ésteres de aminoácidos, ésteres de fosfato, ésteres de sulfonato de sales metálicas, etc.) , carbamatos, amidas, etc.- que al ser administrado a un individuo puede ser transformado directa o indirectamente en dicho compuesto de fórmula (I) en el mencionado individuo. Ventajosamente, dicho derivado es un compuesto que aumenta la biodisponibilidad del compuesto de fórmula (I) cuando se administra a un individuo o que potencia la liberación del compuesto de fórmula (I) en un compartimento biológico. La naturaleza de dicho derivado no es crítica siempre y cuando pueda ser administrado a un individuo y proporcione el compuesto de fórmula (I) en un compartimento biológico de un individuo. La preparación de dicho profármaco puede llevarse a cabo mediante métodos convencionales conocidos por los expertos en la materia. Tal como aquí se utiliza, el término "derivado" incluye tanto a compuestos farmacéuticamente aceptables, es decir, derivados del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como derivados farmacéuticamente no aceptables, ya que éstos pueden ser útiles en la preparación de derivados farmacéuticamente aceptables. Los compuestos de la invención pueden estar en forma cristalina como compuestos libres o como solvatos. En este sentido, el término "solvato", tal como aquí se utiliza, incluye tanto solvatos farmacéuticamente aceptables, es decir, solvatos del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como olvatos farmacéuticamente no aceptables, los cuales pueden ser útiles en la preparación de solvatos o sales farmacéuticamente aceptables. La naturaleza del solvato farmacéuticamente aceptable no es crítica siempre y cuando sea farmacéuticamente aceptable. En una realización particular, el solvato es un hidrato. Los solvatos pueden obtenerse por métodos convencionales de solvatación conocidos por los expertos en la materia. Para su aplicación en terapia, los compuestos de fórmula (I) , sus sales, profármacos o solvatos, se encontrarán, preferentemente, en una forma farmacéuticamente aceptable o sustancialmente pura, es decir, que tiene un nivel de pureza farmacéuticamente aceptable excluyendo los aditivos farmacéuticos normales tales como diluyentes y portadores, y no incluyendo material considerado tóxico a niveles de dosificación normales. Los niveles de pureza para el principio activo son preferiblemente superiores al 50%, más preferiblemente superiores al 70%, y todavía más preferiblemente superiores al 90%. En una realización preferida, son superiores al 95% de compuesto de fórmula (I) , o de sus sales, solvatos o profármacos. COMPOSICIONES Y FORMAS FARMACÉUTICAS DE LA INVENCIÓN Otro aspecto de la invención se refiere a una composición, de ahora en adelante composición de la invención, que comprenden al menos el compuesto de la invención o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para su uso para la prevención, mejora alivio y/o tratamiento del cáncer gastrointestinal en un individuo. En una realización preferida de este aspecto de la invención es el cáncer colorrectal metastásico. Aún más preferiblemente el individuo presenta los niveles de hepsina elevados con respecto a los valores normales. En otra realización preferida de este aspecto, la composición de la invención es una composición farmacéutica. además, comprende un transportador o carrier farmacéuticamente aceptable, un excipiente y/o un vehículo farmacéuticamente aceptable. En otra realización preferida de este aspecto, la composición de la invención comprende, como único principio activo, el compuesto de fórmula (I) de la invención (Venetoclax) en una cantidad terapéuticamente efectiva, aunque puede comprender otros excipientes y/o vehículos farmacéuticamente aceptables. En el sentido utilizado en esta descripción, la expresión "cantidad terapéuticamente efectiva" se refiere a la cantidad del agente o compuesto capaz de desarrollar la acción terapéutica determinada por sus propiedades farmacológicas, calculada para producir el efecto deseado y, en general, vendrá determinada, entre otras causas, por las características propias de los compuestos, incluyendo la edad, estado del paciente, la severidad de la alteración o trastorno, y de la ruta y frecuencia de administración. Los compuestos descritos en la presente invención, sus sales, profármacos y/o solvatos así como las composiciones farmacéuticas que los contienen pueden ser utilizados junto con otros fármacos, o principios activos, adicionales para proporcionar una terapia de combinación. Dichos fármacos adicionales pueden formar parte de la misma composición farmacéutica o, alternativamente, pueden ser proporcionados en forma de una composición separada para su administración simultánea o no a la de la composición farmacéutica que comprende un compuesto de fórmula (I) , o una sal, profármaco o solvato del mismo. Por tanto, en otra realización preferida, la composición farmacéutica además comprende otro (u otros) principio activo. Más preferiblemente, el principio activo se selecciona de la lista que consiste en: agentes antiangiogénicos, terapias frente a EGFR, inhibidores de kinasa, agentes quimioterápicos, agentes inmunoterapéuticos, agentes frente a dianas moleculares, o cualquiera de sus combinaciones, para el tratamiento del cáncer colorrectal. En otra realización preferida los agentes antiangiogénicos se seleccionan de entre: Bevacizumab, Ziv-Aflibercept, Ramucirumab o cualquiera de sus combinaciones. En otra realización preferida las terapias frente a EGFR se seleccionan de entre: Cetuximab, Panitumumab o sus combinaciones. En otra realización preferida el inhibidor de kinasa es el Regofarenib. En otra realización preferida los agentes quimioterápicos se seleccionan de entre: Trifluridine +Tipiracil, Tegafur + Gimeracil + Oteracil, o sus combinaciones. En otra realización preferida los agentes inmunoterapéuticos se seleccionan de entre: Lefitolimod (MGN-1703) , Pembrolizumab, Atezolizumab o cualquiera de sus combinaciones. En otra realización preferida los agentes frente a dianas moleculares se seleccionan de entre: Encorafenib (LGX-818) + Binimetinib (MEK-162) , Napabucasin (BBI-608) , Vargatef (Nintedanib) , Masitinib (AB-1010) , Fruquintinib (HMPL-013) , Famitinib (SHR-1020) , Donafenib (CM-4307) , o cualquiera de sus combinaciones. Otro aspecto de la invención se refiere a una forma farmacéutica, de ahora en adelante forma farmacéutica de la invención, que comprende el compuesto de la invención o la composición de la invención. En esta memoria se entiende por "forma farmacéutica" la mezcla de uno o más principios activos con o sin aditivos que presentan características físicas para su adecuada dosificación, conservación, administración y biodisponibilidad. En otra realización preferida de la presente invención, las composiciones y formas farmacéuticas de la invención son adecuadas para la administración oral, en forma sólida o líquida. Las posibles formas para la administración oral son tabletas, cápsulas, siropes o soluciones y pueden contener excipientes convencionales conocidos en el ámbito farmacéutico, como agentes agregantes, rellenos, disgregantes o un surfactante farmacéuticamente aceptable. Otras formas farmacéuticas pueden ser los sistemas coloidales, dentro de los cuales se incluyen nanoemulsiones, nanocápsulas y nanopartículas poliméricas. Las composiciones para administración oral pueden ser preparadas por métodos los convencionales de Farmacia Galénica, como mezcla y dispersión. Las tabletas se pueden recubrir siguiendo métodos conocidos en la industria farmacéutica. Las composiciones y formas farmacéuticas se pueden adaptar para la administración parenteral, como soluciones estériles, suspensiones, o liofilizados de los productos de la invención, empleando la dosis adecuada. Se pueden emplear excipientes adecuados, como agentes tamponadores del pH o surfactantes. Las formulaciones anteriormente mencionadas pueden ser preparadas usando métodos convencionales, como los descritos en las Farmacopeas de diferentes países y en otros textos de referencia. El término "medicamento", tal y como se usa en esta memoria, hace referencia a cualquier sustancia usada para prevención, diagnóstico, alivio, tratamiento o curación de enfermedades en el hombre y los animales. La administración de los compuestos, composiciones o formas farmacéuticas de la presente invención puede ser realizada mediante cualquier método adecuado, como la infusión intravenosa y las vías oral, tópica o parenteral. La administración oral es la preferida por la conveniencia de los pacientes y por el carácter crónico de las enfermedades a tratar. La cantidad administrada de un compuesto de la presente invención dependerá de la relativa eficacia del compuesto elegido, la severidad de la enfermedad a tratar y el peso del paciente. Sin embargo, los compuestos de esta invención serán administrados una o más veces al día, por ejemplo 1, 2, 3 ó 4 veces diarias, con una dosis total entre 0.1 y 1000 mg/Kg/día. Es importante tener en cuenta que puede ser necesario introducir variaciones en la dosis, dependiendo de la edad y de la condición del paciente, así como modificaciones en la vía de administración. Los compuestos y composiciones de la presente invención pueden ser empleados junto con otros medicamentos en terapias combinadas. Los otros fármacos pueden formar parte de la misma composición o de otra composición diferente, para su administración al mismo tiempo o en tiempos diferentes. A lo largo de la descripción y las reivindicaciones la palabra "comprende" y sus variantes no pretenden excluir otras características técnicas, aditivos, componentes o pasos. Para los expertos en la materia, otros objetos, ventajas y características de la invención se desprenderán en parte de la descripción y en parte de la práctica de la invención. Los siguientes ejemplos y figuras se proporcionan a modo de ilustración, y no se pretende que sean limitativos de la presente invención. EJEMPLOS DE LA INVENCIÓN Cribado virtual Con el objetivo de encontrar nuevos inhibidores para la hepsina se realizó un cribado virtual mediante la técnica de docking molecular a partir de la estructura cristalográfica de la proteína depositada en la Protein Data Bank con código 1P57 frente a la librería de compuestos DrugBank (https://go.drugbank.com/) en las coordenadas de su sitio catalítico, caracterizada por residuos HIS57, ASP102 y SER195. El docking molecular se realizó en un clúster de cónputo de alto rendimiento mediante el software Autodock Vina 1.1.2 (http://vina.scripps.edu/) y para ello se convirtieron tanto la estructura de la proteína como la librería de ligandos DrugBank al formato pdbqt mediante MGLTools. Una vez terminados los cálculos se priorizaron los compuestos en función de docking score y se examinaron visualmente los 8 primeros, seleccionando el compuesto Venetoclax (código DrugBank DB11581) con un docking score de -11 Kcal/mol e nteraciones hidrofóbicas con los residuos PRO-60, LEU-41, GLN-73 y una interacción mediante puente de hidrogeno con el residuo ASN143 como se aprecia en la Figura 1. En dicha figura podemos observar que venetoclax impide el acceso a la triada catalítica, representada en formato de superficie para sus tres residuos. Venetoclax actúa como inhibidor irreversible de hepsina. Mediante un ensayo fluorogénico se determinó la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina. Hepsina es una serín proteasas capaz de hidrolizar al sustrato BOC-Gln-Arg-Arg-AMC (Bachem, Barcelona, Spain) , de manera que es posible registrar la emisión de fluorescencia mediante un lector de placas con longitudes de onda de excitación y emisión de 380 nm y 460 nm, respectivamente. Para ello, se incubó hepsina (0.05 ^M) (R&D Systems, Madrid, Spain) en tampón 50 mM Tris-HCl, pH 9 buffer, con 200 ^M BOC-Gln-Arg-Arg-AMC y registramos la fluorescencia emitida durante 5 minutos. Para comprobar el efecto de Venetoclax, se llevaó a cabo la misma reacción, pero incubando previamente hepsina con Venetoclax durante 1 hora a 37°C y en distintas concentraciones que oscilaron entre 0.167 y 2.5 ^M. De esta forma calculamos el valor de IC50, o concentración de inhibidor a la que se alcanza la mitad de la velocidad máxima de hepsina en la hidrólisis de su sustrato, que fue de 0.48 ^M. Venetoclax reduce la migración de células de cáncer colorrectal Una vez que las células alcanzan confluencia, forman una monocapa. Mediante la eliminación de una tira de células 300-500 ^m de anchura con una punta de pipetea de 200 ^l, es posible evaluar la capacidad de migración de las células y el efecto de Venetoclax en este proceso. La capacidad de migración se evalúa en función del porcentaje de área ocupada tras 48 horas de incubación y se cuantifica utilizando el software ImageJ. Los resultados muestran que Venetoclax a una concentración de 1, 88 ^M reduce de forma significativa la migración de células Caco-2, tanto con expresión basal como con sobreexpresión de hepsina, mediante transfección estable de un plásmido que contiene el gen HPN. Venetoclax reduce la invasión de células de cáncer colorrectal Para evaluar la invasión se realizó un ensayo en el que se evaluó la capacidad de las células para degradar una matriz de gelatina. Para ello, se mezcló gelatina al 0.2% y rodamina (Invitrogen, Life Technologies, Madrid, Spain) , en una ratio 1:55 en tampón NaCl 61 mM, borohidrato sódico 50 mM y después dializamos toda la noche en PBS. Se prepararon cubres con la mezcla preparada cubriéndolos y se fijó la matriz con glutaraldehido 0.5% durante 15 min. Los cubres se lavaron con PBS y se añadieron las suspensiones de células Caco-2 o KATO-III durante 72 horas. Posteriormente se fijaron las células con formaldehído 3.7% y se incubaron con phalloidin (0, 01 mg/ml) y ProLongGold Antifade con DAPI (4', 6-diamino-2-phenylindole; ThermoFisher) . Las imágenes se tomaron con un microscopio confocal SP8 LEICA y se analizaron con ImageJ y se procesaron con Adobe Photoshop. Nuestros resultados mostraron que Venetoclax, a una concentración de 1, 88 ^M, reduce de forma significativa la degradación de la gelatina de células Caco-2 tanto con expresión basal como con sobreexpresión de hepsina. Venetoclax reduce la generación de trombina Puesto que hepsina activa al FVII y, por tanto, la cascada de la coagulación, podría contribuir al estado de hipercoagulabilidad de los pacientes con cáncer colorrectal con niveles elevados de hepsina. Para comprobar esta hipótesis, se incubó plasma procedente de 20 sujetos sanos, a los que se extrajo sangre citratada 3.8% mediante venopunción, con las células Caco-2 con sobreexpresión de hepsina. El plasma se centrifugó previamente a 2500 g 20 minutos. Para el ensayo de generación de trombina, se retiró el plasma incubado y se incubó con el reactivo LOW® (factor tisular: 1 pmol; fosfolípidos: 4 ^mol; Diagnostica Stago) en una placa de 96 pocillo. Todas las muestras se prepararon en duplicado. La coagulación en estas muestras se inició añadiendo cloruro cálcico en un tampón que contenía el sustrato fluorogénico FluCa-kit reagent® (Diagnostica Stago) . Para cada muestra individual se utilizó un calibrador de trombina. La fluorescencia se registró durante 60 min en un fluorímetro Fluoroskan Ascent (Thermolab Systems) y los datos se analizaron utilizando el software Thrombinoscope™ (version 5.0.0.742; Diagnostica Stago) . Se analizaron los siguientes parámetros: (a) lagtime, que indica el inicio de la fase de generación de trombina; (b) tiempo hasta alcanzar la máxima concentración de trombina (ttPeak) ; (c) concentración máxima de trombina (Peak) ; (d) índice de frecuencia media (MRI) de la fase de propagación de la generación de trombina calculada por la fórmula Peak/ (ttPeak - lag-time) y se expresa en nM/min; y (e) potencial endógeno de trombina (ETP) que muestra la actividad enzimática de trombina evaluada como el área bajo la curva. Los resultados muestran que Venetoclax reduce el potencial endógeno de trombina (ETP) , el pico máximo (peak) y la velocidad en alcanzar el pico mientras que provoca n incremento en el tiempo de inicio de la fase de generación de trombina (lag-time) y el tiempo en alcanzar el pico. Tabla 1. Valores promedios del test de generación de trombina. Venetoclax no afecta ni a la muerte celular, ni al ciclo celular ni a la proliferación Puesto que Venetoclax es un fármaco dirigido frente a Bcl-2, quisimos evaluar si la menor migración o invasión celular podría deberse a una mayor muerte, a la alteración del ciclo celular o a una menor proliferación celular. Para ello se incubaron las células (5x105 cells/ml) en placas de 6 pocillos en presencia o ausencia de Venetocláx tras 48 h. El tipo de muerte celular se determinó mediante el ensayo de anexina V/7-ADD (Anexin V Apoptosis Detection Kit FITC; eBiosciences, Thermo Fisher, Karlsruhe, Alemania; 7-ADD BD-Biosciences) siguiendo las instrucciones del fabricante. El ciclo celular se analizó tras tratar las células con RNAse y con ioduro de propidio (Invitrogen) . Para evaluar la actividad proliferativa de las células Caco-2, se añadió 5-etinil-2'-desoxiuridina (EdU) (Thermo Fisher Scientific) durante 48 h. Luego, se usaron alícuotas de las células tumorales para determinar el porcentaje de células positivas, es decir, Caco-2 o Caco-2-HPN-EdU+, detectadas por reacción de acoplamiento de azida fluorescente con EdU de acuerdo con el protocolo del fabricante (Click-iT; Thermo Fisher Scientific) . Los resultados mostraron que Venetoclax no afecta ni a la muerte (porcentajes en torno al 5%) ni a la proliferación celular ni al ciclo celular.
+ ES-2919898_B2 Nuevo tratamiento del cáncer colorrectal CAMPO DE LA INVENCIÓN La presente invención pertenece al campo de la biomedicina, y más concretamente se refiere a un nuevo tratamiento para el cáncer gastrointestinal, y más preferiblemente para el tratamiento del cáncer gástrico y el cáncer colorrectal. ESTADO DE LA TÉCNICA ANTERIOR El cáncer colorrectal es el tercer cáncer más común diagnosticado tanto en hombres como en mujeres. Tiene lugar en el colon y recto y se desarrolla lentamente a partir de pólipos adenomatosos. El crecimiento excesivo de la mucosa del colon genera estos pólipos que tienen una morfología pedunculada o sésil. El desarrollo de cáncer colorrectal puede tener lugar por diferentes vías. Entre ellas se encuentra la aparición de lesiones serradas con apariencia del epitelio en dientes de sierra y que ocurre en el colon proximal. Esta vía se detecta en un tercio de todos los cánceres colorrectales. Con respecto a la secuencia adenoma-carcinoma, se ha propuesto que la progresión desde adenomas pequeños a grandes adenomas o adenocarcinomas avanzados está mediada por múltiples rutas moleculares que incluyen la inestabilidad de microsatélites, la inestabilidad cromosómica y rutas epigenéticas. Es posible hacer una prevención precoz puesto que se ha estimado que al menos lleva 10 años que un pólipo se transforme en célula tumoral (PMID: 28842051 0ines et al. Best Pract Res Clin Gastroenterol. 2017 Aug;31 (4) :419-424) . El diagnóstico precoz mediante colonoscopia y detección de sangre oculta en heces, así como la mejora en los tratamientos ha contribuido a prolongar la supervivencia de los tumores colorrectales en la fase de curación, Sin embargo, la metástasis está presente en aproximadamente el 25% de los pacientes durante el diagnóstico y en total, el 50% de los pacientes con cáncer colorrectal desarrollará metástasis (PMID: 27672422 Ohhara et al. World J Gastrointest Oncol. 2016 Sep 15;8 (9) :642-55) . Debido a la heterogeneidad y naturaleza multifactorial del cáncer colorrectal han aumentado considerablemente en los últimos años estudios para identificar predictores clínicos y moleculares, así como factores pronósticos con potencial para mejorar el manejo de los pacientes (PMID: 26964802 Aran et al. Clin Colorectal Cáncer. 2016 Sep;15 (3) :195-203; PMID: 29139091 Bermejo et al. Drugs. 2018 Jan;78 (1) :1-18) . Tanto la incidencia como la mortalidad del cáncer colorrectal ha disminuido tanto para hombres como para mujeres desde 1970 debido a la detección precoz (PMID: 29313949 Siegel et al. CA Cáncer J Clin. 2018 Jan;68 (1) :7-30) . Sin embargo, aunque diferentes terapias estás disponibles para el cáncer colorrectal metastásico, los resultados no son óptimos debido a la heterogeneidad entre pacientes debido a características moleculares, respuesta a la terapia y presentación clínica (PMID: 25593032 Linnekamp et al. Cáncer Res. 2015 Jan 15;75 (2) :245-9) . Los tratamientos más comunes de estos tumores se basan en la cirugía, la quimioterapia, terapias dirigidas y el tratamiento hormonal sustitutivo. Al menos el 50% de los pacientes con cáncer colorrectal recaen tras la resección quirúrgica y finalmente mueren de enfermedad metastásica. A pesar de la quimioterapia adyuvante postoperatoria en estos pacientes para disminuir el riesgo de recurrencia, el tratamiento adyuvante no da beneficios en supervivencia, especialmente en pacientes diagnosticados con estadío I. La terapia dirigida está basada en anticuerpos monoclonales y pequeños inhibidores moleculares, que selectivamente bloquean la proliferación celular mediante la intervención con ciertas moléculas y proteínas sobreexpresadas requeridas para la expansión del tumor. De acuerdo a la clasificación Mesh, el cáncer colorrectal se encuentra incluido en los cánceres gastrointestinales. La clasificación es la siguiente: Neoplasms [C04] Neoplasms by Site [C04.588] o Digestive System Neoplasms [C04.588.274] Gastrointestinal Neoplasms [C04.588.274.476] Esophageal Neoplasms [C04.588.274.476.205]_ Esophageal Squamous Cell Carcinoma [C04.588.274.476.205.500] Intestinal Neoplasms [C04.588.274.476.411] Cecal Neoplasms [C04.588.274.476.411.184] Appendiceal Neoplasms [C04.588.274.476.411.184.290] Colorectal Neoplasms [C04.588.274.476.411.307], Adenomatous Polyposis Coli [C04.588.274.476.411.307.089], Colonic Neoplasms [C04.588.274.476.411.307.180], Colitis-Associated Neoplasms [C04.588.274.476.411.307.180.400 ] Sigmoid Neoplasms [C04.588.274.476.411.307.180.800 ] Colorectal Neoplasms, Hereditar y Nonpolyposis [C04.588.274.476.411.307.190] Rectal Neoplasms [C04.588.274.476.411.307.790], Anus Neoplasms [C04.588.274.476.411.307.790.040 L Anal Gland Neoplasms [C04.588.274.476.411.307. 790.040.040] Por tanto, es necesario desarrollar nuevos tratamientos para el cáncer colorrectal DESCRIPCIÓN DE LAS FIGURAS Fig. 1. Pose resultante del docking molecular entre Venetoclax y hepsina. Fig. 2. Cálculo del valor de IC50 de Venetoclax sobre la actividad de Hepsina. Velocidad máxima de la actividad de Hepsina en presencia de dosis crecientes de Venetoclax. Fig.3 . Efecto de Venetoclax en la migración de células de cáncer colorrectal. Porcentaje de migración celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 4. Efecto de Venetoclax en la degración de gelatina de células de cáncer colorrectal. Porcentaje de degradación celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 5. Efecto de Venetoclax en la generación de trombina. Valores del tiempo hasta el inicio del pico (Lagtime) y el tiempo en alcanzar el pico máximo (ttPeak) en las células Caco-2-HPN en presencia o ausencia de Venetoclax. Fig .6. Efecto de Venetoclax en el ciclo celular de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN en las diferentes fases del ciclo celular (G0/G1, S, G2/M) en presencia o ausencia de venetoclax. Fig. 7. Efecto de Venetoclax en la proliferación de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN que están proliferando (EdU+) en presencia o ausencia de Venetoclax. DESCRIPCIÓN DE LA INVENCIÓN La presente invención se refiere al Venetoclax y a cualquiera de sus sales, formas en estado sólido y solvatos para su uso en el tratamiento del cáncer cáncer colorrectal, y aún más preferiblemente del cáncer colorrectal metastásico. USO MÉDICO DEL COMPUESTO DE LA INVENCIÓN Por tanto, un primer aspecto de la invención se al Venetoclax, de ahora en adelante compuesto de la invención, o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer gastrointestinal. Venetoclax, es una molécula de nombre IUPAC 4- (4 - {[2- (4-clorofenil) -4, 4-dimetilciclohex-1-en-l- il] metil} piperazin-1 -il) -N - ({3 -nitro-4- [ (tetrahidro-2H-piran-4-ilmetil) amino] fenil} sulfonil) -2- (1H-pirrolo [2, 3-b] piridin-5-iloxi) benzamida, de fórmula (I) y número CAS 1257044-40-8 Fórmula (I) En esta memoria Venetoclax también incluye cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus ombinaciones, así como todas las formas en estado sólido de Venetoclax conocidas y composiciones farmacéuticas de las mismas. Venetoclax se describe en varios documentos de patentes, donde se indica que la sobreexpresión de proteínas Bcl-2 se correlaciona con la resistencia a la quimioterapia, el resultado clínico, la progresión de la enfermedad, el pronóstico general o una combinación de los mismos en varios cánceres y trastornos del sistema inmunológico. Por tanto, es necesario el desarrollo de compuestos que inhiban la actividad de las proteínas Bcl-2 antiapoptóticas, como el Venetoclax, aprobado para el tratamiento de la leucemia linfocítica crónica cuyos tumores tienen una alteración genética específica. Sin embargo, una disminución progresiva en su expresión durante la progresión del tumor indica un papel menor en la supervivencia y resistencia al CCR (Maurer CA et al., 1998. Dig Dis Sci 43 (12) :2641-2648; Flohil CC et al., 1996. J Pathol 178 (4) :393-397; Hawkins N et al., 1997. Tumour Biol 18 (3) :146-156; Kaklamanis L et al., 1996. J Pathol 179 (1) :1014; Kikuchi Y et al., 1997. Virchows Arch 431 (2) :111117; Nakamura T et al., 1995. Pathol Int 45 (10) :721-728; Watson AJ et al., 1996. Br J Cáncer 73 (8) :889-895; van der Heijden M et al., 2016. Nat Commun 7:10916; Ofner D et al., 1995. Br J Cancer 72 (4) :981-985) , y un metaanálisis reciente (Huang Q et al., 2017. World J Gastroenterol.23 (27) :5018-5033, que es el tipo de estudio que aporta el mayor grado de evidencia, concluye que la alta expresión de la proteína antiapoptótica Bcl-2 es un factor de buen pronóstico en el cáncer colorrectal. Además, hasta el momento, de los 344 ensayos clínicos localizados en distintas bases de datos a fecha de enero de 2021, no hay ninguno en el que se emplee el Venetoclax para el tratamiento del cáncer gastrointestinal o colorrectal. Ningún experto en la materia se vería proclive a emplear Venetoclax en este tipo de cánceres. Las proteasas pericelulares han sido ampliamente implicadas en carcinogénesis, no solo porque actúan como enzimas capaces de degradar la matriz extracelulares, permitiendo así a las células tumorales romper la membrana basal e invadir el tejido circundante, sino que son capaces de actuar como modificadores proteolíticos de factores de crecimiento y receptores activados por proteasas que son críticos para la activación de rutas de señalización tumoral (PMID: 27870503 Tanabe et al. FEBS J. 2017 May;284 (10) :1421-1436) . Entre estas proteasas se encuentra hepsina, que pertenece a la super familia de serín proteasas transmembrana de tipo II (TTSP) . Hepsina se encuentra sobreexpresada en cáncer de próstata y sus niveles elevados son indicativos de mal pronóstico y recaida tras prostatectomía radical (PMID: 18927246 Sardana et al. Clin Chem. 2008 Dec;54 (12) :1951-60) . También se ha demostrado su obreexpresión en cáncer de ovario (PMID: 18726901 Miao et al. int J Cáncer, 2008 Nov 1;123 (9) :2041-7) y cáncer de mama (PMID: 21383634) . Recientemente se ha descrito que la hepsina se encuentra elevada en suero de pacientes con cáncer colorrectal metastásico con respecto a pacientes con tumor primario. Aunque aún no existen datos que relacionen su expresión con metástasis en cáncer colorrectal. El desarrollo de eventos tromboembólicos venosos (ETEV) es un problema común en los tumores digestivos. La incidencia acumulada de ETEV en series modernas varía entre 12-20% (PMID: 26738412 Posch et al. Thromb Haemost. 2016 Apr;115 (4) :817-26) , dependiendo de las disparidades en las características de los pacientes en cada estudio y el contexto en el que la evaluación es llevada a cabo. La trombogénesis se atribuye a una combinación de factores clínicos y biológicos, que incluyen la activación del sistema hemostático por parte del tumor y la toxicidad vascular de la quimioterapia. La trombosis se asocia con una mayor morbilidad y mortalidad en estos pacientes (PMID: 28267709 Carmona-Bayonas et al. Br J Cáncer. 2017 Apr 11;116 (8) :994-1001, PMID: 22475313 Kline et al. Thromb Res. 2012 May;129 (5) :e194-9) y es uno de los eventos adversos más importantes en los ensayos clínicos de terapia anti-neoplásica. Tal como se muestra en los ejemplos de la invención, sorprendentemente, los inventores han demostrado mediante un ensayo fluorogénico la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina, así como la capacidad de Veneoclax de reducir la migración y la invasión de células de cáncer colorrectal. También han demostrado que reduce la generación de trombina en plasma procedente de sujetos sanos tras la incubación con células de cáncer colorrectal, y que reduce la generación de trombina en plasma de pacientes con cáncer colorrectal. Por tanto, otro aspecto de la invención se refiere al Venetoclax (compuesto de fórmula I) o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer colorrectal en un individuo, donde dicho individuo muestra los niveles de hepsina elevados con respecto a los valores normales. Más preferiblemente el cáncer colorrectal es el cáncer colorrectal metastásico. Los métodos para examinar los niveles de expresión de la proteína hepsina en muestras biológicas, y en particular en muestras de tejidos, son ampliamente conocidos en el stado de la técnica, por ejemplo, mediante métodos inmunohistoquímicos y/o el western blot. Los compuestos de la presente invención representados por la fórmula (I) pueden incluir isómeros, dependiendo de la presencia de enlaces múltiples, incluyendo isómeros ópticos o enantiómeros, dependiendo de la presencia de centros quirales. Los isómeros, enantiómeros o diastereoisómeros individuales y las mezclas de los mismos caen dentro del alcance de la presente invención, es decir, el término isómero también se refiere a cualquier mezcla de isómeros, como diastereómeros, racémicos, etc., incluso a sus isómeros ópticamente activos o las mezclas en distintas proporciones de los mismos. Los enantiómeros o diastereoisómeros individuales, así como sus mezclas, pueden separarse mediante técnicas convencionales. Asimismo, dentro del alcance de esta invención se encuentran los profármacos de los compuestos de fórmula (I) . El término "prodroga" o "profármaco" tal como aquí se utiliza incluye cualquier derivado de un compuesto de fórmula (I) -por ejemplo y no limitativamente: ésteres (incluyendo ésteres de ácidos carboxílicos, ésteres de aminoácidos, ésteres de fosfato, ésteres de sulfonato de sales metálicas, etc.) , carbamatos, amidas, etc.- que al ser administrado a un individuo puede ser transformado directa o indirectamente en dicho compuesto de fórmula (I) en el mencionado individuo. Ventajosamente, dicho derivado es un compuesto que aumenta la biodisponibilidad del compuesto de fórmula (I) cuando se administra a un individuo o que potencia la liberación del compuesto de fórmula (I) en un compartimento biológico. La naturaleza de dicho derivado no es crítica siempre y cuando pueda ser administrado a un individuo y proporcione el compuesto de fórmula (I) en un compartimento biológico de un individuo. La preparación de dicho profármaco puede llevarse a cabo mediante métodos convencionales conocidos por los expertos en la materia. Tal como aquí se utiliza, el término "derivado" incluye tanto a compuestos farmacéuticamente aceptables, es decir, derivados del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como derivados farmacéuticamente no aceptables, ya que éstos pueden ser útiles en la preparación de derivados farmacéuticamente aceptables. Los compuestos de la invención pueden estar en forma cristalina como compuestos libres o como solvatos. En este sentido, el término "solvato", tal como aquí se utiliza, incluye tanto solvatos farmacéuticamente aceptables, es decir, solvatos del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como olvatos farmacéuticamente no aceptables, los cuales pueden ser útiles en la preparación de solvatos o sales farmacéuticamente aceptables. La naturaleza del solvato farmacéuticamente aceptable no es crítica siempre y cuando sea farmacéuticamente aceptable. En una realización particular, el solvato es un hidrato. Los solvatos pueden obtenerse por métodos convencionales de solvatación conocidos por los expertos en la materia. Para su aplicación en terapia, los compuestos de fórmula (I) , sus sales, profármacos o solvatos, se encontrarán, preferentemente, en una forma farmacéuticamente aceptable o sustancialmente pura, es decir, que tiene un nivel de pureza farmacéuticamente aceptable excluyendo los aditivos farmacéuticos normales tales como diluyentes y portadores, y no incluyendo material considerado tóxico a niveles de dosificación normales. Los niveles de pureza para el principio activo son preferiblemente superiores al 50%, más preferiblemente superiores al 70%, y todavía más preferiblemente superiores al 90%. En una realización preferida, son superiores al 95% de compuesto de fórmula (I) , o de sus sales, solvatos o profármacos. COMPOSICIONES Y FORMAS FARMACÉUTICAS DE LA INVENCIÓN Otro aspecto de la invención se refiere a una composición, de ahora en adelante composición de la invención, que comprenden al menos el compuesto de la invención o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para su uso para la prevención, mejora alivio y/o tratamiento del cáncer gastrointestinal en un individuo. En una realización preferida de este aspecto de la invención es el cáncer colorrectal metastásico. Aún más preferiblemente el individuo presenta los niveles de hepsina elevados con respecto a los valores normales. En otra realización preferida de este aspecto, la composición de la invención es una composición farmacéutica. además, comprende un transportador o carrier farmacéuticamente aceptable, un excipiente y/o un vehículo farmacéuticamente aceptable. En otra realización preferida de este aspecto, la composición de la invención comprende, como único principio activo, el compuesto de fórmula (I) de la invención (Venetoclax) en una cantidad terapéuticamente efectiva, aunque puede comprender otros excipientes y/o vehículos farmacéuticamente aceptables. En el sentido utilizado en esta descripción, la expresión "cantidad terapéuticamente efectiva" se refiere a la cantidad del agente o compuesto capaz de desarrollar la acción terapéutica determinada por sus propiedades farmacológicas, calculada para producir el efecto deseado y, en general, vendrá determinada, entre otras causas, por las características propias de los compuestos, incluyendo la edad, estado del paciente, la severidad de la alteración o trastorno, y de la ruta y frecuencia de administración. Los compuestos descritos en la presente invención, sus sales, profármacos y/o solvatos así como las composiciones farmacéuticas que los contienen pueden ser utilizados junto con otros fármacos, o principios activos, adicionales para proporcionar una terapia de combinación. Dichos fármacos adicionales pueden formar parte de la misma composición farmacéutica o, alternativamente, pueden ser proporcionados en forma de una composición separada para su administración simultánea o no a la de la composición farmacéutica que comprende un compuesto de fórmula (I) , o una sal, profármaco o solvato del mismo. Por tanto, en otra realización preferida, la composición farmacéutica además comprende otro (u otros) principio activo. Más preferiblemente, el principio activo se selecciona de la lista que consiste en: agentes antiangiogénicos, terapias frente a EGFR, inhibidores de kinasa, agentes quimioterápicos, agentes inmunoterapéuticos, agentes frente a dianas moleculares, o cualquiera de sus combinaciones, para el tratamiento del cáncer colorrectal. En otra realización preferida los agentes antiangiogénicos se seleccionan de entre: Bevacizumab, Ziv-Aflibercept, Ramucirumab o cualquiera de sus combinaciones. En otra realización preferida las terapias frente a EGFR se seleccionan de entre: Cetuximab, Panitumumab o sus combinaciones. En otra realización preferida el inhibidor de kinasa es el Regofarenib. En otra realización preferida los agentes quimioterápicos se seleccionan de entre: Trifluridine +Tipiracil, Tegafur + Gimeracil + Oteracil, o sus combinaciones. En otra realización preferida los agentes inmunoterapéuticos se seleccionan de entre: Lefitolimod (MGN-1703) , Pembrolizumab, Atezolizumab o cualquiera de sus combinaciones. En otra realización preferida los agentes frente a dianas moleculares se seleccionan de entre: Encorafenib (LGX-818) + Binimetinib (MEK-162) , Napabucasin (BBI-608) , Vargatef (Nintedanib) , Masitinib (AB-1010) , Fruquintinib (HMPL-013) , Famitinib (SHR-1020) , Donafenib (CM-4307) , o cualquiera de sus combinaciones. Otro aspecto de la invención se refiere a una forma farmacéutica, de ahora en adelante forma farmacéutica de la invención, que comprende el compuesto de la invención o la composición de la invención. En esta memoria se entiende por "forma farmacéutica" la mezcla de uno o más principios activos con o sin aditivos que presentan características físicas para su adecuada dosificación, conservación, administración y biodisponibilidad. En otra realización preferida de la presente invención, las composiciones y formas farmacéuticas de la invención son adecuadas para la administración oral, en forma sólida o líquida. Las posibles formas para la administración oral son tabletas, cápsulas, siropes o soluciones y pueden contener excipientes convencionales conocidos en el ámbito farmacéutico, como agentes agregantes, rellenos, disgregantes o un surfactante farmacéuticamente aceptable. Otras formas farmacéuticas pueden ser los sistemas coloidales, dentro de los cuales se incluyen nanoemulsiones, nanocápsulas y nanopartículas poliméricas. Las composiciones para administración oral pueden ser preparadas por métodos los convencionales de Farmacia Galénica, como mezcla y dispersión. Las tabletas se pueden recubrir siguiendo métodos conocidos en la industria farmacéutica. Las composiciones y formas farmacéuticas se pueden adaptar para la administración parenteral, como soluciones estériles, suspensiones, o liofilizados de los productos de la invención, empleando la dosis adecuada. Se pueden emplear excipientes adecuados, como agentes tamponadores del pH o surfactantes. Las formulaciones anteriormente mencionadas pueden ser preparadas usando métodos convencionales, como los descritos en las Farmacopeas de diferentes países y en otros textos de referencia. El término "medicamento", tal y como se usa en esta memoria, hace referencia a cualquier sustancia usada para prevención, diagnóstico, alivio, tratamiento o curación de enfermedades en el hombre y los animales. La administración de los compuestos, composiciones o formas farmacéuticas de la presente invención puede ser realizada mediante cualquier método adecuado, como la infusión intravenosa y las vías oral, tópica o parenteral. La administración oral es la preferida por la conveniencia de los pacientes y por el carácter crónico de las enfermedades a tratar. La cantidad administrada de un compuesto de la presente invención dependerá de la relativa eficacia del compuesto elegido, la severidad de la enfermedad a tratar y el peso del paciente. Sin embargo, los compuestos de esta invención serán administrados una o más veces al día, por ejemplo 1, 2, 3 ó 4 veces diarias, con una dosis total entre 0.1 y 1000 mg/Kg/día. Es importante tener en cuenta que puede ser necesario introducir variaciones en la dosis, dependiendo de la edad y de la condición del paciente, así como modificaciones en la vía de administración. Los compuestos y composiciones de la presente invención pueden ser empleados junto con otros medicamentos en terapias combinadas. Los otros fármacos pueden formar parte de la misma composición o de otra composición diferente, para su administración al mismo tiempo o en tiempos diferentes. A lo largo de la descripción y las reivindicaciones la palabra "comprende" y sus variantes no pretenden excluir otras características técnicas, aditivos, componentes o pasos. Para los expertos en la materia, otros objetos, ventajas y características de la invención se desprenderán en parte de la descripción y en parte de la práctica de la invención. Los siguientes ejemplos y figuras se proporcionan a modo de ilustración, y no se pretende que sean limitativos de la presente invención. EJEMPLOS DE LA INVENCIÓN Cribado virtual Con el objetivo de encontrar nuevos inhibidores para la hepsina se realizó un cribado virtual mediante la técnica de docking molecular a partir de la estructura cristalográfica de la proteína depositada en la Protein Data Bank con código 1P57 frente a la librería de compuestos DrugBank (https://go.drugbank.com/) en las coordenadas de su sitio catalítico, caracterizada por residuos HIS57, ASP102 y SER195. El docking molecular se realizó en un clúster de cónputo de alto rendimiento mediante el software Autodock Vina 1.1.2 (http://vina.scripps.edu/) y para ello se convirtieron tanto la estructura de la proteína como la librería de ligandos DrugBank al formato pdbqt mediante MGLTools. Una vez terminados los cálculos se priorizaron los compuestos en función de docking score y se examinaron visualmente los 8 primeros, seleccionando el compuesto Venetoclax (código DrugBank DB11581) con un docking score de -11 Kcal/mol e nteraciones hidrofóbicas con los residuos PRO-60, LEU-41, GLN-73 y una interacción mediante puente de hidrogeno con el residuo ASN143 como se aprecia en la Figura 1. En dicha figura podemos observar que venetoclax impide el acceso a la triada catalítica, representada en formato de superficie para sus tres residuos. Venetoclax actúa como inhibidor irreversible de hepsina. Mediante un ensayo fluorogénico se determinó la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina. Hepsina es una serín proteasas capaz de hidrolizar al sustrato BOC-Gln-Arg-Arg-AMC (Bachem, Barcelona, Spain) , de manera que es posible registrar la emisión de fluorescencia mediante un lector de placas con longitudes de onda de excitación y emisión de 380 nm y 460 nm, respectivamente. Para ello, se incubó hepsina (0.05 M) (R&D Systems, Madrid, Spain) en tampón 50 mM Tris-HCl, pH 9 buffer, con 200 M BOC-Gln-Arg-Arg-AMC y registramos la fluorescencia emitida durante 5 minutos. Para comprobar el efecto de Venetoclax, se llevaó a cabo la misma reacción, pero incubando previamente hepsina con Venetoclax durante 1 hora a 37°C y en distintas concentraciones que oscilaron entre 0.167 y 2.5 M. De esta forma calculamos el valor de IC5O, o concentración de inhibidor a la que se alcanza la mitad de la velocidad máxima de hepsina en la hidrólisis de su sustrato, que fue de 0.48 M. Venetoclax reduce la migración de células de cáncer colorrectal Una vez que las células alcanzan confluencia, forman una monocapa. Mediante la eliminación de una tira de células 300-500 m de anchura con una punta de pipetea de 200 l, es posible evaluar la capacidad de migración de las células y el efecto de Venetoclax en este proceso. La capacidad de migración se evalúa en función del porcentaje de área ocupada tras 48 horas de incubación y se cuantifica utilizando el software ImageJ. Los resultados muestran que Venetoclax a una concentración de 1, 88 M reduce de forma significativa la migración de células Caco-2, tanto con expresión basal como con sobreexpresión de hepsina, mediante transfección estable de un plásmido que contiene el gen HPN. Venetoclax reduce la invasión de células de cáncer colorrectal Para evaluar la invasión se realizó un ensayo en el que se evaluó la capacidad de las células para degradar una matriz de gelatina. Para ello, se mezcló gelatina al 0.2% y rodamina (Invitrogen, Life Technologies, Madrid, Spain) , en una ratio 1:55 en tampón NaCl 61 mM, borohidrato sódico 50 mM y después dializamos toda la noche en PBS. Se prepararon cubres con la mezcla preparada cubriéndolos y se fijó la matriz con glutaraldehido 0.5% durante 15 min. Los cubres se lavaron con PBS y se añadieron las suspensiones de células Caco-2 o KATO-III durante 72 horas. Posteriormente se fijaron las células con formaldehído 3.7% y se incubaron con phalloidin (0, 01 mg/ml) y ProLongGold Antifade con DAPI (4', 6-diamino-2-phenylindole; ThermoFisher) . Las imágenes se tomaron con un microscopio confocal SP8 LEICA y se analizaron con ImageJ y se procesaron con Adobe Photoshop. Nuestros resultados mostraron que Venetoclax, a una concentración de 1, 88 M, reduce de forma significativa la degradación de la gelatina de células Caco-2 tanto con expresión basal como con sobreexpresión de hepsina. Venetoclax reduce la generación de trombina Puesto que hepsina activa al FVII y, por tanto, la cascada de la coagulación, podría contribuir al estado de hipercoagulabilidad de los pacientes con cáncer colorrectal con niveles elevados de hepsina. Para comprobar esta hipótesis, se incubó plasma procedente de 20 sujetos sanos, a los que se extrajo sangre citratada 3.8% mediante venopunción, con las células Caco-2 con sobreexpresión de hepsina. El plasma se centrifugó previamente a 2500 g 20 minutos. Para el ensayo de generación de trombina, se retiró el plasma incubado y se incubó con el reactivo LOW® (factor tisular: 1 pmol; fosfolípidos: 4 mol; Diagnostica Stago) en una placa de 96 pocillo. Todas las muestras se prepararon en duplicado. La coagulación en estas muestras se inició añadiendo cloruro cálcico en un tampón que contenía el sustrato fluorogénico FluCa-kit reagent® (Diagnostica Stago) . Para cada muestra individual se utilizó un calibrador de trombina. La fluorescencia se registró durante 60 min en un fluorímetro Fluoroskan Ascent (Thermolab Systems) y los datos se analizaron utilizando el software Thrombinoscope™ (version 5.0.0.742; Diagnostica Stago) . Se analizaron los siguientes parámetros: (a) lagtime, que indica el inicio de la fase de generación de trombina; (b) tiempo hasta alcanzar la máxima concentración de trombina (ttPeak) ; (c) concentración máxima de trombina (Peak) ; (d) índice de frecuencia media (MRI) de la fase de propagación de la generación de trombina calculada por la fórmula Peak/ (ttPeak - lag-time) y se expresa en nM/min; y (e) potencial endógeno de trombina (ETP) que muestra la actividad enzimática de trombina evaluada como el área bajo la curva. Los resultados muestran que Venetoclax reduce el potencial endógeno de trombina (ETP) , el pico máximo (peak) y la velocidad en alcanzar el pico mientras que provoca n incremento en el tiempo de inicio de la fase de generación de trombina (lag-time) y el tiempo en alcanzar el pico. Tabla 1. Valores promedios del test de generación de trombina. Venetoclax no afecta ni a la muerte celular, ni al ciclo celular ni a la proliferación Puesto que Venetoclax es un fármaco dirigido frente a Bcl-2, quisimos evaluar si la menor migración o invasión celular podría deberse a una mayor muerte, a la alteración del ciclo celular o a una menor proliferación celular. Para ello se incubaron las células (5x105 cells/ml) en placas de 6 pocillos en presencia o ausencia de Venetocláx tras 48 h. El tipo de muerte celular se determinó mediante el ensayo de anexina V/7-ADD (Anexin V Apoptosis Detection Kit FITC; eBiosciences, Thermo Fisher, Karlsruhe, Alemania; 7-ADD BD-Biosciences) siguiendo las instrucciones del fabricante. El ciclo celular se analizó tras tratar las células con RNAse y con ioduro de propidio (Invitrogen) . Para evaluar la actividad proliferativa de las células Caco-2, se añadió 5-etinil-2'-desoxiuridina (EdU) (Thermo Fisher Scientific) durante 48 h. Luego, se usaron alícuotas de las células tumorales para determinar el porcentaje de células positivas, es decir, Caco-2 o Caco-2-HPN-EdU+, detectadas por reacción de acoplamiento de azida fluorescente con EdU de acuerdo con el protocolo del fabricante (Click-iT; Thermo Fisher Scientific) . Los resultados mostraron que Venetoclax no afecta ni a la muerte (porcentajes en torno al 5%) ni a la proliferación celular ni al ciclo celular.
Publicaciones:
ES2919898 (28/07/2022) - A1 Solicitud de patente con informe sobre el estado de la técnica
ES2919898 (13/10/2023) - B2 Patente de invención con examen
ES2919898 (02/02/2024) - B8 Corrección de la primera página de patente de invención
Eventos:
En fecha 27/01/2021 se realizó Registro Instancia de Solicitud
En fecha 27/01/2021 se realizó Admisión a Trámite
En fecha 27/01/2021 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 28/01/2021 se realizó 3406X_Solicitud Correcciones
En fecha 01/02/2021 se realizó 1551X_Notificación Correcciones Admitidas
En fecha 12/02/2021 se realizó Superado examen de oficio
En fecha 26/07/2021 se realizó 3406X_Solicitud Correcciones
En fecha 17/12/2021 se realizó Realizado IET
En fecha 22/12/2021 se realizó 1109P_Comunicación Traslado del IET
En fecha 11/03/2022 se realizó 1550X_Notificación Rechazo Correcciones
En fecha 17/03/2022 se realizó Publicación Rechazo Correcciones
En fecha 23/03/2022 se realizó Registro Documentación no Identificada
En fecha 28/07/2022 se realizó Publicación Solicitud
En fecha 28/07/2022 se realizó Publicación Folleto Solicitud con IET (A1)
En fecha 27/10/2022 se realizó PETEX_Petición de examen sustantivo
En fecha 14/11/2022 se realizó Validación petición y/o pago de examen sustantivo conforme
En fecha 23/03/2023 se realizó El solicitante ha contestado pero existen nuevas objeciones a la concesión de la solicitud
En fecha 23/03/2023 se realizó Elaboración de examen sustantivo
En fecha 23/03/2023 se realizó 6120P_Notificación de examen sustantivo
En fecha 29/03/2023 se realizó Publicación de examen sustantivo
En fecha 29/05/2023 se realizó 3585X_Registro Solicitud Prórroga de Plazos
En fecha 29/05/2023 se realizó Concesión Prórroga de Plazos
En fecha 29/05/2023 se realizó 1585X_Notificación Concesión Prórroga de Plazos
En fecha 02/06/2023 se realizó Publicación Concesión Prórroga de Plazos (BOPI)
En fecha 12/06/2023 se realizó 5127P_Subsanación a defectos en examen sustantivo
En fecha 20/09/2023 se realizó Designación de Comisión de Expertos
En fecha 25/09/2023 se realizó Finalización de Examen Sustantivo
En fecha 25/09/2023 se realizó 6121P_Comunicación finalización de examen sustantivo
En fecha 29/09/2023 se realizó Publicación finalización de examen sustantivo
En fecha 05/10/2023 se realizó Concesión con examen sustantivo
En fecha 05/10/2023 se realizó Entrega título
En fecha 05/10/2023 se realizó 6125P_Notificación de concesión con examen sustantivo
En fecha 13/10/2023 se realizó Publicación concesión Patente
En fecha 13/10/2023 se realizó Publicación Folleto Concesión
En fecha 02/02/2024 se realizó Publicación de la Corrección de la primera pagina de la patente de invención (BOPI)
En fecha 02/02/2024 se realizó Publicación Folleto Corrección de la Primera Página de la Patente de Invención (B8)
Pagos:
27/01/2021 - Pago Tasas IET
16/10/2023 - Pago 03 Anualidad
28/02/2024 - Pago 04 Anualidad
+ ES-2919898_A11. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer gastrointestinal en un individuo. Fórmula (I) 2. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según la reivindicación anterior, donde el cáncer gastrointestinal es el cáncer colorrectal. 3. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según la reivindicación anterior, donde el cáncer colorrectal es el cáncer colorrectal metastásico. 4. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según cualquiera de las reivindicaciones 1-3, donde el individuo presenta los niveles de hepsina elevados con respecto a los niveles normales. 5. Una composición que comprende el compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según cualquiera de las reivindicaciones 1-4. 6. La composición según la reivindicación 5, que es una composición farmacéutica. 7. La composición según cualquiera de las reivindicaciones 5-6, donde la composición además comprende excipientes y/o un vehículo farmacéuticamente aceptable. 8. La composición según cualquiera de las reivindicaciones 5-7, donde la composición además comprende otro principio activo.
+ ES-2919898_B21. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso en la prevención, mejora, alivio y/o tratamiento del cáncer colorrectal en un individuo donde dicho individuo presenta los niveles de hepsina elevados con respecto a los niveles normales. Fórmula (I) 2. El compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según la reivindicación anterior, donde el cáncer colorrectal es el cáncer colorrectal metastásico.345 3. Una composición que comprende el compuesto de fórmula (I) o cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus combinaciones, para su uso según cualquiera de las reivindicaciones 1-2. 4. La composición según la reivindicación 3, que es una composición farmacéutica. 5. La composición según cualquiera de las reivindicaciones 3-4, donde la composición además comprende excipientes y/o un vehículo farmacéuticamente aceptable. 6. La composición según cualquiera de las reivindicaciones 3-5, donde la composición además comprende otro principio activo.
Los productos y servicios protegidos por este registro son:
A61K 31/496 - A61P 35/00
Descripciones:
+ ES-2919898_A1 Nuevo tratamiento del cáncer colorrectal CAMPO DE LA INVENCIÓN La presente invención pertenece al campo de la biomedicina, y más concretamente se refiere a un nuevo tratamiento para el cáncer gastrointestinal, y más preferiblemente para el tratamiento del cáncer gástrico y el cáncer colorrectal. ESTADO DE LA TÉCNICA ANTERIOR El cáncer colorrectal es el tercer cáncer más común diagnosticado tanto en hombres como en mujeres. Tiene lugar en el colon y recto y se desarrolla lentamente a partir de pólipos adenomatosos. El crecimiento excesivo de la mucosa del colon genera estos pólipos que tienen una morfología pedunculada o sésil. El desarrollo de cáncer colorrectal puede tener lugar por diferentes vías. Entre ellas se encuentra la aparición de lesiones serradas con apariencia del epitelio en dientes de sierra y que ocurre en el colon proximal. Esta vía se detecta en un tercio de todos los cánceres colorrectales. Con respecto a la secuencia adenoma-carcinoma, se ha propuesto que la progresión desde adenomas pequeños a grandes adenomas o adenocarcinomas avanzados está mediada por múltiples rutas moleculares que incluyen la inestabilidad de microsatélites, la inestabilidad cromosómica y rutas epigenéticas. Es posible hacer una prevención precoz puesto que se ha estimado que al menos lleva 10 años que un pólipo se transforme en célula tumoral (PMID: 28842051 0ines et al. Best Pract Res Clin Gastroenterol. 2017 Aug;31 (4) :419-424) . El diagnóstico precoz mediante colonoscopia y detección de sangre oculta en heces, así como la mejora en los tratamientos ha contribuido a prolongar la supervivencia de los tumores colorrectales en la fase de curación, Sin embargo, la metástasis está presente en aproximadamente el 25% de los pacientes durante el diagnóstico y en total, el 50% de los pacientes con cáncer colorrectal desarrollará metástasis (PMID: 27672422 Ohhara et al. World J Gastrointest Oncol. 2016 Sep 15;8 (9) :642-55) . Debido a la heterogeneidad y naturaleza multifactorial del cáncer colorrectal han aumentado considerablemente en los últimos años estudios para identificar predictores clínicos y moleculares, así como factores pronósticos con potencial para mejorar el manejo de los pacientes (PMID: 26964802 Aran et al. Clin Colorectal Cáncer. 2016 Sep;15 (3) :195-203; PMID: 29139091 Bermejo et al. Drugs. 2018 Jan;78 (1) :1-18) . Tanto la incidencia como la mortalidad del cáncer colorrectal ha disminuido tanto para hombres como para mujeres desde 1970 debido a la detección precoz (PMID: 29313949 Siegel et al. CA Cáncer J Clin. 2018 Jan;68 (1) :7-30) . Sin embargo, aunque diferentes terapias estás disponibles para el cáncer colorrectal metastásico, los resultados no son óptimos debido a la heterogeneidad entre pacientes debido a características moleculares, respuesta a la terapia y presentación clínica (PMID: 25593032 Linnekamp et al. Cáncer Res. 2015 Jan 15;75 (2) :245-9) . Los tratamientos más comunes de estos tumores se basan en la cirugía, la quimioterapia, terapias dirigidas y el tratamiento hormonal sustitutivo. Al menos el 50% de los pacientes con cáncer colorrectal recaen tras la resección quirúrgica y finalmente mueren de enfermedad metastásica. A pesar de la quimioterapia adyuvante postoperatoria en estos pacientes para disminuir el riesgo de recurrencia, el tratamiento adyuvante no da beneficios en supervivencia, especialmente en pacientes diagnosticados con estadío I. La terapia dirigida está basada en anticuerpos monoclonales y pequeños inhibidores moleculares, que selectivamente bloquean la proliferación celular mediante la intervención con ciertas moléculas y proteínas sobreexpresadas requeridas para la expansión del tumor. De acuerdo a la clasificación Mesh, el cáncer colorrectal se encuentra incluido en los cánceres gastrointestinales. La clasificación es la siguiente: Neoplasms [C04] Neoplasms by Site [C04.588] o Digestive System Neoplasms [C04.588.274] Gastrointestinal Neoplasms [C04.588.274.476] Esophageal Neoplasms [C04.588.274.476.205]_ Esophageal Squamous Cell Carcinoma [C04.588.274.476.205.500] Intestinal Neoplasms [C04.588.274.476.411] Cecal Neoplasms [C04.588.274.476.411.184], Appendiceal Neoplasms [C04.588.274.476.411.184.290] Colorectal Neoplasms [C04.588.274.476.411.307] Adenomatous Polyposis Coli [C04.588.274.476.411.307.089] Colonic Neoplasms [C04.588.274.476.411.307.180] Colitis-Associated Neoplasms [C04.588.274.476.411.307.180.400 ] Sigmoid Neoplasms [C04.588.274.476.411.307.180.800 ] Colorectal Neoplasms, Hereditar y Nonpolyposis [C04.588.274.476.411.307.190] Rectal Neoplasms [C04.588.274.476.411.307.790] Anus Neoplasms [C04.588.274.476.411.307.790.040 ] Anal Gland Neoplasms [C04.588.274.476.411.307. 790.040.040] Por tanto, es necesario desarrollar nuevos tratamientos para el cáncer colorrectal DESCRIPCIÓN DE LAS FIGURAS Fig. 1. Pose resultante del docking molecular entre Venetoclax y hepsina. Fig. 2. Cálculo del valor de IC50 de Venetoclax sobre la actividad de Hepsina. Velocidad máxima de la actividad de Hepsina en presencia de dosis crecientes de Venetoclax. Fig.3 . Efecto de Venetoclax en la migración de células de cáncer colorrectal. Porcentaje de migración celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 4. Efecto de Venetoclax en la degración de gelatina de células de cáncer colorrectal. Porcentaje de degradación celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 5. Efecto de Venetoclax en la generación de trombina. Valores del tiempo hasta el inicio del pico (Lagtime) y el tiempo en alcanzar el pico máximo (ttPeak) en las células Caco-2-HPN en presencia o ausencia de Venetoclax. Fig .6. Efecto de Venetoclax en el ciclo celular de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN en las diferentes fases del ciclo celular (G0/G1, S, G2/M) en presencia o ausencia de venetoclax. Fig. 7. Efecto de Venetoclax en la proliferación de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN que están proliferando (EdU+) en presencia o ausencia de Venetoclax. DESCRIPCIÓN DE LA INVENCIÓN La presente invención se refiere al Venetoclax y a cualquiera de sus sales, formas en estado sólido y solvatos para su uso en el tratamiento del cáncer cáncer colorrectal, y aún más preferiblemente del cáncer colorrectal metastásico. USO MÉDICO DEL COMPUESTO DE LA INVENCIÓN Por tanto, un primer aspecto de la invención se al Venetoclax, de ahora en adelante compuesto de la invención, o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer gastrointestinal. Venetoclax, es una molécula de nombre IUPAC 4- (4 - {[2- (4-clorofenil) -4, 4-dimetilciclohex-1-en-l- il] metil} piperazin-1 -il) -N - ({3 -nitro-4- [ (tetrahidro-2H-piran-4-ilmetil) amino] fenil} sulfonil) -2- (1H-pirrolo [2, 3-b] piridin-5-iloxi) benzamida, de fórmula (I) y número CAS 1257044-40-8 Fórmula (I) En esta memoria Venetoclax también incluye cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus ombinaciones, así como todas las formas en estado sólido de Venetoclax conocidas y composiciones farmacéuticas de las mismas. Venetoclax se describe en varios documentos de patentes, donde se indica que la sobreexpresión de proteínas Bcl-2 se correlaciona con la resistencia a la quimioterapia, el resultado clínico, la progresión de la enfermedad, el pronóstico general o una combinación de los mismos en varios cánceres y trastornos del sistema inmunológico. Por tanto, es necesario el desarrollo de compuestos que inhiban la actividad de las proteínas Bcl-2 antiapoptóticas, como el Venetoclax, aprobado para el tratamiento de la leucemia linfocítica crónica cuyos tumores tienen una alteración genética específica. Sin embargo, una disminución progresiva en su expresión durante la progresión del tumor indica un papel menor en la supervivencia y resistencia al CCR (Maurer CA et al., 1998. Dig Dis Sci 43 (12) :2641-2648; Flohil CC et al., 1996. J Pathol 178 (4) :393-397; Hawkins N et al., 1997. Tumour Biol 18 (3) :146-156; Kaklamanis L et al., 1996. J Pathol 179 (1) :1014; Kikuchi Y et al., 1997. Virchows Arch 431 (2) :111-117; Nakamura T et al., 1995. Pathol Int 45 (10) :721-728; Watson AJ et al., 1996. Br J Cáncer 73 (8) :889-895; van der Heijden M et al., 2016. Nat Commun 7:10916; Ofner D et al., 1995. Br J Cancer 72 (4) :981-985) , y un metaanálisis reciente (Huang Q et al., 2017. World J Gastroenterol.23 (27) :5018-5033, que es el tipo de estudio que aporta el mayor grado de evidencia, concluye que la alta expresión de la proteína antiapoptótica Bcl-2 es un factor de buen pronóstico en el cáncer colorrectal. Además, hasta el momento, de los 344 ensayos clínicos localizados en distintas bases de datos a fecha de enero de 2021, no hay ninguno en el que se emplee el Venetoclax para el tratamiento del cáncer gastrointestinal o colorrectal. Ningún experto en la materia se vería proclive a emplear Venetoclax en este tipo de cánceres. Las proteasas pericelulares han sido ampliamente implicadas en carcinogénesis, no solo porque actúan como enzimas capaces de degradar la matriz extracelulares, permitiendo así a las células tumorales romper la membrana basal e invadir el tejido circundante, sino que son capaces de actuar como modificadores proteolíticos de factores de crecimiento y receptores activados por proteasas que son críticos para la activación de rutas de señalización tumoral (PMID: 27870503 Tanabe et al. FEBS J. 2017 May;284 (10) :1421-1436) . Entre estas proteasas se encuentra hepsina, que pertenece a la super familia de serín proteasas transmembrana de tipo II (TTSP) . Hepsina se encuentra sobreexpresada en cáncer de próstata y sus niveles elevados son indicativos de mal pronóstico y recaida tras prostatectomía radical (PMID: 18927246 Sardana et al. Clin Chem. 2008 Dec;54 (12) :1951-60) . También se ha demostrado su obreexpresión en cáncer de ovario (PMID: 18726901 Miao et al. Int J Cáncer. 2008 Nov 1;123 (9) :2041-7) y cáncer de mama (PMID: 21383634) . Recientemente se ha descrito que la hepsina se encuentra elevada en suero de pacientes con cáncer colorrectal metastásico con respecto a pacientes con tumor primario. Aunque aún no existen datos que relacionen su expresión con metástasis en cáncer colorrectal. El desarrollo de eventos tromboembólicos venosos (ETEV) es un problema común en los tumores digestivos. La incidencia acumulada de ETEV en series modernas varía entre 12-20% (PMID: 26738412 Posch et al. Thromb Haemost. 2016 Apr;115 (4) :817-26) , dependiendo de las disparidades en las características de los pacientes en cada estudio y el contexto en el que la evaluación es llevada a cabo. La trombogénesis se atribuye a una combinación de factores clínicos y biológicos, que incluyen la activación del sistema hemostático por parte del tumor y la toxicidad vascular de la quimioterapia. La trombosis se asocia con una mayor morbilidad y mortalidad en estos pacientes (PMID: 28267709 Carmona-Bayonas et al. Br J Cáncer. 2017 Apr 11;116 (8) :994-1001, PMID: 22475313 Kline et al. Thromb Res. 2012 May;129 (5) :e194-9) y es uno de los eventos adversos más importantes en los ensayos clínicos de terapia anti-neoplásica. Tal como se muestra en los ejemplos de la invención, sorprendentemente, los inventores han demostrado mediante un ensayo fluorogénico la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina, así como la capacidad de Veneoclax de reducir la migración y la invasión de células de cáncer colorrectal. También han demostrado que reduce la generación de trombina en plasma procedente de sujetos sanos tras la incubación con células de cáncer colorrectal, y que reduce la generación de trombina en plasma de pacientes con cáncer colorrectal. Por tanto, otro aspecto de la invención se refiere al Venetoclax (compuesto de fórmula I) o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer colorrectal en un individuo. Más preferiblemente el cáncer colorrectal es el cáncer colorrectal metastásico. Aún más preferiblemente el individuo muestra los niveles de hepsina elevados con respecto a los valores normales. Los métodos para examinar los niveles de expresión de la proteína hepsina en muestras biológicas, y en particular en muestras de tejidos, son ampliamente conocidos en el stado de la técnica, por ejemplo, mediante métodos inmunohistoquímicos y/o el western blot. Los compuestos de la presente invención representados por la fórmula (I) pueden incluir isómeros, dependiendo de la presencia de enlaces múltiples, incluyendo isómeros ópticos o enantiómeros, dependiendo de la presencia de centros quirales. Los isómeros, enantiómeros o diastereoisómeros individuales y las mezclas de los mismos caen dentro del alcance de la presente invención, es decir, el término isómero también se refiere a cualquier mezcla de isómeros, como diastereómeros, racémicos, etc., incluso a sus isómeros ópticamente activos o las mezclas en distintas proporciones de los mismos. Los enantiómeros o diastereoisómeros individuales, así como sus mezclas, pueden separarse mediante técnicas convencionales. Asimismo, dentro del alcance de esta invención se encuentran los profármacos de los compuestos de fórmula (I) . El término "prodroga" o "profármaco" tal como aquí se utiliza incluye cualquier derivado de un compuesto de fórmula (I) -por ejemplo y no limitativamente: ésteres (incluyendo ésteres de ácidos carboxílicos, ésteres de aminoácidos, ésteres de fosfato, ésteres de sulfonato de sales metálicas, etc.) , carbamatos, amidas, etc.- que al ser administrado a un individuo puede ser transformado directa o indirectamente en dicho compuesto de fórmula (I) en el mencionado individuo. Ventajosamente, dicho derivado es un compuesto que aumenta la biodisponibilidad del compuesto de fórmula (I) cuando se administra a un individuo o que potencia la liberación del compuesto de fórmula (I) en un compartimento biológico. La naturaleza de dicho derivado no es crítica siempre y cuando pueda ser administrado a un individuo y proporcione el compuesto de fórmula (I) en un compartimento biológico de un individuo. La preparación de dicho profármaco puede llevarse a cabo mediante métodos convencionales conocidos por los expertos en la materia. Tal como aquí se utiliza, el término "derivado" incluye tanto a compuestos farmacéuticamente aceptables, es decir, derivados del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como derivados farmacéuticamente no aceptables, ya que éstos pueden ser útiles en la preparación de derivados farmacéuticamente aceptables. Los compuestos de la invención pueden estar en forma cristalina como compuestos libres o como solvatos. En este sentido, el término "solvato", tal como aquí se utiliza, incluye tanto solvatos farmacéuticamente aceptables, es decir, solvatos del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como olvatos farmacéuticamente no aceptables, los cuales pueden ser útiles en la preparación de solvatos o sales farmacéuticamente aceptables. La naturaleza del solvato farmacéuticamente aceptable no es crítica siempre y cuando sea farmacéuticamente aceptable. En una realización particular, el solvato es un hidrato. Los solvatos pueden obtenerse por métodos convencionales de solvatación conocidos por los expertos en la materia. Para su aplicación en terapia, los compuestos de fórmula (I) , sus sales, profármacos o solvatos, se encontrarán, preferentemente, en una forma farmacéuticamente aceptable o sustancialmente pura, es decir, que tiene un nivel de pureza farmacéuticamente aceptable excluyendo los aditivos farmacéuticos normales tales como diluyentes y portadores, y no incluyendo material considerado tóxico a niveles de dosificación normales. Los niveles de pureza para el principio activo son preferiblemente superiores al 50%, más preferiblemente superiores al 70%, y todavía más preferiblemente superiores al 90%. En una realización preferida, son superiores al 95% de compuesto de fórmula (I) , o de sus sales, solvatos o profármacos. COMPOSICIONES Y FORMAS FARMACÉUTICAS DE LA INVENCIÓN Otro aspecto de la invención se refiere a una composición, de ahora en adelante composición de la invención, que comprenden al menos el compuesto de la invención o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para su uso para la prevención, mejora alivio y/o tratamiento del cáncer gastrointestinal en un individuo. En una realización preferida de este aspecto de la invención es el cáncer colorrectal metastásico. Aún más preferiblemente el individuo presenta los niveles de hepsina elevados con respecto a los valores normales. En otra realización preferida de este aspecto, la composición de la invención es una composición farmacéutica. además, comprende un transportador o carrier farmacéuticamente aceptable, un excipiente y/o un vehículo farmacéuticamente aceptable. En otra realización preferida de este aspecto, la composición de la invención comprende, como único principio activo, el compuesto de fórmula (I) de la invención (Venetoclax) en una cantidad terapéuticamente efectiva, aunque puede comprender otros excipientes y/o vehículos farmacéuticamente aceptables. En el sentido utilizado en esta descripción, la expresión "cantidad terapéuticamente efectiva" se refiere a la cantidad del agente o compuesto capaz de desarrollar la acción terapéutica determinada por sus propiedades farmacológicas, calculada para producir el efecto deseado y, en general, vendrá determinada, entre otras causas, por las características propias de los compuestos, incluyendo la edad, estado del paciente, la severidad de la alteración o trastorno, y de la ruta y frecuencia de administración. Los compuestos descritos en la presente invención, sus sales, profármacos y/o solvatos así como las composiciones farmacéuticas que los contienen pueden ser utilizados junto con otros fármacos, o principios activos, adicionales para proporcionar una terapia de combinación. Dichos fármacos adicionales pueden formar parte de la misma composición farmacéutica o, alternativamente, pueden ser proporcionados en forma de una composición separada para su administración simultánea o no a la de la composición farmacéutica que comprende un compuesto de fórmula (I) , o una sal, profármaco o solvato del mismo. Por tanto, en otra realización preferida, la composición farmacéutica además comprende otro (u otros) principio activo. Más preferiblemente, el principio activo se selecciona de la lista que consiste en: agentes antiangiogénicos, terapias frente a EGFR, inhibidores de kinasa, agentes quimioterápicos, agentes inmunoterapéuticos, agentes frente a dianas moleculares, o cualquiera de sus combinaciones, para el tratamiento del cáncer colorrectal. En otra realización preferida los agentes antiangiogénicos se seleccionan de entre: Bevacizumab, Ziv-Aflibercept, Ramucirumab o cualquiera de sus combinaciones. En otra realización preferida las terapias frente a EGFR se seleccionan de entre: Cetuximab, Panitumumab o sus combinaciones. En otra realización preferida el inhibidor de kinasa es el Regofarenib. En otra realización preferida los agentes quimioterápicos se seleccionan de entre: Trifluridine +Tipiracil, Tegafur + Gimeracil + Oteracil, o sus combinaciones. En otra realización preferida los agentes inmunoterapéuticos se seleccionan de entre: Lefitolimod (MGN-1703) , Pembrolizumab, Atezolizumab o cualquiera de sus combinaciones. En otra realización preferida los agentes frente a dianas moleculares se seleccionan de entre: Encorafenib (LGX-818) + Binimetinib (MEK-162) , Napabucasin (BBI-608) , Vargatef (Nintedanib) , Masitinib (AB-1010) , Fruquintinib (HMPL-013) , Famitinib (SHR-1020) , Donafenib (CM-4307) , o cualquiera de sus combinaciones. Otro aspecto de la invención se refiere a una forma farmacéutica, de ahora en adelante forma farmacéutica de la invención, que comprende el compuesto de la invención o la composición de la invención. En esta memoria se entiende por "forma farmacéutica" la mezcla de uno o más principios activos con o sin aditivos que presentan características físicas para su adecuada dosificación, conservación, administración y biodisponibilidad. En otra realización preferida de la presente invención, las composiciones y formas farmacéuticas de la invención son adecuadas para la administración oral, en forma sólida o líquida. Las posibles formas para la administración oral son tabletas, cápsulas, siropes o soluciones y pueden contener excipientes convencionales conocidos en el ámbito farmacéutico, como agentes agregantes, rellenos, disgregantes o un surfactante farmacéuticamente aceptable. Otras formas farmacéuticas pueden ser los sistemas coloidales, dentro de los cuales se incluyen nanoemulsiones, nanocápsulas y nanopartículas poliméricas. Las composiciones para administración oral pueden ser preparadas por métodos los convencionales de Farmacia Galénica, como mezcla y dispersión. Las tabletas se pueden recubrir siguiendo métodos conocidos en la industria farmacéutica. Las composiciones y formas farmacéuticas se pueden adaptar para la administración parenteral, como soluciones estériles, suspensiones, o liofilizados de los productos de la invención, empleando la dosis adecuada. Se pueden emplear excipientes adecuados, como agentes tamponadores del pH o surfactantes. Las formulaciones anteriormente mencionadas pueden ser preparadas usando métodos convencionales, como los descritos en las Farmacopeas de diferentes países y en otros textos de referencia. El término "medicamento", tal y como se usa en esta memoria, hace referencia a cualquier sustancia usada para prevención, diagnóstico, alivio, tratamiento o curación de enfermedades en el hombre y los animales. La administración de los compuestos, composiciones o formas farmacéuticas de la presente invención puede ser realizada mediante cualquier método adecuado, como la infusión intravenosa y las vías oral, tópica o parenteral. La administración oral es la preferida por la conveniencia de los pacientes y por el carácter crónico de las enfermedades a tratar. La cantidad administrada de un compuesto de la presente invención dependerá de la relativa eficacia del compuesto elegido, la severidad de la enfermedad a tratar y el peso del paciente. Sin embargo, los compuestos de esta invención serán administrados una o más veces al día, por ejemplo 1, 2, 3 ó 4 veces diarias, con una dosis total entre 0.1 y 1000 mg/Kg/día. Es importante tener en cuenta que puede ser necesario introducir variaciones en la dosis, dependiendo de la edad y de la condición del paciente, así como modificaciones en la vía de administración. Los compuestos y composiciones de la presente invención pueden ser empleados junto con otros medicamentos en terapias combinadas. Los otros fármacos pueden formar parte de la misma composición o de otra composición diferente, para su administración al mismo tiempo o en tiempos diferentes. A lo largo de la descripción y las reivindicaciones la palabra "comprende" y sus variantes no pretenden excluir otras características técnicas, aditivos, componentes o pasos. Para los expertos en la materia, otros objetos, ventajas y características de la invención se desprenderán en parte de la descripción y en parte de la práctica de la invención. Los siguientes ejemplos y figuras se proporcionan a modo de ilustración, y no se pretende que sean limitativos de la presente invención. EJEMPLOS DE LA INVENCIÓN Cribado virtual Con el objetivo de encontrar nuevos inhibidores para la hepsina se realizó un cribado virtual mediante la técnica de docking molecular a partir de la estructura cristalográfica de la proteína depositada en la Protein Data Bank con código 1P57 frente a la librería de compuestos DrugBank (https://go.drugbank.com/) en las coordenadas de su sitio catalítico, caracterizada por residuos HIS57, ASP102 y SER195. El docking molecular se realizó en un clúster de cónputo de alto rendimiento mediante el software Autodock Vina 1.1.2 (http://vina.scripps.edu/) y para ello se convirtieron tanto la estructura de la proteína como la librería de ligandos DrugBank al formato pdbqt mediante MGLTools. Una vez terminados los cálculos se priorizaron los compuestos en función de docking score y se examinaron visualmente los 8 primeros, seleccionando el compuesto Venetoclax (código DrugBank DB11581) con un docking score de -11 Kcal/mol e nteraciones hidrofóbicas con los residuos PRO-60, LEU-41, GLN-73 y una interacción mediante puente de hidrogeno con el residuo ASN143 como se aprecia en la Figura 1. En dicha figura podemos observar que venetoclax impide el acceso a la triada catalítica, representada en formato de superficie para sus tres residuos. Venetoclax actúa como inhibidor irreversible de hepsina. Mediante un ensayo fluorogénico se determinó la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina. Hepsina es una serín proteasas capaz de hidrolizar al sustrato BOC-Gln-Arg-Arg-AMC (Bachem, Barcelona, Spain) , de manera que es posible registrar la emisión de fluorescencia mediante un lector de placas con longitudes de onda de excitación y emisión de 380 nm y 460 nm, respectivamente. Para ello, se incubó hepsina (0.05 ^M) (R&D Systems, Madrid, Spain) en tampón 50 mM Tris-HCl, pH 9 buffer, con 200 ^M BOC-Gln-Arg-Arg-AMC y registramos la fluorescencia emitida durante 5 minutos. Para comprobar el efecto de Venetoclax, se llevaó a cabo la misma reacción, pero incubando previamente hepsina con Venetoclax durante 1 hora a 37°C y en distintas concentraciones que oscilaron entre 0.167 y 2.5 ^M. De esta forma calculamos el valor de IC50, o concentración de inhibidor a la que se alcanza la mitad de la velocidad máxima de hepsina en la hidrólisis de su sustrato, que fue de 0.48 ^M. Venetoclax reduce la migración de células de cáncer colorrectal Una vez que las células alcanzan confluencia, forman una monocapa. Mediante la eliminación de una tira de células 300-500 ^m de anchura con una punta de pipetea de 200 ^l, es posible evaluar la capacidad de migración de las células y el efecto de Venetoclax en este proceso. La capacidad de migración se evalúa en función del porcentaje de área ocupada tras 48 horas de incubación y se cuantifica utilizando el software ImageJ. Los resultados muestran que Venetoclax a una concentración de 1, 88 ^M reduce de forma significativa la migración de células Caco-2, tanto con expresión basal como con sobreexpresión de hepsina, mediante transfección estable de un plásmido que contiene el gen HPN. Venetoclax reduce la invasión de células de cáncer colorrectal Para evaluar la invasión se realizó un ensayo en el que se evaluó la capacidad de las células para degradar una matriz de gelatina. Para ello, se mezcló gelatina al 0.2% y rodamina (Invitrogen, Life Technologies, Madrid, Spain) , en una ratio 1:55 en tampón NaCl 61 mM, borohidrato sódico 50 mM y después dializamos toda la noche en PBS. Se prepararon cubres con la mezcla preparada cubriéndolos y se fijó la matriz con glutaraldehido 0.5% durante 15 min. Los cubres se lavaron con PBS y se añadieron las suspensiones de células Caco-2 o KATO-III durante 72 horas. Posteriormente se fijaron las células con formaldehído 3.7% y se incubaron con phalloidin (0, 01 mg/ml) y ProLongGold Antifade con DAPI (4', 6-diamino-2-phenylindole; ThermoFisher) . Las imágenes se tomaron con un microscopio confocal SP8 LEICA y se analizaron con ImageJ y se procesaron con Adobe Photoshop. Nuestros resultados mostraron que Venetoclax, a una concentración de 1, 88 ^M, reduce de forma significativa la degradación de la gelatina de células Caco-2 tanto con expresión basal como con sobreexpresión de hepsina. Venetoclax reduce la generación de trombina Puesto que hepsina activa al FVII y, por tanto, la cascada de la coagulación, podría contribuir al estado de hipercoagulabilidad de los pacientes con cáncer colorrectal con niveles elevados de hepsina. Para comprobar esta hipótesis, se incubó plasma procedente de 20 sujetos sanos, a los que se extrajo sangre citratada 3.8% mediante venopunción, con las células Caco-2 con sobreexpresión de hepsina. El plasma se centrifugó previamente a 2500 g 20 minutos. Para el ensayo de generación de trombina, se retiró el plasma incubado y se incubó con el reactivo LOW® (factor tisular: 1 pmol; fosfolípidos: 4 ^mol; Diagnostica Stago) en una placa de 96 pocillo. Todas las muestras se prepararon en duplicado. La coagulación en estas muestras se inició añadiendo cloruro cálcico en un tampón que contenía el sustrato fluorogénico FluCa-kit reagent® (Diagnostica Stago) . Para cada muestra individual se utilizó un calibrador de trombina. La fluorescencia se registró durante 60 min en un fluorímetro Fluoroskan Ascent (Thermolab Systems) y los datos se analizaron utilizando el software Thrombinoscope™ (version 5.0.0.742; Diagnostica Stago) . Se analizaron los siguientes parámetros: (a) lagtime, que indica el inicio de la fase de generación de trombina; (b) tiempo hasta alcanzar la máxima concentración de trombina (ttPeak) ; (c) concentración máxima de trombina (Peak) ; (d) índice de frecuencia media (MRI) de la fase de propagación de la generación de trombina calculada por la fórmula Peak/ (ttPeak - lag-time) y se expresa en nM/min; y (e) potencial endógeno de trombina (ETP) que muestra la actividad enzimática de trombina evaluada como el área bajo la curva. Los resultados muestran que Venetoclax reduce el potencial endógeno de trombina (ETP) , el pico máximo (peak) y la velocidad en alcanzar el pico mientras que provoca n incremento en el tiempo de inicio de la fase de generación de trombina (lag-time) y el tiempo en alcanzar el pico. Tabla 1. Valores promedios del test de generación de trombina. Venetoclax no afecta ni a la muerte celular, ni al ciclo celular ni a la proliferación Puesto que Venetoclax es un fármaco dirigido frente a Bcl-2, quisimos evaluar si la menor migración o invasión celular podría deberse a una mayor muerte, a la alteración del ciclo celular o a una menor proliferación celular. Para ello se incubaron las células (5x105 cells/ml) en placas de 6 pocillos en presencia o ausencia de Venetocláx tras 48 h. El tipo de muerte celular se determinó mediante el ensayo de anexina V/7-ADD (Anexin V Apoptosis Detection Kit FITC; eBiosciences, Thermo Fisher, Karlsruhe, Alemania; 7-ADD BD-Biosciences) siguiendo las instrucciones del fabricante. El ciclo celular se analizó tras tratar las células con RNAse y con ioduro de propidio (Invitrogen) . Para evaluar la actividad proliferativa de las células Caco-2, se añadió 5-etinil-2'-desoxiuridina (EdU) (Thermo Fisher Scientific) durante 48 h. Luego, se usaron alícuotas de las células tumorales para determinar el porcentaje de células positivas, es decir, Caco-2 o Caco-2-HPN-EdU+, detectadas por reacción de acoplamiento de azida fluorescente con EdU de acuerdo con el protocolo del fabricante (Click-iT; Thermo Fisher Scientific) . Los resultados mostraron que Venetoclax no afecta ni a la muerte (porcentajes en torno al 5%) ni a la proliferación celular ni al ciclo celular.
+ ES-2919898_B2 Nuevo tratamiento del cáncer colorrectal CAMPO DE LA INVENCIÓN La presente invención pertenece al campo de la biomedicina, y más concretamente se refiere a un nuevo tratamiento para el cáncer gastrointestinal, y más preferiblemente para el tratamiento del cáncer gástrico y el cáncer colorrectal. ESTADO DE LA TÉCNICA ANTERIOR El cáncer colorrectal es el tercer cáncer más común diagnosticado tanto en hombres como en mujeres. Tiene lugar en el colon y recto y se desarrolla lentamente a partir de pólipos adenomatosos. El crecimiento excesivo de la mucosa del colon genera estos pólipos que tienen una morfología pedunculada o sésil. El desarrollo de cáncer colorrectal puede tener lugar por diferentes vías. Entre ellas se encuentra la aparición de lesiones serradas con apariencia del epitelio en dientes de sierra y que ocurre en el colon proximal. Esta vía se detecta en un tercio de todos los cánceres colorrectales. Con respecto a la secuencia adenoma-carcinoma, se ha propuesto que la progresión desde adenomas pequeños a grandes adenomas o adenocarcinomas avanzados está mediada por múltiples rutas moleculares que incluyen la inestabilidad de microsatélites, la inestabilidad cromosómica y rutas epigenéticas. Es posible hacer una prevención precoz puesto que se ha estimado que al menos lleva 10 años que un pólipo se transforme en célula tumoral (PMID: 28842051 0ines et al. Best Pract Res Clin Gastroenterol. 2017 Aug;31 (4) :419-424) . El diagnóstico precoz mediante colonoscopia y detección de sangre oculta en heces, así como la mejora en los tratamientos ha contribuido a prolongar la supervivencia de los tumores colorrectales en la fase de curación, Sin embargo, la metástasis está presente en aproximadamente el 25% de los pacientes durante el diagnóstico y en total, el 50% de los pacientes con cáncer colorrectal desarrollará metástasis (PMID: 27672422 Ohhara et al. World J Gastrointest Oncol. 2016 Sep 15;8 (9) :642-55) . Debido a la heterogeneidad y naturaleza multifactorial del cáncer colorrectal han aumentado considerablemente en los últimos años estudios para identificar predictores clínicos y moleculares, así como factores pronósticos con potencial para mejorar el manejo de los pacientes (PMID: 26964802 Aran et al. Clin Colorectal Cáncer. 2016 Sep;15 (3) :195-203; PMID: 29139091 Bermejo et al. Drugs. 2018 Jan;78 (1) :1-18) . Tanto la incidencia como la mortalidad del cáncer colorrectal ha disminuido tanto para hombres como para mujeres desde 1970 debido a la detección precoz (PMID: 29313949 Siegel et al. CA Cáncer J Clin. 2018 Jan;68 (1) :7-30) . Sin embargo, aunque diferentes terapias estás disponibles para el cáncer colorrectal metastásico, los resultados no son óptimos debido a la heterogeneidad entre pacientes debido a características moleculares, respuesta a la terapia y presentación clínica (PMID: 25593032 Linnekamp et al. Cáncer Res. 2015 Jan 15;75 (2) :245-9) . Los tratamientos más comunes de estos tumores se basan en la cirugía, la quimioterapia, terapias dirigidas y el tratamiento hormonal sustitutivo. Al menos el 50% de los pacientes con cáncer colorrectal recaen tras la resección quirúrgica y finalmente mueren de enfermedad metastásica. A pesar de la quimioterapia adyuvante postoperatoria en estos pacientes para disminuir el riesgo de recurrencia, el tratamiento adyuvante no da beneficios en supervivencia, especialmente en pacientes diagnosticados con estadío I. La terapia dirigida está basada en anticuerpos monoclonales y pequeños inhibidores moleculares, que selectivamente bloquean la proliferación celular mediante la intervención con ciertas moléculas y proteínas sobreexpresadas requeridas para la expansión del tumor. De acuerdo a la clasificación Mesh, el cáncer colorrectal se encuentra incluido en los cánceres gastrointestinales. La clasificación es la siguiente: Neoplasms [C04] Neoplasms by Site [C04.588] o Digestive System Neoplasms [C04.588.274] Gastrointestinal Neoplasms [C04.588.274.476] Esophageal Neoplasms [C04.588.274.476.205]_ Esophageal Squamous Cell Carcinoma [C04.588.274.476.205.500] Intestinal Neoplasms [C04.588.274.476.411] Cecal Neoplasms [C04.588.274.476.411.184] Appendiceal Neoplasms [C04.588.274.476.411.184.290] Colorectal Neoplasms [C04.588.274.476.411.307], Adenomatous Polyposis Coli [C04.588.274.476.411.307.089], Colonic Neoplasms [C04.588.274.476.411.307.180], Colitis-Associated Neoplasms [C04.588.274.476.411.307.180.400 ] Sigmoid Neoplasms [C04.588.274.476.411.307.180.800 ] Colorectal Neoplasms, Hereditar y Nonpolyposis [C04.588.274.476.411.307.190] Rectal Neoplasms [C04.588.274.476.411.307.790], Anus Neoplasms [C04.588.274.476.411.307.790.040 L Anal Gland Neoplasms [C04.588.274.476.411.307. 790.040.040] Por tanto, es necesario desarrollar nuevos tratamientos para el cáncer colorrectal DESCRIPCIÓN DE LAS FIGURAS Fig. 1. Pose resultante del docking molecular entre Venetoclax y hepsina. Fig. 2. Cálculo del valor de IC50 de Venetoclax sobre la actividad de Hepsina. Velocidad máxima de la actividad de Hepsina en presencia de dosis crecientes de Venetoclax. Fig.3 . Efecto de Venetoclax en la migración de células de cáncer colorrectal. Porcentaje de migración celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 4. Efecto de Venetoclax en la degración de gelatina de células de cáncer colorrectal. Porcentaje de degradación celular de las células Caco-2 y Caco-2-HPN en presencia o ausencia de Venetoclax. Fig. 5. Efecto de Venetoclax en la generación de trombina. Valores del tiempo hasta el inicio del pico (Lagtime) y el tiempo en alcanzar el pico máximo (ttPeak) en las células Caco-2-HPN en presencia o ausencia de Venetoclax. Fig .6. Efecto de Venetoclax en el ciclo celular de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN en las diferentes fases del ciclo celular (G0/G1, S, G2/M) en presencia o ausencia de venetoclax. Fig. 7. Efecto de Venetoclax en la proliferación de células de cáncer colorrectal. Porcentaje de células Caco-2 y Caco-2-HPN que están proliferando (EdU+) en presencia o ausencia de Venetoclax. DESCRIPCIÓN DE LA INVENCIÓN La presente invención se refiere al Venetoclax y a cualquiera de sus sales, formas en estado sólido y solvatos para su uso en el tratamiento del cáncer cáncer colorrectal, y aún más preferiblemente del cáncer colorrectal metastásico. USO MÉDICO DEL COMPUESTO DE LA INVENCIÓN Por tanto, un primer aspecto de la invención se al Venetoclax, de ahora en adelante compuesto de la invención, o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer gastrointestinal. Venetoclax, es una molécula de nombre IUPAC 4- (4 - {[2- (4-clorofenil) -4, 4-dimetilciclohex-1-en-l- il] metil} piperazin-1 -il) -N - ({3 -nitro-4- [ (tetrahidro-2H-piran-4-ilmetil) amino] fenil} sulfonil) -2- (1H-pirrolo [2, 3-b] piridin-5-iloxi) benzamida, de fórmula (I) y número CAS 1257044-40-8 Fórmula (I) En esta memoria Venetoclax también incluye cualquiera de sus sales, ésteres, tautómeros, solvatos e hidratos farmacéuticamente aceptables, o cualquiera de sus ombinaciones, así como todas las formas en estado sólido de Venetoclax conocidas y composiciones farmacéuticas de las mismas. Venetoclax se describe en varios documentos de patentes, donde se indica que la sobreexpresión de proteínas Bcl-2 se correlaciona con la resistencia a la quimioterapia, el resultado clínico, la progresión de la enfermedad, el pronóstico general o una combinación de los mismos en varios cánceres y trastornos del sistema inmunológico. Por tanto, es necesario el desarrollo de compuestos que inhiban la actividad de las proteínas Bcl-2 antiapoptóticas, como el Venetoclax, aprobado para el tratamiento de la leucemia linfocítica crónica cuyos tumores tienen una alteración genética específica. Sin embargo, una disminución progresiva en su expresión durante la progresión del tumor indica un papel menor en la supervivencia y resistencia al CCR (Maurer CA et al., 1998. Dig Dis Sci 43 (12) :2641-2648; Flohil CC et al., 1996. J Pathol 178 (4) :393-397; Hawkins N et al., 1997. Tumour Biol 18 (3) :146-156; Kaklamanis L et al., 1996. J Pathol 179 (1) :1014; Kikuchi Y et al., 1997. Virchows Arch 431 (2) :111117; Nakamura T et al., 1995. Pathol Int 45 (10) :721-728; Watson AJ et al., 1996. Br J Cáncer 73 (8) :889-895; van der Heijden M et al., 2016. Nat Commun 7:10916; Ofner D et al., 1995. Br J Cancer 72 (4) :981-985) , y un metaanálisis reciente (Huang Q et al., 2017. World J Gastroenterol.23 (27) :5018-5033, que es el tipo de estudio que aporta el mayor grado de evidencia, concluye que la alta expresión de la proteína antiapoptótica Bcl-2 es un factor de buen pronóstico en el cáncer colorrectal. Además, hasta el momento, de los 344 ensayos clínicos localizados en distintas bases de datos a fecha de enero de 2021, no hay ninguno en el que se emplee el Venetoclax para el tratamiento del cáncer gastrointestinal o colorrectal. Ningún experto en la materia se vería proclive a emplear Venetoclax en este tipo de cánceres. Las proteasas pericelulares han sido ampliamente implicadas en carcinogénesis, no solo porque actúan como enzimas capaces de degradar la matriz extracelulares, permitiendo así a las células tumorales romper la membrana basal e invadir el tejido circundante, sino que son capaces de actuar como modificadores proteolíticos de factores de crecimiento y receptores activados por proteasas que son críticos para la activación de rutas de señalización tumoral (PMID: 27870503 Tanabe et al. FEBS J. 2017 May;284 (10) :1421-1436) . Entre estas proteasas se encuentra hepsina, que pertenece a la super familia de serín proteasas transmembrana de tipo II (TTSP) . Hepsina se encuentra sobreexpresada en cáncer de próstata y sus niveles elevados son indicativos de mal pronóstico y recaida tras prostatectomía radical (PMID: 18927246 Sardana et al. Clin Chem. 2008 Dec;54 (12) :1951-60) . También se ha demostrado su obreexpresión en cáncer de ovario (PMID: 18726901 Miao et al. int J Cáncer, 2008 Nov 1;123 (9) :2041-7) y cáncer de mama (PMID: 21383634) . Recientemente se ha descrito que la hepsina se encuentra elevada en suero de pacientes con cáncer colorrectal metastásico con respecto a pacientes con tumor primario. Aunque aún no existen datos que relacionen su expresión con metástasis en cáncer colorrectal. El desarrollo de eventos tromboembólicos venosos (ETEV) es un problema común en los tumores digestivos. La incidencia acumulada de ETEV en series modernas varía entre 12-20% (PMID: 26738412 Posch et al. Thromb Haemost. 2016 Apr;115 (4) :817-26) , dependiendo de las disparidades en las características de los pacientes en cada estudio y el contexto en el que la evaluación es llevada a cabo. La trombogénesis se atribuye a una combinación de factores clínicos y biológicos, que incluyen la activación del sistema hemostático por parte del tumor y la toxicidad vascular de la quimioterapia. La trombosis se asocia con una mayor morbilidad y mortalidad en estos pacientes (PMID: 28267709 Carmona-Bayonas et al. Br J Cáncer. 2017 Apr 11;116 (8) :994-1001, PMID: 22475313 Kline et al. Thromb Res. 2012 May;129 (5) :e194-9) y es uno de los eventos adversos más importantes en los ensayos clínicos de terapia anti-neoplásica. Tal como se muestra en los ejemplos de la invención, sorprendentemente, los inventores han demostrado mediante un ensayo fluorogénico la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina, así como la capacidad de Veneoclax de reducir la migración y la invasión de células de cáncer colorrectal. También han demostrado que reduce la generación de trombina en plasma procedente de sujetos sanos tras la incubación con células de cáncer colorrectal, y que reduce la generación de trombina en plasma de pacientes con cáncer colorrectal. Por tanto, otro aspecto de la invención se refiere al Venetoclax (compuesto de fórmula I) o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para la prevención, mejora, alivio y/o tratamiento del cáncer colorrectal en un individuo, donde dicho individuo muestra los niveles de hepsina elevados con respecto a los valores normales. Más preferiblemente el cáncer colorrectal es el cáncer colorrectal metastásico. Los métodos para examinar los niveles de expresión de la proteína hepsina en muestras biológicas, y en particular en muestras de tejidos, son ampliamente conocidos en el stado de la técnica, por ejemplo, mediante métodos inmunohistoquímicos y/o el western blot. Los compuestos de la presente invención representados por la fórmula (I) pueden incluir isómeros, dependiendo de la presencia de enlaces múltiples, incluyendo isómeros ópticos o enantiómeros, dependiendo de la presencia de centros quirales. Los isómeros, enantiómeros o diastereoisómeros individuales y las mezclas de los mismos caen dentro del alcance de la presente invención, es decir, el término isómero también se refiere a cualquier mezcla de isómeros, como diastereómeros, racémicos, etc., incluso a sus isómeros ópticamente activos o las mezclas en distintas proporciones de los mismos. Los enantiómeros o diastereoisómeros individuales, así como sus mezclas, pueden separarse mediante técnicas convencionales. Asimismo, dentro del alcance de esta invención se encuentran los profármacos de los compuestos de fórmula (I) . El término "prodroga" o "profármaco" tal como aquí se utiliza incluye cualquier derivado de un compuesto de fórmula (I) -por ejemplo y no limitativamente: ésteres (incluyendo ésteres de ácidos carboxílicos, ésteres de aminoácidos, ésteres de fosfato, ésteres de sulfonato de sales metálicas, etc.) , carbamatos, amidas, etc.- que al ser administrado a un individuo puede ser transformado directa o indirectamente en dicho compuesto de fórmula (I) en el mencionado individuo. Ventajosamente, dicho derivado es un compuesto que aumenta la biodisponibilidad del compuesto de fórmula (I) cuando se administra a un individuo o que potencia la liberación del compuesto de fórmula (I) en un compartimento biológico. La naturaleza de dicho derivado no es crítica siempre y cuando pueda ser administrado a un individuo y proporcione el compuesto de fórmula (I) en un compartimento biológico de un individuo. La preparación de dicho profármaco puede llevarse a cabo mediante métodos convencionales conocidos por los expertos en la materia. Tal como aquí se utiliza, el término "derivado" incluye tanto a compuestos farmacéuticamente aceptables, es decir, derivados del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como derivados farmacéuticamente no aceptables, ya que éstos pueden ser útiles en la preparación de derivados farmacéuticamente aceptables. Los compuestos de la invención pueden estar en forma cristalina como compuestos libres o como solvatos. En este sentido, el término "solvato", tal como aquí se utiliza, incluye tanto solvatos farmacéuticamente aceptables, es decir, solvatos del compuesto de fórmula (I) que pueden ser utilizados en la elaboración de un medicamento, como olvatos farmacéuticamente no aceptables, los cuales pueden ser útiles en la preparación de solvatos o sales farmacéuticamente aceptables. La naturaleza del solvato farmacéuticamente aceptable no es crítica siempre y cuando sea farmacéuticamente aceptable. En una realización particular, el solvato es un hidrato. Los solvatos pueden obtenerse por métodos convencionales de solvatación conocidos por los expertos en la materia. Para su aplicación en terapia, los compuestos de fórmula (I) , sus sales, profármacos o solvatos, se encontrarán, preferentemente, en una forma farmacéuticamente aceptable o sustancialmente pura, es decir, que tiene un nivel de pureza farmacéuticamente aceptable excluyendo los aditivos farmacéuticos normales tales como diluyentes y portadores, y no incluyendo material considerado tóxico a niveles de dosificación normales. Los niveles de pureza para el principio activo son preferiblemente superiores al 50%, más preferiblemente superiores al 70%, y todavía más preferiblemente superiores al 90%. En una realización preferida, son superiores al 95% de compuesto de fórmula (I) , o de sus sales, solvatos o profármacos. COMPOSICIONES Y FORMAS FARMACÉUTICAS DE LA INVENCIÓN Otro aspecto de la invención se refiere a una composición, de ahora en adelante composición de la invención, que comprenden al menos el compuesto de la invención o cualquiera de sus sales, preferiblemente cualquier sal farmacéuticamente aceptable, ésteres, tautómeros, polimorfos, hidratos farmacéuticamente aceptables, o un isómero, profármacos, derivados, solvatos o análogos, o cualquiera de sus combinaciones, para su uso para la prevención, mejora alivio y/o tratamiento del cáncer gastrointestinal en un individuo. En una realización preferida de este aspecto de la invención es el cáncer colorrectal metastásico. Aún más preferiblemente el individuo presenta los niveles de hepsina elevados con respecto a los valores normales. En otra realización preferida de este aspecto, la composición de la invención es una composición farmacéutica. además, comprende un transportador o carrier farmacéuticamente aceptable, un excipiente y/o un vehículo farmacéuticamente aceptable. En otra realización preferida de este aspecto, la composición de la invención comprende, como único principio activo, el compuesto de fórmula (I) de la invención (Venetoclax) en una cantidad terapéuticamente efectiva, aunque puede comprender otros excipientes y/o vehículos farmacéuticamente aceptables. En el sentido utilizado en esta descripción, la expresión "cantidad terapéuticamente efectiva" se refiere a la cantidad del agente o compuesto capaz de desarrollar la acción terapéutica determinada por sus propiedades farmacológicas, calculada para producir el efecto deseado y, en general, vendrá determinada, entre otras causas, por las características propias de los compuestos, incluyendo la edad, estado del paciente, la severidad de la alteración o trastorno, y de la ruta y frecuencia de administración. Los compuestos descritos en la presente invención, sus sales, profármacos y/o solvatos así como las composiciones farmacéuticas que los contienen pueden ser utilizados junto con otros fármacos, o principios activos, adicionales para proporcionar una terapia de combinación. Dichos fármacos adicionales pueden formar parte de la misma composición farmacéutica o, alternativamente, pueden ser proporcionados en forma de una composición separada para su administración simultánea o no a la de la composición farmacéutica que comprende un compuesto de fórmula (I) , o una sal, profármaco o solvato del mismo. Por tanto, en otra realización preferida, la composición farmacéutica además comprende otro (u otros) principio activo. Más preferiblemente, el principio activo se selecciona de la lista que consiste en: agentes antiangiogénicos, terapias frente a EGFR, inhibidores de kinasa, agentes quimioterápicos, agentes inmunoterapéuticos, agentes frente a dianas moleculares, o cualquiera de sus combinaciones, para el tratamiento del cáncer colorrectal. En otra realización preferida los agentes antiangiogénicos se seleccionan de entre: Bevacizumab, Ziv-Aflibercept, Ramucirumab o cualquiera de sus combinaciones. En otra realización preferida las terapias frente a EGFR se seleccionan de entre: Cetuximab, Panitumumab o sus combinaciones. En otra realización preferida el inhibidor de kinasa es el Regofarenib. En otra realización preferida los agentes quimioterápicos se seleccionan de entre: Trifluridine +Tipiracil, Tegafur + Gimeracil + Oteracil, o sus combinaciones. En otra realización preferida los agentes inmunoterapéuticos se seleccionan de entre: Lefitolimod (MGN-1703) , Pembrolizumab, Atezolizumab o cualquiera de sus combinaciones. En otra realización preferida los agentes frente a dianas moleculares se seleccionan de entre: Encorafenib (LGX-818) + Binimetinib (MEK-162) , Napabucasin (BBI-608) , Vargatef (Nintedanib) , Masitinib (AB-1010) , Fruquintinib (HMPL-013) , Famitinib (SHR-1020) , Donafenib (CM-4307) , o cualquiera de sus combinaciones. Otro aspecto de la invención se refiere a una forma farmacéutica, de ahora en adelante forma farmacéutica de la invención, que comprende el compuesto de la invención o la composición de la invención. En esta memoria se entiende por "forma farmacéutica" la mezcla de uno o más principios activos con o sin aditivos que presentan características físicas para su adecuada dosificación, conservación, administración y biodisponibilidad. En otra realización preferida de la presente invención, las composiciones y formas farmacéuticas de la invención son adecuadas para la administración oral, en forma sólida o líquida. Las posibles formas para la administración oral son tabletas, cápsulas, siropes o soluciones y pueden contener excipientes convencionales conocidos en el ámbito farmacéutico, como agentes agregantes, rellenos, disgregantes o un surfactante farmacéuticamente aceptable. Otras formas farmacéuticas pueden ser los sistemas coloidales, dentro de los cuales se incluyen nanoemulsiones, nanocápsulas y nanopartículas poliméricas. Las composiciones para administración oral pueden ser preparadas por métodos los convencionales de Farmacia Galénica, como mezcla y dispersión. Las tabletas se pueden recubrir siguiendo métodos conocidos en la industria farmacéutica. Las composiciones y formas farmacéuticas se pueden adaptar para la administración parenteral, como soluciones estériles, suspensiones, o liofilizados de los productos de la invención, empleando la dosis adecuada. Se pueden emplear excipientes adecuados, como agentes tamponadores del pH o surfactantes. Las formulaciones anteriormente mencionadas pueden ser preparadas usando métodos convencionales, como los descritos en las Farmacopeas de diferentes países y en otros textos de referencia. El término "medicamento", tal y como se usa en esta memoria, hace referencia a cualquier sustancia usada para prevención, diagnóstico, alivio, tratamiento o curación de enfermedades en el hombre y los animales. La administración de los compuestos, composiciones o formas farmacéuticas de la presente invención puede ser realizada mediante cualquier método adecuado, como la infusión intravenosa y las vías oral, tópica o parenteral. La administración oral es la preferida por la conveniencia de los pacientes y por el carácter crónico de las enfermedades a tratar. La cantidad administrada de un compuesto de la presente invención dependerá de la relativa eficacia del compuesto elegido, la severidad de la enfermedad a tratar y el peso del paciente. Sin embargo, los compuestos de esta invención serán administrados una o más veces al día, por ejemplo 1, 2, 3 ó 4 veces diarias, con una dosis total entre 0.1 y 1000 mg/Kg/día. Es importante tener en cuenta que puede ser necesario introducir variaciones en la dosis, dependiendo de la edad y de la condición del paciente, así como modificaciones en la vía de administración. Los compuestos y composiciones de la presente invención pueden ser empleados junto con otros medicamentos en terapias combinadas. Los otros fármacos pueden formar parte de la misma composición o de otra composición diferente, para su administración al mismo tiempo o en tiempos diferentes. A lo largo de la descripción y las reivindicaciones la palabra "comprende" y sus variantes no pretenden excluir otras características técnicas, aditivos, componentes o pasos. Para los expertos en la materia, otros objetos, ventajas y características de la invención se desprenderán en parte de la descripción y en parte de la práctica de la invención. Los siguientes ejemplos y figuras se proporcionan a modo de ilustración, y no se pretende que sean limitativos de la presente invención. EJEMPLOS DE LA INVENCIÓN Cribado virtual Con el objetivo de encontrar nuevos inhibidores para la hepsina se realizó un cribado virtual mediante la técnica de docking molecular a partir de la estructura cristalográfica de la proteína depositada en la Protein Data Bank con código 1P57 frente a la librería de compuestos DrugBank (https://go.drugbank.com/) en las coordenadas de su sitio catalítico, caracterizada por residuos HIS57, ASP102 y SER195. El docking molecular se realizó en un clúster de cónputo de alto rendimiento mediante el software Autodock Vina 1.1.2 (http://vina.scripps.edu/) y para ello se convirtieron tanto la estructura de la proteína como la librería de ligandos DrugBank al formato pdbqt mediante MGLTools. Una vez terminados los cálculos se priorizaron los compuestos en función de docking score y se examinaron visualmente los 8 primeros, seleccionando el compuesto Venetoclax (código DrugBank DB11581) con un docking score de -11 Kcal/mol e nteraciones hidrofóbicas con los residuos PRO-60, LEU-41, GLN-73 y una interacción mediante puente de hidrogeno con el residuo ASN143 como se aprecia en la Figura 1. En dicha figura podemos observar que venetoclax impide el acceso a la triada catalítica, representada en formato de superficie para sus tres residuos. Venetoclax actúa como inhibidor irreversible de hepsina. Mediante un ensayo fluorogénico se determinó la capacidad de Veneoclax de inhibir la actividad proteolítica de hepsina. Hepsina es una serín proteasas capaz de hidrolizar al sustrato BOC-Gln-Arg-Arg-AMC (Bachem, Barcelona, Spain) , de manera que es posible registrar la emisión de fluorescencia mediante un lector de placas con longitudes de onda de excitación y emisión de 380 nm y 460 nm, respectivamente. Para ello, se incubó hepsina (0.05 M) (R&D Systems, Madrid, Spain) en tampón 50 mM Tris-HCl, pH 9 buffer, con 200 M BOC-Gln-Arg-Arg-AMC y registramos la fluorescencia emitida durante 5 minutos. Para comprobar el efecto de Venetoclax, se llevaó a cabo la misma reacción, pero incubando previamente hepsina con Venetoclax durante 1 hora a 37°C y en distintas concentraciones que oscilaron entre 0.167 y 2.5 M. De esta forma calculamos el valor de IC5O, o concentración de inhibidor a la que se alcanza la mitad de la velocidad máxima de hepsina en la hidrólisis de su sustrato, que fue de 0.48 M. Venetoclax reduce la migración de células de cáncer colorrectal Una vez que las células alcanzan confluencia, forman una monocapa. Mediante la eliminación de una tira de células 300-500 m de anchura con una punta de pipetea de 200 l, es posible evaluar la capacidad de migración de las células y el efecto de Venetoclax en este proceso. La capacidad de migración se evalúa en función del porcentaje de área ocupada tras 48 horas de incubación y se cuantifica utilizando el software ImageJ. Los resultados muestran que Venetoclax a una concentración de 1, 88 M reduce de forma significativa la migración de células Caco-2, tanto con expresión basal como con sobreexpresión de hepsina, mediante transfección estable de un plásmido que contiene el gen HPN. Venetoclax reduce la invasión de células de cáncer colorrectal Para evaluar la invasión se realizó un ensayo en el que se evaluó la capacidad de las células para degradar una matriz de gelatina. Para ello, se mezcló gelatina al 0.2% y rodamina (Invitrogen, Life Technologies, Madrid, Spain) , en una ratio 1:55 en tampón NaCl 61 mM, borohidrato sódico 50 mM y después dializamos toda la noche en PBS. Se prepararon cubres con la mezcla preparada cubriéndolos y se fijó la matriz con glutaraldehido 0.5% durante 15 min. Los cubres se lavaron con PBS y se añadieron las suspensiones de células Caco-2 o KATO-III durante 72 horas. Posteriormente se fijaron las células con formaldehído 3.7% y se incubaron con phalloidin (0, 01 mg/ml) y ProLongGold Antifade con DAPI (4', 6-diamino-2-phenylindole; ThermoFisher) . Las imágenes se tomaron con un microscopio confocal SP8 LEICA y se analizaron con ImageJ y se procesaron con Adobe Photoshop. Nuestros resultados mostraron que Venetoclax, a una concentración de 1, 88 M, reduce de forma significativa la degradación de la gelatina de células Caco-2 tanto con expresión basal como con sobreexpresión de hepsina. Venetoclax reduce la generación de trombina Puesto que hepsina activa al FVII y, por tanto, la cascada de la coagulación, podría contribuir al estado de hipercoagulabilidad de los pacientes con cáncer colorrectal con niveles elevados de hepsina. Para comprobar esta hipótesis, se incubó plasma procedente de 20 sujetos sanos, a los que se extrajo sangre citratada 3.8% mediante venopunción, con las células Caco-2 con sobreexpresión de hepsina. El plasma se centrifugó previamente a 2500 g 20 minutos. Para el ensayo de generación de trombina, se retiró el plasma incubado y se incubó con el reactivo LOW® (factor tisular: 1 pmol; fosfolípidos: 4 mol; Diagnostica Stago) en una placa de 96 pocillo. Todas las muestras se prepararon en duplicado. La coagulación en estas muestras se inició añadiendo cloruro cálcico en un tampón que contenía el sustrato fluorogénico FluCa-kit reagent® (Diagnostica Stago) . Para cada muestra individual se utilizó un calibrador de trombina. La fluorescencia se registró durante 60 min en un fluorímetro Fluoroskan Ascent (Thermolab Systems) y los datos se analizaron utilizando el software Thrombinoscope™ (version 5.0.0.742; Diagnostica Stago) . Se analizaron los siguientes parámetros: (a) lagtime, que indica el inicio de la fase de generación de trombina; (b) tiempo hasta alcanzar la máxima concentración de trombina (ttPeak) ; (c) concentración máxima de trombina (Peak) ; (d) índice de frecuencia media (MRI) de la fase de propagación de la generación de trombina calculada por la fórmula Peak/ (ttPeak - lag-time) y se expresa en nM/min; y (e) potencial endógeno de trombina (ETP) que muestra la actividad enzimática de trombina evaluada como el área bajo la curva. Los resultados muestran que Venetoclax reduce el potencial endógeno de trombina (ETP) , el pico máximo (peak) y la velocidad en alcanzar el pico mientras que provoca n incremento en el tiempo de inicio de la fase de generación de trombina (lag-time) y el tiempo en alcanzar el pico. Tabla 1. Valores promedios del test de generación de trombina. Venetoclax no afecta ni a la muerte celular, ni al ciclo celular ni a la proliferación Puesto que Venetoclax es un fármaco dirigido frente a Bcl-2, quisimos evaluar si la menor migración o invasión celular podría deberse a una mayor muerte, a la alteración del ciclo celular o a una menor proliferación celular. Para ello se incubaron las células (5x105 cells/ml) en placas de 6 pocillos en presencia o ausencia de Venetocláx tras 48 h. El tipo de muerte celular se determinó mediante el ensayo de anexina V/7-ADD (Anexin V Apoptosis Detection Kit FITC; eBiosciences, Thermo Fisher, Karlsruhe, Alemania; 7-ADD BD-Biosciences) siguiendo las instrucciones del fabricante. El ciclo celular se analizó tras tratar las células con RNAse y con ioduro de propidio (Invitrogen) . Para evaluar la actividad proliferativa de las células Caco-2, se añadió 5-etinil-2'-desoxiuridina (EdU) (Thermo Fisher Scientific) durante 48 h. Luego, se usaron alícuotas de las células tumorales para determinar el porcentaje de células positivas, es decir, Caco-2 o Caco-2-HPN-EdU+, detectadas por reacción de acoplamiento de azida fluorescente con EdU de acuerdo con el protocolo del fabricante (Click-iT; Thermo Fisher Scientific) . Los resultados mostraron que Venetoclax no afecta ni a la muerte (porcentajes en torno al 5%) ni a la proliferación celular ni al ciclo celular.
Publicaciones:
ES2919898 (28/07/2022) - A1 Solicitud de patente con informe sobre el estado de la técnica
ES2919898 (13/10/2023) - B2 Patente de invención con examen
ES2919898 (02/02/2024) - B8 Corrección de la primera página de patente de invención
Eventos:
En fecha 27/01/2021 se realizó Registro Instancia de Solicitud
En fecha 27/01/2021 se realizó Admisión a Trámite
En fecha 27/01/2021 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 28/01/2021 se realizó 3406X_Solicitud Correcciones
En fecha 01/02/2021 se realizó 1551X_Notificación Correcciones Admitidas
En fecha 12/02/2021 se realizó Superado examen de oficio
En fecha 26/07/2021 se realizó 3406X_Solicitud Correcciones
En fecha 17/12/2021 se realizó Realizado IET
En fecha 22/12/2021 se realizó 1109P_Comunicación Traslado del IET
En fecha 11/03/2022 se realizó 1550X_Notificación Rechazo Correcciones
En fecha 17/03/2022 se realizó Publicación Rechazo Correcciones
En fecha 23/03/2022 se realizó Registro Documentación no Identificada
En fecha 28/07/2022 se realizó Publicación Solicitud
En fecha 28/07/2022 se realizó Publicación Folleto Solicitud con IET (A1)
En fecha 27/10/2022 se realizó PETEX_Petición de examen sustantivo
En fecha 14/11/2022 se realizó Validación petición y/o pago de examen sustantivo conforme
En fecha 23/03/2023 se realizó El solicitante ha contestado pero existen nuevas objeciones a la concesión de la solicitud
En fecha 23/03/2023 se realizó Elaboración de examen sustantivo
En fecha 23/03/2023 se realizó 6120P_Notificación de examen sustantivo
En fecha 29/03/2023 se realizó Publicación de examen sustantivo
En fecha 29/05/2023 se realizó 3585X_Registro Solicitud Prórroga de Plazos
En fecha 29/05/2023 se realizó Concesión Prórroga de Plazos
En fecha 29/05/2023 se realizó 1585X_Notificación Concesión Prórroga de Plazos
En fecha 02/06/2023 se realizó Publicación Concesión Prórroga de Plazos (BOPI)
En fecha 12/06/2023 se realizó 5127P_Subsanación a defectos en examen sustantivo
En fecha 20/09/2023 se realizó Designación de Comisión de Expertos
En fecha 25/09/2023 se realizó Finalización de Examen Sustantivo
En fecha 25/09/2023 se realizó 6121P_Comunicación finalización de examen sustantivo
En fecha 29/09/2023 se realizó Publicación finalización de examen sustantivo
En fecha 05/10/2023 se realizó Concesión con examen sustantivo
En fecha 05/10/2023 se realizó Entrega título
En fecha 05/10/2023 se realizó 6125P_Notificación de concesión con examen sustantivo
En fecha 13/10/2023 se realizó Publicación concesión Patente
En fecha 13/10/2023 se realizó Publicación Folleto Concesión
En fecha 02/02/2024 se realizó Publicación de la Corrección de la primera pagina de la patente de invención (BOPI)
En fecha 02/02/2024 se realizó Publicación Folleto Corrección de la Primera Página de la Patente de Invención (B8)
Pagos:
27/01/2021 - Pago Tasas IET
16/10/2023 - Pago 03 Anualidad
28/02/2024 - Pago 04 Anualidad
Fuente de la información
Parte de la información aquí publicada es pública puesto que ha sido obtenida de la Oficina de Propiedad Industrial de los diferentes países el 27/04/2024 y por lo tanto puede ser que la información no esté actualizada.Parte de la información aquí mostrada ha sido calculada por nuestro sistema informático y puede no ser veraz.
Privacidad
Si considera que al información aquí publicada afecta a su privacidad y desea que eliminemos la información aquí publicada envíe un email a info@patentes-y-marcas.com o rellene el formulario que encontrará aquí.Información sobre el registro de patente nacional por Nuevo tratamiento del cáncer colorrectal con el número P202130064
El registro de patente nacional por Nuevo tratamiento del cáncer colorrectal con el número P202130064 fue solicitada el 27/01/2021. Se trata de un registro en España por lo que este registro no ofrece protección en el resto de países. El registro Nuevo tratamiento del cáncer colorrectal con el número P202130064 fue solicitada por FUNDACION UNIVERSITARIA SAN ANTONIO mediante los servicios del agente MARIA DESAMPARADOS DIAZ PACHECO. El registro [modality] por Nuevo tratamiento del cáncer colorrectal con el número P202130064 está clasificado como A61K 31/496,A61P 35/00 según la clasificación internacional de patentes.
Otras invenciones solicitadas por FUNDACION UNIVERSITARIA SAN ANTONIO
Es posible conocer todas las invenciones solicitadas por FUNDACION UNIVERSITARIA SAN ANTONIO entre las que se encuentra el registro de patente nacional por Nuevo tratamiento del cáncer colorrectal con el número P202130064. Si se desean conocer más invenciones solicitadas por FUNDACION UNIVERSITARIA SAN ANTONIO clicar aquí.Otras invenciones solicitadas en la clasificación internacional de patentes A61K 31/496,A61P 35/00.
Es posible conocer invenciones similares al campo de la técnica se refiere. El registro de patente nacional por Nuevo tratamiento del cáncer colorrectal con el número P202130064 está clasificado con la clasificación A61K 31/496,A61P 35/00 por lo que si se desea conocer más registros con la clasificación A61K 31/496,A61P 35/00 clicar aquí.Otras invenciones solicitadas a través del representante MARIA DESAMPARADOS DIAZ PACHECO
Es posible conocer todas las invenciones solicitadas a través del agente MARIA DESAMPARADOS DIAZ PACHECO entre las que se encuentra el registro patente nacional por Nuevo tratamiento del cáncer colorrectal con el número P202130064. Si se desean conocer más invenciones solicitadas a través del agente MARIA DESAMPARADOS DIAZ PACHECO clicar aquí.Patentes en España
Es posible conocer todas las invenciones publicadas en España entre las que se encuentra el registro patente nacional por Nuevo tratamiento del cáncer colorrectal. Nuestro portal www.patentes-y-marcas.com ofrece acceso a las publicaciones de patentes en España. Conocer las patentes registradas en un país es importante para saber las posibilidades de fabricar, vender o explotar una invención en España.Patentes registradas en la clase A
Es posible conocer todas las patentes registradas en la clase A (NECESIDADES CORRIENTES DE LA VIDA) entre las que se encuentra la patente Nuevo tratamiento del cáncer colorrectal con el número P202130064. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61
Es posible conocer todas las patentes registradas en la clase A61 (CIENCIAS MEDICAS O VETERINARIAS; HIGIENE) entre las que se encuentra la patente Nuevo tratamiento del cáncer colorrectal con el número P202130064. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61K
Es posible conocer todas las patentes registradas en la clase A61K (PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO ) entre las que se encuentra la patente Nuevo tratamiento del cáncer colorrectal con el número P202130064. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61P
Es posible conocer todas las patentes registradas en la clase A61P (ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES) entre las que se encuentra la patente Nuevo tratamiento del cáncer colorrectal con el número P202130064. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.
¿Tienes alguna duda?
Escribe tu consulta y te responderemos rápida y gratuitamente.


 P202130055
P202130055