- Home /
- Publicaciones de patentes /
- DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL
Patente nacional por "DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL"
Este registro ha sido solicitado por
Persona física
Contacto
- Estado: Vigente
- País:
- España
- Fecha solicitud:
- 28/06/2023
- Número solicitud:
-
P202330541
- Número publicación:
-
ES2957299
- Fecha de concesión:
-
- Inventores:
-
Persona física
- Datos del titular:
-
Persona física
- Datos del representante:
-
- Clasificación Internacional de Patentes:
- G01T 1/20,G01T 1/161,A61B 6/00
- Clasificación Internacional de Patentes de la publicación:
- G01T 1/20,G01T 1/161,A61B 6/00
- Fecha de vencimiento:
Quiero registrar una patente
Reivindicaciones:
+ ES-2957299_A11. Detector para la medida no invasiva de la función de entrada arterial que consiste en: - entre una y cinco fibras centelleadoras (1) , - un único fotodetector acoplado a la/las fibras centelleadoras (1) , - al menos, una placa electrónica, donde la/las fibras centelleadoras (1) tienen una disposición esencialmente rectilínea. 2. Detector según la reivindicación 1 en el que las fibras centelleadoras (1) están dispuestas de forma adyacente cuando son más de una. 3. Detector según la reivindicación 1 en el que las fibras centelleadoras (1) están dispuestas esencialmente en un único plano cuando son más de dos. 4. Detector según cualquiera de las reivindicaciones anteriores en el que la/las fibras centelleadoras (1) tienen un diámetro comprendido entre 250 m y 2 mm y una longitud entre 1 y20cm. 5. Detector según cualquiera de las reivindicaciones anteriores en el que la sección de la/las fibras centelleadoras (1) puede ser circular, cuadrada o rectangular. 6. Detector según cualquiera de las reivindicaciones anteriores en el que el fotodetector es un fotomultiplicador de silicio (SiPM) (2) . 7. Detector según cualquiera de las reivindicaciones anteriores en el que se incorpora un identificador de venas y arterias. 8. Detector según la reivindicación 7 en el que el identificador de venas y arterias es un LED de color rojo, infrarrojo o naranja. 9. Detector para la medida no invasiva de la función de entrada arterial que consiste en: - entre dos y diez fibras centelleadoras (1) , - dos únicos fotodetectores acoplados a las fibras centelleadoras (1) , - al menos, una placa electrónica (3) , donde las fibras centelladoras (1) tienen una disposición esencialmente rectilínea, donde entre una y la mitad de las fibras centelladoras (1) están recubiertas con un material de blindaje (10) capaz de absorber los positrones antes de que alcancen la fibra centelleadora (1) , donde uno de los fotodetectores está acoplado a la/las fibras centelleadoras (1) sin blindaje y el otro fotodetector está acoplado a la/las fibras centelleadoras (1) con blindaje. 10. Dispositivo según la reivindicación 9 en el que las fibras centelleadoras (1) están dispuestas de forma adyacente y, cuando son más de dos, esencialmente en un mismo plano. 11. Dispositivo según cualquiera de las reivindicaciones 9-10 en el que el material de blindaje es un material de alta densidad. 12. Detector según la reivindicación 11 en el que el material de blindaje (10) se selecciona del grupo formado por aluminio, acero, plomo, cobre, tungsteno, polietileno, polimetilmetacrilato y/o teflón. 13. Detector según cualquiera de las reivindicaciones 9-12 en el que los fotodetectores son fotomultiplicadores de silicio (SiPM) (2) . 14. Detector según cualquiera de las reivindicaciones 9-13 en el que la lectura de cada fotodetector es independiente de la lectura del otro fotodetector. 15. Detector según cualquiera de las reivindicaciones 9-14 en el que se incorpora un identificador de venas y arterias. 16. Detector según la reivindicación 15 en el que el identificador de venas y arterias es un LED de color rojo, infrarrojo o naranja.
Los productos y servicios protegidos por este registro son:
G01T 1/20 - G01T 1/161 - A61B 6/00
Descripciones:
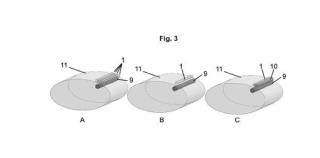
+ ES-2957299_A1 DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL SECTOR DE LA TÉCNICA La presente invención se encuadra en el sector de la medicina nuclear y, en concreto, en el sector de la tomografía por emisión de positrones (PET) como técnica de imagen molecular. Dentro de este sector de la técnica, la invención se refiere a sistemas y métodos para la medición de la función de entrada arterial de forma no invasiva en estudios farmacocinéticos PET. ANTECEDENTES DE LA INVENCIÓN La tomografía por emisión de positrones (PET) es una técnica de medicina nuclear que produce imágenes de distribución de diferentes moléculas (radiofármacos) , por lo que se considera una técnica de imagen molecular. Proporciona información funcional, que se complementa con la información suministrada por técnicas como la resonancia magnética (RM) o la tomografía axial computarizada (TC) para producir imágenes de gran utilidad en oncología, cardiología, neurología y otras especialidades. Para la realización de esta técnica, se administra un radiofármaco al paciente que consiste en cantidades traza de compuestos biológicamente activos marcados con radionucleidos emisores de positrones (11C, 150, 13N, 68Ga, 64Cu o 18F) . Por ejemplo, el flujo sanguíneo puede medirse utilizando agua marcada con 150 y el metabolismo se puede medir con fluorodesoxiglucosa marcada con 18F (18F-FDG) . En la actualidad, la mayor parte de los estudios PET que se realizan, tanto en su aplicación clínica como preclínica, comienzan un cierto tiempo después de la inyección del radiofármaco. De este modo, se adquiere una imagen estática de la distribución del radiotrazador en el organismo y, posteriormente, se realiza un análisis mediante índices semicuantitativos. Este tipo de análisis conllevan muchas limitaciones incluyendo factores biológicos, como el nivel de glucosa en sangre, el tiempo de incorporación del radiofármaco y el movimiento respiratorio y cardiaco, y factores tecnológicos, como la variabilidad entre escáneres, los parámetros de adquisición y econstrucción de imágenes y la variabilidad entre observadores. Otro modo de realizar estudios PET es mediante la aplicación de protocolos de adquisición de imágenes dinámicas y de modelos farmacocinéticos permitiendo extraer mucha más información de interés biológico y médico. Sin embargo, debido a su complejidad metodológica, estos protocolos han estado restringidos principalmente al desarrollo de nuevos medicamentos y a aplicaciones de investigación clínica y preclínica. Una de las áreas de mejora en los estudios farmacocinéticos realizados con PET se centra en la medición de la concentración de radiofármacos en sangre que, habitualmente, se obtiene partiendo de una extracción de sangre, es decir, de forma invasiva con los problemas y riesgos que ello conlleva. Existen trabajos que buscan la detección de la función de entrada arterial de forma no invasiva; entre estos trabajos, cabe citar los siguientes. El documento US2020163633A1 hace referencia a un método y un sistema no invasivos para establecer la función de entrada arterial en tomografías por emisión de positrones y tomografías computarizadas por emisión de fotón único. Se determina una posición de interacción a lo largo de una bobina de fibra centelleadora, detectando una primera pluralidad y una segunda pluralidad de fotones en cada uno de los extremos de la fibra. De esta manera se determina la posición de la interacción mediante un parámetro de temporización. El dispositivo que se describe en esta solicitud de patente propone la utilización de fibra curvada con múltiples configuraciones posibles (circular, en S, en zigzag y similares) . Para discriminar la radiación proveniente de las arterias del resto de radiación, la patente propone la medida de la luz visible de la fibra de manera simultánea en los dos extremos de la misma, tanto utilizando dos fotodetectores (uno en cada extremo) como utilizando un fotodetector común a los dos extremos. Por otro lado, para discriminar la radiación de la arteria del resto de la radiación que mide la fibra, esta invención requiere la medida simultánea de la luz visible en ambos extremos de la fibra, por lo que la señal eléctrica medida en ambos fotodetectores debe ser procesada por una unidad de coincidencia y un módulo de posicionamiento. El documento WO2018150348A1 divulga un sistema no invasivo para la medición de la función de entrada arterial en PET, en concreto para la medición de radiación gamma. El sistema comprende unos transductores que se fijan al cuerpo del paciente cada transductor comprende a su vez un cristal de centelleo encapsulado en un conductor, un fotodiodo, un módulo de amplificación y un módulo de control y comunicación. En esta invención, los datos enviados por los transductores se procesan mediante un dispositivo de procesamiento externo. En US2012232381A1 se describe un sistema para cuantificar los niveles de radionucleidos en el torrente sanguíneo que comprende una unidad de procesamiento conectada a un contador de centelleo gamma que proporciona una señal que representa la concentración de radionucleidos. El contador consiste en una sonda que se coloca sobre el cuerpo del paciente. El sistema es adecuado para acceder cuantitativamente a los niveles de radionucleidos en el torrente sanguíneo, diagnosticar la enfermedad de Alzheimer, localizar focos de convulsiones, diagnosticar o estudiar la aterosclerosis y las enfermedades vasculares, identificar el miocardio en hibernación, así como para estudiar la esquizofrenia y diagnosticar trastornos del estado de ánimo y afecciones psiquiátricas. El documento titulado "Non-invasive positrón detector to monitor the input function in pet" (Turgeon V; Nejad Enger S A Kertzscher G, 60th Annual Meeting of the American-Association-of-Physicists-in-Medicine, 2018) hace referencia a un sistema para caracterizar la atenuación, las pérdidas por flexión y la respuesta a los positrones de un sistema de detección de muñeca basado en una fibra centelleadora, adecuado para determinar la función de entrada arterial en PET. Se evalúan las pérdidas de señal para diferentes radios de curvatura y se compara la relación de salida de bucles con diferentes radios con una fibra recta, para determinar las posibles pérdidas de señal. El artículo "Characterization of scintillating fibers for use as positrón detector in positrón emission tomography" de Turgeon, V. et al., de 2019 (Physica Medica 65:114-120) , se centra en la caracterización de las fibras centelleadoras utilizadas para desarrollar un detector de positrones no invasivo. El detector consiste en una fibra centelleadora acoplada en cada extremo a cables de fibra óptica de transmisión que están conectados a tubos fotomultiplicadores en una configuración de lectura dual. El detector está diseñado para ser enrollado alrededor de la muñeca del paciente sometido a PET dinámica. La longitud de atenuación y las pérdidas por flexión se midieron con excitación de radiación gamma (137Cs) y luz ultravioleta (UV) . La respuesta a los radiotrazadores emisores de positrones se evaluó con 18F y 11C. En el documento "Cross-validation of a non-invasive positrón detector to measure the arterial input function for pharmacokinetic modelling in dynamic positrón emission tomography" (Carroll, L. et al. 2020. Physica Medica 76:92-99) se describen los ensayos realizados con un detector de positrones no invasivo, previamente descrito, comparando sus resultados con un detector de positrones microfluídico invasivo también conocido. Un primer diseño está basado en una fibra centelleadora de plástico de 3 m de longitud con cada extremo acoplado a una fibra de transmisión de 5 m de longitud seguida de un fotomultiplicador de silicio. La fibra centelleadora está encerrada en las ranuras de una carcasa cilindrica de ácido poliláctico (PLA) impresa en 3D y dispuesta en bucles con un diámetro de 100 mm y un paso de 10 mm por bucle, con un total de diez bucles. En un segundo diseño la fibra centelleadora se enrolló alrededor de un manguito de PLA impreso en 3D que sujeta la fibra en una bobina con 16 bucles de 50 mm de diámetro cada uno y un paso de 5 mm. Carroll, L. y Enger, S.A, en su artículo "Simulation of a novel, non-invasive radiation detector to measure the arterial input function for dynamic positrón emission tomography" (Medical Physics, Nov 2022;1-13) , describen mejoras del dispositivo del párrafo anterior. Se simularon dos geometrías con diferentes disposiciones de las fibras centelleadoras: en el primer diseño se utilizó una sola capa de 64 fibras y en el segundo se utilizaron 59 fibras distribuidas en dos capas, una interior con 29 fibras y otra exterior con 30 fibras. En principio, funcionó mejor la segunda geometría aunque los autores destacan la necesidad de hacer pruebas in vivo. Teniendo en cuenta los documentos citados, en el ámbito de la medicina nuclear aún es necesario mejorar la medición de radiofármacos en sangre de manera no invasiva, es decir, sin necesidad de obtener muestras de sangre del paciente, y desarrollar un dispositivo adecuado para ello. EXPLICACIÓN DE LA INVENCIÓN Detector para la medida no invasiva de la función de entrada arterial. Para obtener de manera precisa la medida temporal de la concentración de radiofármacos en sangre arterial, es decir, de la función de entrada arterial o AIF, se resenta un dispositivo capaz de medir la AIF de manera no invasiva. Un aspecto de la presente invención se refiere a un dispositivo para la medida no invasiva de la AIF que incluye una fibra centelleadora con disposición esencialmente rectilínea acoplada por uno de sus extremos a un único fotodetector, preferentemente un fotomultiplicador de silicio (SiPM) , conectado con una placa electrónica, de tal manera que, para tomar las medidas, el dispositivo se pueda colocar de forma que la fibra centelleadora quede esencialmente alineada con el vaso sanguíneo u órgano en el que se quiere medir la concentración de radiofármaco. Por otro lado, el detector para la medida no invasiva de la AIF puede tener más de una fibra centelleadora, hasta cinco fibras centelleadoras adyacentes unas a otras y dispuestas en un único plano cuando son 3 o más, con disposición esencialmente rectilínea. Aunque sean varias, todas las fibras centelleadoras se acoplan a un único fotodetector. Se pueden utilizar fibras centelleadoras con características variadas: su diámetro puede estar comprendido entre 250 m y 2 mm, su longitud puede ser de entre 1 y 20 cm; su sección puede ser circular, cuadrada o rectangular. Opcionalmente, el detector para la medida no invasiva de la AIF puede incorporar un identificador de venas y arterias o de otros órganos de interés. Para la identificación de la localización de venas y arterias, se pueden utilizar LED de color rojo, naranja o infrarrojo. Los positrones se propagan por los tejidos disminuyendo su energía hasta que eventualmente la pierden casi por completo y se aniquilan con un electrón del medio emitiéndose mayoritariamente 2 fotones gamma de 511 keV. Sin embargo, en los tejidos superficiales, una parte de los positrones emitidos puede llegar hasta la piel del paciente y escapar al exterior. De este modo, la fibra centelleadora puede detectar estos positrones y proporcionar una medida directa del radiotrazador presente en el vaso sanguíneo o en el órgano junto al que está situada. Al tratarse de un detector con un volumen de detección pequeño y una densidad baja, la detección de fotones gamma provenientes del resto del cuerpo es muy baja mientras que la detección de los positrones se realiza de manera muy eficiente. Sin embargo, es posible que en lgunos casos sea necesario estimar la cantidad de fotones gamma medidos por la fibra ya que constituyen un fondo que debemos diferenciar de los positrones. Para ello, un segundo aspecto de la invención se refiere a un dispositivo para la medida no invasiva de la AIF que, además de disponer de una fibra centelleadora con disposición esencialmente rectilínea acoplada por uno de sus extremos a un único fotodetector conectado con una placa electrónica, de tal manera que, para tomar las medidas, el dispositivo se pueda colocar de forma que la fibra centelleadora quede alineada con el vaso sanguíneo u órgano en el que se quiere medir la concentración de radiofármaco, incluye una segunda fibra centelleadora situada de forma adyacente y esencialmente paralela a la primera y recubierta de un material de alta densidad que permita absorber los positrones antes de que alcancen la propia fibra. El material de alta densidad puede ser un metal o un plástico, pudiendo seleccionarse del grupo formado por: aluminio, acero, plomo, cobre, tungsteno, polietileno, polimetilmetacrilato y/o teflón. Este revestimiento o blindaje apenas afecta a la detección de fotones gamma y, por tanto, esta fibra proporciona una estimación directa de la radiación de fondo medida en la primera fibra. La fibra recubierta con el blindaje de material de alta densidad se acopla a un segundo fotodetector y este a la placa electrónica con un canal de lectura independiente. Preferentemente, como fotodetectores, se seleccionan fotomultiplicadores de silicio (SiPM) La fibra centelleadora, tanto la que lleva blindaje como la que no lleva blindaje, puede tener una sección transversal de forma circular, cuadrada o rectangular, entre otras. El tamaño de la fibra centelleadora, en ambos casos, puede variar en función de la aplicación. En términos generales la longitud de la fibra puede oscilar entre 1 y20cm en función de la extensión de la región a cubrir. El tamaño transversal de la fibra, con o sin blindaje, puede oscilar entre 250 p m y 2 mm en función del tamaño transversal de la región a cubrir y del rango de la partícula beta que queramos detectar. La fibra centelleadora puede estar formada por una única fibra del tamaño deseado o por una agrupación de entre 2 y 5 fibras más pequeñas que juntas alcanzan el tamaño deseado. En cualquiera de los casos, la fibra o agrupación de fibras se acoplan a un único SiPM para medir la luz visible en uno de los extremos de la fibra centelleadora. Si el dispositivo incluye fibras centelleadoras con blindaje, estas pueden estar en el ismo número que las fibras sin blindaje y pueden estar distribuidas entre ellas o bien separadas en dos grupos: un grupo con blindaje y otros grupo sin blindaje, si bien todas ellas tendrán disposición esencialmente rectilínea, esencialmente paralelas unas a otras, adyacentes y en un único plano cuando sean más de dos. El objetivo de esta invención es poder aplicar esta metodología tanto en estudios clínicos con humanos como en estudios preclínicos con animales. En cada caso debemos adaptar el diseño del detector para obtener resultados óptimos. En el caso de estudios clínicos en humanos los vasos sanguíneos tienen varios milímetros de diámetro y están situados a varios milímetros de profundidad bajo la piel. Por otro lado, el ratón, que es el animal más utilizado en ensayos preclínicos, posee unos vasos sanguíneos de unos pocos cientos de mieras de diámetro y están situados a una profundidad también de pocas mieras. Otra diferencia entre animales y humanos radica en la concentración de radiofármaco presente en sangre tras la inyección del radiofármaco, siendo mucho mayor en animales. La radiación de fondo que mida el detector proveniente del radiofármaco distribuido por el resto del cuerpo es también distinta ya que en humanos la actividad total es mayor y está distribuida por un volumen mucho mayor mientras que en ratones la actividad total es menor aunque se distribuyen en un volumen mucho más pequeño y cercano al detector. Otro aspecto importante en este dispositivo es la colocación de la fibra centelleadora a lo largo del vaso u órgano estudiado. Esta tarea podemos realizarla mediante la utilización de emisores (LED, por ejemplo) y detectores de luz (fotodiodos, por ejemplo) para detectar la posición del vaso u órgano aprovechando las diferentes características de absorción lumínica de los tejidos. BREVE DESCRIPCIÓN DE LOS DIBUJOS Para complementar la descripción que se está realizando y con objeto de ayudar a una mejor comprensión de las características de la invención, se acompaña como parte integrante de dicha descripción un juego de figuras en donde, con carácter ilustrativo y no limitativo, se ha representado lo que se muestra a continuación. Se proporciona, además, una lista de los distintos elementos representados en las figuras que forman parte de esta memoria descriptiva: 1: fibra centelladora 2: SiPM 3: placa electrónica 4: sistema de digitalización de la señal 5: ordenador 6: sección transversal de la cola de un ratón 7: vena 8: hueso 9: arteria 10: blindaje 11: antebrazo 12: luz LED Figura 1. Detector basado en una fibra centelleadora (1) con disposición rectilínea y acoplada a un SiPM (2) , y toda la cadena digitalizadora: placa electrónica (3) , sistema de digitalización de la señal (4) y sistema de procesamiento de datos (5) . Figura 2. Esquema del posicionamiento del detector junto a la arteria (9) de la cola de un ratón. Se muestra una versión con una fibra centelleadora (1) y otra fibra centelleadora (1) adicional con blindaje (10) para la medida del fondo de radiación gamma. Figura 3. Esquema del posicionamiento del detector cerca de la arteria (9) radial en el antebrazo (11) de un paciente. Se muestran 3 versiones: con 4 fibras centelleadoras (1) de sección cuadrada adyacentes y esencialmente paralelas entre sí (Fig. 3A) , con 1 fibra centelleadora (1) de sección circular (Fig. 3B) y con 2 fibras centelleadoras (1) de sección circular adyacentes y esencialmente paralelas entre sí, una de las cuales incluye blindaje (10) y se utiliza para la medida del fondo de radiación gamma (Fig.3C) . Figura 4. Esquema de la utilización de un emisor de luz, luz LED (12) , para ayudar en el correcto posicionamiento del detector sobre la arteria (9) de la cola de un ratón. REALIZACIÓN PREFERENTE DE LA INVENCIÓN La presente invención se ilustra mediante los siguientes ejemplos, que no pretenden er limitativos de su alcance. En la figura 1 se muestra un esquema del detector para la medida no invasiva de la función de entrada arterial que muestra una fibra centelleadora (1) acoplada a un SiPM (2) , una placa electrónica (3) , un sistema de digitalización de la señal (4) y un sistema de procesamiento de datos (5) . Ejemplo 1. Simulaciones Monte Cario. Los métodos Monte Cario permiten la simulación estadística de procesos físicos a partir del muestreo de las variables aleatorias que los caracterizan. Para ello, los métodos se basan en la continua generación de variables aleatorias mediante números aleatorios generados con algoritmos. En este ejemplo se utilizó el software PeneloPET (España, S. et al. Phys. Med. Biol. 54 (2009) 1723-1742; doi:10.1088/0031-9155/54/6/021) , que es un código Monte Cario especializado en simular la propagación de electrones, positrones y rayos gamma para estudiar la eficiencia y otras propiedades de escáneres PET. Ejemplo 1.1. Validación del software Para verificar el correcto funcionamiento del programa, se comprobó que la emisión de positrones de la fuente de 18F simulada presentaba un branching-ratio, espectro de emisión y rango en agua compatibles con los datos disponibles en el estado de la técnica. Con este fin, se simularon 5041 decaimientos en una fuente cilindrica de 18F dentro de un cilindro de agua y se comprobó que un 96, 88% de los decaimientos habían generado positrones, siendo este porcentaje muy similar al branching-ratio tabulado 96, 86% (http://nucleardata.nuclear.lu.se/toi/nuclide.asp?iZA=90018) . Así mismo se ha comprobado que la distribución del rango del positrón se corresponde con los resultados conocidos en el estado de la técnica obteniendo un rango medio y máximo en agua para el 18F de 0.5 y 2.1 mm, respectivamente (J. Cal-Gonzalez, J.L. Herraiz, S. España, P.M.G Corzo, J.J. Vaquero, M. Deseo, & J.M. Udias. Positrón range estimationswith PeneloPET. Phys. Med. Biol., volume 58, number 15) . Ejemplo 1.2. Viabilidad de medidas en ratón. Se utilizó el software PeneloPET para determinar de forma teórica la viabilidad de edidas en arteria (9) de cola de ratón. Para ello se estimó su eficiencia de detección para la radiación emitida desde la arteria (9) y el efecto de posibles contaminaciones procedentes de venas (7) y del cuerpo del ratón en la medida. Se estudió la eficiencia de detección de una fibra centelleadora (1) de 1 mm de diámetro situada de forma esencialmente rectilínea junto la arteria (9) de la cola de un ratón que contenía una concentración de 1 MBq/ml de 18F o 68Ga. Adicionalmente, se simuló el efecto de fuentes externas de radiación calculando la eficiencia de detección de la fibra centelleadora (1) para la radiación proveniente de las venas (7) de la cola y el cuerpo del ratón. En la figura 2 se muestran una sección transversal (6) de la cola del ratón y el detector de la invención. La cola del ratón se simuló como un cilindro de agua de 3, 2 mm de diámetro, en su interior se añadió un cilindro de 1 mm que simula el hueso (8) de la cola y, dentro de la cola, se añadieron cuatro cilindros adicionales que se corresponden con los vasos sanguíneos. El diámetro de la arteria (9) simulada es de 100 mieras y el de cada una de las venas (7) , de 200 mieras. De este modo se obtuvo una eficiencia de detección de un 16-18% para el 18F y de un 18-22% para el 68Ga, que se justifica por el mayor rango de los positrones emitidos por el galio. Teniendo en cuenta las simulaciones de fondo, se calculó la actividad mínima detectable para medidas de 1 segundo, obteniendo valores de 90 kBq/mL y 40 kBq/mL para el 18F y 68Ga, respectivamente. Estos valores están muy por debajo de las concentraciones iniciales de radiotrazador en sangre en estudios PET con ratones, que suelen oscilar entre los 500 y los 1000 kBq/mL. Por consiguiente, concluimos que el dispositivo detector es viable para la medición de la función de entrada arterial en ratones. Ejemplo 2.1. Dispositivo detector Se realizaron varios ensayos con una fibra centelleadora (1) utilizando distintos modelos: SCFSF-81J, SCSF-78J RD, SCSF-78 MJ y SCSF-78J SQ de la marca Kuraray de 1 mm de diámetro y un revestimiento de 0, 02 mm. El material de centelleo utilizado fue el poliestireno (PS) y el de revestimiento, el polimetacrilato de metilo (PMMA) . La longitud de la fibra era de 5 cm. Como fotodetectores se utilizaron SiPMs (2) , concretamente se probaron los modelos ASD-NUV4S-P y ASD-RGB4S-P de 4x4 mm2 de área sensible y los modelos ASD-NUV1S-P y ASD-RGB1S-P de 1 x 1 mm2 de área sensible de AdvanSiD. El acoplamiento entre la fibra centelleadora (1) y el SiPM (2) se realizó mediante grasa óptica BC-630 de Saint Gobain. Se utilizó una lámina de Tediar® (que es un fluoropolímero) para aislar ópticamente la fibra centelleadora (1) del exterior. Como sustento mecánico del dispositivo detector se dispuso de una carcasa de plástico construida mediante impresión 3D. Para la amplificación y conformación de los pulsos electrónicos se utilizó la placa electrónica (3) ASD-EP-EB-PZ, de AdvanSiD. Los pulsos eléctricos generados por la radiación detectada se registraron mediante un sistema de digitalización de la señal (4) que, en estos ejemplos, fue un osciloscopio digital del modelo PicoScope 3403D, de cuatro canales y un ancho de banda de 50 MHz. La adquisición de datos se controló desde un ordenador, como sistema de procesamiento de datos (5) , utilizando un software que gestiona y procesa los datos medidos con el osciloscopio. Para comprobar el correcto funcionamiento del detector se situó una fuente puntual de 22Na y 10 Ci de actividad a 1 mm de distancia de la fibra centelleadora (1) . En la tabla 1 se muestran las tasas de eventos medidos con la fibra centelleadora (1) SCFSF-81J acoplada, en ensayos independientes, a cada uno de los SiPMs (2) mencionados en este ejemplo. Así mismo, se muestran los resultados obtenidos utilizando el SiPM ASD-NUV4S-P acoplado a las distintas fibras centelleadoras (1) mencionadas en este ejemplo. De todas la pruebas realizadas, la que ofrece mejores resultados es la prueba en la que utilizamos el SiPM (2) ASD-NUV4S-P de 4x4 mm2 de área sensible y la fibra centelleadora (1) SCSF-78J SQ con sección de forma cuadrada de 1x1 mm2. Tabla 1 Ejemplo 2.2. Versión 1 del dispositivo detector Se realizaron dispositivos detectores como los descritos en el ejemplo 2.1 y se añadió na segunda fibra centelleadora (1) conectada a un segundo SiPM (2) . En cada detector, ambas fibras tenían 7 cm de longitud y se dispusieron contiguas y paralelas entre sí a una distancia 3 mm. Una de las fibras se blindó de la radiación beta rodeándola con un cilindro de cobre de 500m de grosor que constituyó el blindaje (10) (Figuras 2 y 3C) . Ejemplo 2.3. Versión 2 del dispositivo detector En el caso de aplicación en humanos, el tamaño del vaso sanguíneo y la distancia entre la fibra centelleadora (1) y el vaso está en torno a los 2 mm de diámetro y 2 mm de profundidad, respectivamente, lo cual es mucho más que para ratones. Por tanto, en humanos podemos utilizar fibras centelleadoras (1) de mayor tamaño transversal. Como ejemplo hemos simulado distinto número de fibras centelleadoras de sección cuadrada situadas a 2 mm de la superficie de un vaso de 2 mm de diámetro en el que se sitúa una distribución uniforme de radiofármaco marcado con Ga-68. Se han simulado entre 1 y 4 fibras centelleadoras de 1x1 mm2 de sección y 5 cm de longitud, dispuestas de manera contigua y en un único plano (figura 3A) y de forma esencialmente rectilínea. Las simulaciones nos permiten concluir que un número mayor de fibras da lugar a una mayor sensibilidad de detección obteniendo valores de 1, 6, 2, 7, 3, 7 y 4, 4 % para 1, 2, 3 y 4 fibras centelleadoras (ver figura 3) . Todas las fibras centelleadoras (1) pueden acoplarse a un solo SiPM (2) lo que permite simplificar la electrónica de lectura. Para validar experimentalmente estas medidas se implementaron 3 detectores con 1, 2 y 4 fibras SCSF-78J SQ con 7cm de longitud acopladas a un SiPM ASD-RGB4S-P. Se situó una fuente puntual de Na-22 a 2 mm de las fibras registrando 2179, 3412 y 8837 cuentas por segundo para los detectores de 1, 2 y 4 fibras respectivamente. Basándonos en los detectores descritos más arriba en este mismo ejemplo, realizamos un detector en el que se incluyó una fibra centelleadora (1) con blindaje (10) para la medida de fondo por cada una de las fibras centelleadoras (1) de la parte detectora de partículas beta, cada fibra centelleadora (1) se acopló a un SiPM (2) distinto para su lectura de manera independiente y el blindaje (10) se consiguió rodeando la fibra centelleadora (1) con un material que impide la llegada de partículas beta. En este ejemplo, el detector incluyó una fibra SCSF-78J SQ con 7cm de longitud acoplada a un SiPM ASD-RGB4S-P. La fibra centelleadora (1) se introdujo dentro de un cilindro ueco de cobre con 1.5 mm de grosor y 7 cm de longitud como blindaje (10) . Con este detector, se realizaron medidas utilizando una fuente de Na-22 situada a 2 mm del detector, obteniendo una tasa de eventos de 287. Como control, para frenar todos los positrones antes de que alcancen el detector, se intercaló una lámina de aluminio de 2 mm de grosor entre la fuente y el detector, obteniendo en este caso una tasa de eventos de 284. Por tanto, se comprobó que el detector detecta en ambos casos únicamente fotones gamma que emite la fuente y el blindaje (10) de cobre funciona correctamente. Ejemplo 2.4 Se elaboró un nuevo dispositivo detector en el que se incluyó un sistema de apoyo para el posicionamiento del propio dispositivo detector de manera que la fibra centelleadora (1) esencialmente rectilínea esté situada lo más próxima posible al vaso sanguíneo del que se desea medir la concentración de radiofármaco. Para conseguir esto, se incluyó una luz LED que podía seleccionarse entre el color naranja, el infrarrojo y el rojo dispuesta de tal manera que incidiera sobre la piel del sujeto, facilitando la identificación visual de los vasos sanguíneos. Es conocido que la luz reflejada por la sangre venosa, la sangre arterial y otros tejidos difiere, lo que ayuda a localizar el vaso que se desea monitorizar. Se elaboraron detectores como los descritos en los ejemplos 2.2 y 2.3, para su utilización en animales que, a continuación de la fibra centelleadora (1) incluían LED de color rojo con los que se ilumina la región de la cola donde se inyecta el radiotrazador y que permiten localizar con facilidad los vasos sanguíneos tanto para el posicionamiento del detector como para la inyección (figura 4) .
Publicaciones:
ES2957299 (16/01/2024) - A1 Solicitud de patente con informe sobre el estado de la técnica
Eventos:
En fecha 28/06/2023 se realizó Registro Instancia de Solicitud
En fecha 29/06/2023 se realizó Admisión a Trámite
En fecha 29/06/2023 se realizó Aceptación Tramitación CAP
En fecha 29/06/2023 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 06/07/2023 se realizó Superado examen de oficio
En fecha 16/10/2023 se realizó Registro Documentación no Identificada
En fecha 16/10/2023 se realizó 3406X_Solicitud Correcciones
En fecha 14/11/2023 se realizó 1550X_Notificación Rechazo Correcciones
En fecha 20/11/2023 se realizó Publicación Rechazo Correcciones
En fecha 25/12/2023 se realizó Realizado IET
En fecha 08/01/2024 se realizó 1109P_Comunicación Traslado del IET
En fecha 16/01/2024 se realizó Publicación Solicitud
En fecha 16/01/2024 se realizó Publicación Folleto Solicitud con IET (A1)
Pagos:
20/06/2023 - Pago Tasas IET
20/06/2023 - Pago Tasas IET
+ ES-2957299_A11. Detector para la medida no invasiva de la función de entrada arterial que consiste en: - entre una y cinco fibras centelleadoras (1) , - un único fotodetector acoplado a la/las fibras centelleadoras (1) , - al menos, una placa electrónica, donde la/las fibras centelleadoras (1) tienen una disposición esencialmente rectilínea. 2. Detector según la reivindicación 1 en el que las fibras centelleadoras (1) están dispuestas de forma adyacente cuando son más de una. 3. Detector según la reivindicación 1 en el que las fibras centelleadoras (1) están dispuestas esencialmente en un único plano cuando son más de dos. 4. Detector según cualquiera de las reivindicaciones anteriores en el que la/las fibras centelleadoras (1) tienen un diámetro comprendido entre 250 m y 2 mm y una longitud entre 1 y20cm. 5. Detector según cualquiera de las reivindicaciones anteriores en el que la sección de la/las fibras centelleadoras (1) puede ser circular, cuadrada o rectangular. 6. Detector según cualquiera de las reivindicaciones anteriores en el que el fotodetector es un fotomultiplicador de silicio (SiPM) (2) . 7. Detector según cualquiera de las reivindicaciones anteriores en el que se incorpora un identificador de venas y arterias. 8. Detector según la reivindicación 7 en el que el identificador de venas y arterias es un LED de color rojo, infrarrojo o naranja. 9. Detector para la medida no invasiva de la función de entrada arterial que consiste en: - entre dos y diez fibras centelleadoras (1) , - dos únicos fotodetectores acoplados a las fibras centelleadoras (1) , - al menos, una placa electrónica (3) , donde las fibras centelladoras (1) tienen una disposición esencialmente rectilínea, donde entre una y la mitad de las fibras centelladoras (1) están recubiertas con un material de blindaje (10) capaz de absorber los positrones antes de que alcancen la fibra centelleadora (1) , donde uno de los fotodetectores está acoplado a la/las fibras centelleadoras (1) sin blindaje y el otro fotodetector está acoplado a la/las fibras centelleadoras (1) con blindaje. 10. Dispositivo según la reivindicación 9 en el que las fibras centelleadoras (1) están dispuestas de forma adyacente y, cuando son más de dos, esencialmente en un mismo plano. 11. Dispositivo según cualquiera de las reivindicaciones 9-10 en el que el material de blindaje es un material de alta densidad. 12. Detector según la reivindicación 11 en el que el material de blindaje (10) se selecciona del grupo formado por aluminio, acero, plomo, cobre, tungsteno, polietileno, polimetilmetacrilato y/o teflón. 13. Detector según cualquiera de las reivindicaciones 9-12 en el que los fotodetectores son fotomultiplicadores de silicio (SiPM) (2) . 14. Detector según cualquiera de las reivindicaciones 9-13 en el que la lectura de cada fotodetector es independiente de la lectura del otro fotodetector. 15. Detector según cualquiera de las reivindicaciones 9-14 en el que se incorpora un identificador de venas y arterias. 16. Detector según la reivindicación 15 en el que el identificador de venas y arterias es un LED de color rojo, infrarrojo o naranja.
Los productos y servicios protegidos por este registro son:
G01T 1/20 - G01T 1/161 - A61B 6/00
Descripciones:
+ ES-2957299_A1 DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL SECTOR DE LA TÉCNICA La presente invención se encuadra en el sector de la medicina nuclear y, en concreto, en el sector de la tomografía por emisión de positrones (PET) como técnica de imagen molecular. Dentro de este sector de la técnica, la invención se refiere a sistemas y métodos para la medición de la función de entrada arterial de forma no invasiva en estudios farmacocinéticos PET. ANTECEDENTES DE LA INVENCIÓN La tomografía por emisión de positrones (PET) es una técnica de medicina nuclear que produce imágenes de distribución de diferentes moléculas (radiofármacos) , por lo que se considera una técnica de imagen molecular. Proporciona información funcional, que se complementa con la información suministrada por técnicas como la resonancia magnética (RM) o la tomografía axial computarizada (TC) para producir imágenes de gran utilidad en oncología, cardiología, neurología y otras especialidades. Para la realización de esta técnica, se administra un radiofármaco al paciente que consiste en cantidades traza de compuestos biológicamente activos marcados con radionucleidos emisores de positrones (11C, 150, 13N, 68Ga, 64Cu o 18F) . Por ejemplo, el flujo sanguíneo puede medirse utilizando agua marcada con 150 y el metabolismo se puede medir con fluorodesoxiglucosa marcada con 18F (18F-FDG) . En la actualidad, la mayor parte de los estudios PET que se realizan, tanto en su aplicación clínica como preclínica, comienzan un cierto tiempo después de la inyección del radiofármaco. De este modo, se adquiere una imagen estática de la distribución del radiotrazador en el organismo y, posteriormente, se realiza un análisis mediante índices semicuantitativos. Este tipo de análisis conllevan muchas limitaciones incluyendo factores biológicos, como el nivel de glucosa en sangre, el tiempo de incorporación del radiofármaco y el movimiento respiratorio y cardiaco, y factores tecnológicos, como la variabilidad entre escáneres, los parámetros de adquisición y econstrucción de imágenes y la variabilidad entre observadores. Otro modo de realizar estudios PET es mediante la aplicación de protocolos de adquisición de imágenes dinámicas y de modelos farmacocinéticos permitiendo extraer mucha más información de interés biológico y médico. Sin embargo, debido a su complejidad metodológica, estos protocolos han estado restringidos principalmente al desarrollo de nuevos medicamentos y a aplicaciones de investigación clínica y preclínica. Una de las áreas de mejora en los estudios farmacocinéticos realizados con PET se centra en la medición de la concentración de radiofármacos en sangre que, habitualmente, se obtiene partiendo de una extracción de sangre, es decir, de forma invasiva con los problemas y riesgos que ello conlleva. Existen trabajos que buscan la detección de la función de entrada arterial de forma no invasiva; entre estos trabajos, cabe citar los siguientes. El documento US2020163633A1 hace referencia a un método y un sistema no invasivos para establecer la función de entrada arterial en tomografías por emisión de positrones y tomografías computarizadas por emisión de fotón único. Se determina una posición de interacción a lo largo de una bobina de fibra centelleadora, detectando una primera pluralidad y una segunda pluralidad de fotones en cada uno de los extremos de la fibra. De esta manera se determina la posición de la interacción mediante un parámetro de temporización. El dispositivo que se describe en esta solicitud de patente propone la utilización de fibra curvada con múltiples configuraciones posibles (circular, en S, en zigzag y similares) . Para discriminar la radiación proveniente de las arterias del resto de radiación, la patente propone la medida de la luz visible de la fibra de manera simultánea en los dos extremos de la misma, tanto utilizando dos fotodetectores (uno en cada extremo) como utilizando un fotodetector común a los dos extremos. Por otro lado, para discriminar la radiación de la arteria del resto de la radiación que mide la fibra, esta invención requiere la medida simultánea de la luz visible en ambos extremos de la fibra, por lo que la señal eléctrica medida en ambos fotodetectores debe ser procesada por una unidad de coincidencia y un módulo de posicionamiento. El documento WO2018150348A1 divulga un sistema no invasivo para la medición de la función de entrada arterial en PET, en concreto para la medición de radiación gamma. El sistema comprende unos transductores que se fijan al cuerpo del paciente cada transductor comprende a su vez un cristal de centelleo encapsulado en un conductor, un fotodiodo, un módulo de amplificación y un módulo de control y comunicación. En esta invención, los datos enviados por los transductores se procesan mediante un dispositivo de procesamiento externo. En US2012232381A1 se describe un sistema para cuantificar los niveles de radionucleidos en el torrente sanguíneo que comprende una unidad de procesamiento conectada a un contador de centelleo gamma que proporciona una señal que representa la concentración de radionucleidos. El contador consiste en una sonda que se coloca sobre el cuerpo del paciente. El sistema es adecuado para acceder cuantitativamente a los niveles de radionucleidos en el torrente sanguíneo, diagnosticar la enfermedad de Alzheimer, localizar focos de convulsiones, diagnosticar o estudiar la aterosclerosis y las enfermedades vasculares, identificar el miocardio en hibernación, así como para estudiar la esquizofrenia y diagnosticar trastornos del estado de ánimo y afecciones psiquiátricas. El documento titulado "Non-invasive positrón detector to monitor the input function in pet" (Turgeon V; Nejad Enger S A Kertzscher G, 60th Annual Meeting of the American-Association-of-Physicists-in-Medicine, 2018) hace referencia a un sistema para caracterizar la atenuación, las pérdidas por flexión y la respuesta a los positrones de un sistema de detección de muñeca basado en una fibra centelleadora, adecuado para determinar la función de entrada arterial en PET. Se evalúan las pérdidas de señal para diferentes radios de curvatura y se compara la relación de salida de bucles con diferentes radios con una fibra recta, para determinar las posibles pérdidas de señal. El artículo "Characterization of scintillating fibers for use as positrón detector in positrón emission tomography" de Turgeon, V. et al., de 2019 (Physica Medica 65:114-120) , se centra en la caracterización de las fibras centelleadoras utilizadas para desarrollar un detector de positrones no invasivo. El detector consiste en una fibra centelleadora acoplada en cada extremo a cables de fibra óptica de transmisión que están conectados a tubos fotomultiplicadores en una configuración de lectura dual. El detector está diseñado para ser enrollado alrededor de la muñeca del paciente sometido a PET dinámica. La longitud de atenuación y las pérdidas por flexión se midieron con excitación de radiación gamma (137Cs) y luz ultravioleta (UV) . La respuesta a los radiotrazadores emisores de positrones se evaluó con 18F y 11C. En el documento "Cross-validation of a non-invasive positrón detector to measure the arterial input function for pharmacokinetic modelling in dynamic positrón emission tomography" (Carroll, L. et al. 2020. Physica Medica 76:92-99) se describen los ensayos realizados con un detector de positrones no invasivo, previamente descrito, comparando sus resultados con un detector de positrones microfluídico invasivo también conocido. Un primer diseño está basado en una fibra centelleadora de plástico de 3 m de longitud con cada extremo acoplado a una fibra de transmisión de 5 m de longitud seguida de un fotomultiplicador de silicio. La fibra centelleadora está encerrada en las ranuras de una carcasa cilindrica de ácido poliláctico (PLA) impresa en 3D y dispuesta en bucles con un diámetro de 100 mm y un paso de 10 mm por bucle, con un total de diez bucles. En un segundo diseño la fibra centelleadora se enrolló alrededor de un manguito de PLA impreso en 3D que sujeta la fibra en una bobina con 16 bucles de 50 mm de diámetro cada uno y un paso de 5 mm. Carroll, L. y Enger, S.A, en su artículo "Simulation of a novel, non-invasive radiation detector to measure the arterial input function for dynamic positrón emission tomography" (Medical Physics, Nov 2022;1-13) , describen mejoras del dispositivo del párrafo anterior. Se simularon dos geometrías con diferentes disposiciones de las fibras centelleadoras: en el primer diseño se utilizó una sola capa de 64 fibras y en el segundo se utilizaron 59 fibras distribuidas en dos capas, una interior con 29 fibras y otra exterior con 30 fibras. En principio, funcionó mejor la segunda geometría aunque los autores destacan la necesidad de hacer pruebas in vivo. Teniendo en cuenta los documentos citados, en el ámbito de la medicina nuclear aún es necesario mejorar la medición de radiofármacos en sangre de manera no invasiva, es decir, sin necesidad de obtener muestras de sangre del paciente, y desarrollar un dispositivo adecuado para ello. EXPLICACIÓN DE LA INVENCIÓN Detector para la medida no invasiva de la función de entrada arterial. Para obtener de manera precisa la medida temporal de la concentración de radiofármacos en sangre arterial, es decir, de la función de entrada arterial o AIF, se resenta un dispositivo capaz de medir la AIF de manera no invasiva. Un aspecto de la presente invención se refiere a un dispositivo para la medida no invasiva de la AIF que incluye una fibra centelleadora con disposición esencialmente rectilínea acoplada por uno de sus extremos a un único fotodetector, preferentemente un fotomultiplicador de silicio (SiPM) , conectado con una placa electrónica, de tal manera que, para tomar las medidas, el dispositivo se pueda colocar de forma que la fibra centelleadora quede esencialmente alineada con el vaso sanguíneo u órgano en el que se quiere medir la concentración de radiofármaco. Por otro lado, el detector para la medida no invasiva de la AIF puede tener más de una fibra centelleadora, hasta cinco fibras centelleadoras adyacentes unas a otras y dispuestas en un único plano cuando son 3 o más, con disposición esencialmente rectilínea. Aunque sean varias, todas las fibras centelleadoras se acoplan a un único fotodetector. Se pueden utilizar fibras centelleadoras con características variadas: su diámetro puede estar comprendido entre 250 m y 2 mm, su longitud puede ser de entre 1 y 20 cm; su sección puede ser circular, cuadrada o rectangular. Opcionalmente, el detector para la medida no invasiva de la AIF puede incorporar un identificador de venas y arterias o de otros órganos de interés. Para la identificación de la localización de venas y arterias, se pueden utilizar LED de color rojo, naranja o infrarrojo. Los positrones se propagan por los tejidos disminuyendo su energía hasta que eventualmente la pierden casi por completo y se aniquilan con un electrón del medio emitiéndose mayoritariamente 2 fotones gamma de 511 keV. Sin embargo, en los tejidos superficiales, una parte de los positrones emitidos puede llegar hasta la piel del paciente y escapar al exterior. De este modo, la fibra centelleadora puede detectar estos positrones y proporcionar una medida directa del radiotrazador presente en el vaso sanguíneo o en el órgano junto al que está situada. Al tratarse de un detector con un volumen de detección pequeño y una densidad baja, la detección de fotones gamma provenientes del resto del cuerpo es muy baja mientras que la detección de los positrones se realiza de manera muy eficiente. Sin embargo, es posible que en lgunos casos sea necesario estimar la cantidad de fotones gamma medidos por la fibra ya que constituyen un fondo que debemos diferenciar de los positrones. Para ello, un segundo aspecto de la invención se refiere a un dispositivo para la medida no invasiva de la AIF que, además de disponer de una fibra centelleadora con disposición esencialmente rectilínea acoplada por uno de sus extremos a un único fotodetector conectado con una placa electrónica, de tal manera que, para tomar las medidas, el dispositivo se pueda colocar de forma que la fibra centelleadora quede alineada con el vaso sanguíneo u órgano en el que se quiere medir la concentración de radiofármaco, incluye una segunda fibra centelleadora situada de forma adyacente y esencialmente paralela a la primera y recubierta de un material de alta densidad que permita absorber los positrones antes de que alcancen la propia fibra. El material de alta densidad puede ser un metal o un plástico, pudiendo seleccionarse del grupo formado por: aluminio, acero, plomo, cobre, tungsteno, polietileno, polimetilmetacrilato y/o teflón. Este revestimiento o blindaje apenas afecta a la detección de fotones gamma y, por tanto, esta fibra proporciona una estimación directa de la radiación de fondo medida en la primera fibra. La fibra recubierta con el blindaje de material de alta densidad se acopla a un segundo fotodetector y este a la placa electrónica con un canal de lectura independiente. Preferentemente, como fotodetectores, se seleccionan fotomultiplicadores de silicio (SiPM) La fibra centelleadora, tanto la que lleva blindaje como la que no lleva blindaje, puede tener una sección transversal de forma circular, cuadrada o rectangular, entre otras. El tamaño de la fibra centelleadora, en ambos casos, puede variar en función de la aplicación. En términos generales la longitud de la fibra puede oscilar entre 1 y20cm en función de la extensión de la región a cubrir. El tamaño transversal de la fibra, con o sin blindaje, puede oscilar entre 250 p m y 2 mm en función del tamaño transversal de la región a cubrir y del rango de la partícula beta que queramos detectar. La fibra centelleadora puede estar formada por una única fibra del tamaño deseado o por una agrupación de entre 2 y 5 fibras más pequeñas que juntas alcanzan el tamaño deseado. En cualquiera de los casos, la fibra o agrupación de fibras se acoplan a un único SiPM para medir la luz visible en uno de los extremos de la fibra centelleadora. Si el dispositivo incluye fibras centelleadoras con blindaje, estas pueden estar en el ismo número que las fibras sin blindaje y pueden estar distribuidas entre ellas o bien separadas en dos grupos: un grupo con blindaje y otros grupo sin blindaje, si bien todas ellas tendrán disposición esencialmente rectilínea, esencialmente paralelas unas a otras, adyacentes y en un único plano cuando sean más de dos. El objetivo de esta invención es poder aplicar esta metodología tanto en estudios clínicos con humanos como en estudios preclínicos con animales. En cada caso debemos adaptar el diseño del detector para obtener resultados óptimos. En el caso de estudios clínicos en humanos los vasos sanguíneos tienen varios milímetros de diámetro y están situados a varios milímetros de profundidad bajo la piel. Por otro lado, el ratón, que es el animal más utilizado en ensayos preclínicos, posee unos vasos sanguíneos de unos pocos cientos de mieras de diámetro y están situados a una profundidad también de pocas mieras. Otra diferencia entre animales y humanos radica en la concentración de radiofármaco presente en sangre tras la inyección del radiofármaco, siendo mucho mayor en animales. La radiación de fondo que mida el detector proveniente del radiofármaco distribuido por el resto del cuerpo es también distinta ya que en humanos la actividad total es mayor y está distribuida por un volumen mucho mayor mientras que en ratones la actividad total es menor aunque se distribuyen en un volumen mucho más pequeño y cercano al detector. Otro aspecto importante en este dispositivo es la colocación de la fibra centelleadora a lo largo del vaso u órgano estudiado. Esta tarea podemos realizarla mediante la utilización de emisores (LED, por ejemplo) y detectores de luz (fotodiodos, por ejemplo) para detectar la posición del vaso u órgano aprovechando las diferentes características de absorción lumínica de los tejidos. BREVE DESCRIPCIÓN DE LOS DIBUJOS Para complementar la descripción que se está realizando y con objeto de ayudar a una mejor comprensión de las características de la invención, se acompaña como parte integrante de dicha descripción un juego de figuras en donde, con carácter ilustrativo y no limitativo, se ha representado lo que se muestra a continuación. Se proporciona, además, una lista de los distintos elementos representados en las figuras que forman parte de esta memoria descriptiva: 1: fibra centelladora 2: SiPM 3: placa electrónica 4: sistema de digitalización de la señal 5: ordenador 6: sección transversal de la cola de un ratón 7: vena 8: hueso 9: arteria 10: blindaje 11: antebrazo 12: luz LED Figura 1. Detector basado en una fibra centelleadora (1) con disposición rectilínea y acoplada a un SiPM (2) , y toda la cadena digitalizadora: placa electrónica (3) , sistema de digitalización de la señal (4) y sistema de procesamiento de datos (5) . Figura 2. Esquema del posicionamiento del detector junto a la arteria (9) de la cola de un ratón. Se muestra una versión con una fibra centelleadora (1) y otra fibra centelleadora (1) adicional con blindaje (10) para la medida del fondo de radiación gamma. Figura 3. Esquema del posicionamiento del detector cerca de la arteria (9) radial en el antebrazo (11) de un paciente. Se muestran 3 versiones: con 4 fibras centelleadoras (1) de sección cuadrada adyacentes y esencialmente paralelas entre sí (Fig. 3A) , con 1 fibra centelleadora (1) de sección circular (Fig. 3B) y con 2 fibras centelleadoras (1) de sección circular adyacentes y esencialmente paralelas entre sí, una de las cuales incluye blindaje (10) y se utiliza para la medida del fondo de radiación gamma (Fig.3C) . Figura 4. Esquema de la utilización de un emisor de luz, luz LED (12) , para ayudar en el correcto posicionamiento del detector sobre la arteria (9) de la cola de un ratón. REALIZACIÓN PREFERENTE DE LA INVENCIÓN La presente invención se ilustra mediante los siguientes ejemplos, que no pretenden er limitativos de su alcance. En la figura 1 se muestra un esquema del detector para la medida no invasiva de la función de entrada arterial que muestra una fibra centelleadora (1) acoplada a un SiPM (2) , una placa electrónica (3) , un sistema de digitalización de la señal (4) y un sistema de procesamiento de datos (5) . Ejemplo 1. Simulaciones Monte Cario. Los métodos Monte Cario permiten la simulación estadística de procesos físicos a partir del muestreo de las variables aleatorias que los caracterizan. Para ello, los métodos se basan en la continua generación de variables aleatorias mediante números aleatorios generados con algoritmos. En este ejemplo se utilizó el software PeneloPET (España, S. et al. Phys. Med. Biol. 54 (2009) 1723-1742; doi:10.1088/0031-9155/54/6/021) , que es un código Monte Cario especializado en simular la propagación de electrones, positrones y rayos gamma para estudiar la eficiencia y otras propiedades de escáneres PET. Ejemplo 1.1. Validación del software Para verificar el correcto funcionamiento del programa, se comprobó que la emisión de positrones de la fuente de 18F simulada presentaba un branching-ratio, espectro de emisión y rango en agua compatibles con los datos disponibles en el estado de la técnica. Con este fin, se simularon 5041 decaimientos en una fuente cilindrica de 18F dentro de un cilindro de agua y se comprobó que un 96, 88% de los decaimientos habían generado positrones, siendo este porcentaje muy similar al branching-ratio tabulado 96, 86% (http://nucleardata.nuclear.lu.se/toi/nuclide.asp?iZA=90018) . Así mismo se ha comprobado que la distribución del rango del positrón se corresponde con los resultados conocidos en el estado de la técnica obteniendo un rango medio y máximo en agua para el 18F de 0.5 y 2.1 mm, respectivamente (J. Cal-Gonzalez, J.L. Herraiz, S. España, P.M.G Corzo, J.J. Vaquero, M. Deseo, & J.M. Udias. Positrón range estimationswith PeneloPET. Phys. Med. Biol., volume 58, number 15) . Ejemplo 1.2. Viabilidad de medidas en ratón. Se utilizó el software PeneloPET para determinar de forma teórica la viabilidad de edidas en arteria (9) de cola de ratón. Para ello se estimó su eficiencia de detección para la radiación emitida desde la arteria (9) y el efecto de posibles contaminaciones procedentes de venas (7) y del cuerpo del ratón en la medida. Se estudió la eficiencia de detección de una fibra centelleadora (1) de 1 mm de diámetro situada de forma esencialmente rectilínea junto la arteria (9) de la cola de un ratón que contenía una concentración de 1 MBq/ml de 18F o 68Ga. Adicionalmente, se simuló el efecto de fuentes externas de radiación calculando la eficiencia de detección de la fibra centelleadora (1) para la radiación proveniente de las venas (7) de la cola y el cuerpo del ratón. En la figura 2 se muestran una sección transversal (6) de la cola del ratón y el detector de la invención. La cola del ratón se simuló como un cilindro de agua de 3, 2 mm de diámetro, en su interior se añadió un cilindro de 1 mm que simula el hueso (8) de la cola y, dentro de la cola, se añadieron cuatro cilindros adicionales que se corresponden con los vasos sanguíneos. El diámetro de la arteria (9) simulada es de 100 mieras y el de cada una de las venas (7) , de 200 mieras. De este modo se obtuvo una eficiencia de detección de un 16-18% para el 18F y de un 18-22% para el 68Ga, que se justifica por el mayor rango de los positrones emitidos por el galio. Teniendo en cuenta las simulaciones de fondo, se calculó la actividad mínima detectable para medidas de 1 segundo, obteniendo valores de 90 kBq/mL y 40 kBq/mL para el 18F y 68Ga, respectivamente. Estos valores están muy por debajo de las concentraciones iniciales de radiotrazador en sangre en estudios PET con ratones, que suelen oscilar entre los 500 y los 1000 kBq/mL. Por consiguiente, concluimos que el dispositivo detector es viable para la medición de la función de entrada arterial en ratones. Ejemplo 2.1. Dispositivo detector Se realizaron varios ensayos con una fibra centelleadora (1) utilizando distintos modelos: SCFSF-81J, SCSF-78J RD, SCSF-78 MJ y SCSF-78J SQ de la marca Kuraray de 1 mm de diámetro y un revestimiento de 0, 02 mm. El material de centelleo utilizado fue el poliestireno (PS) y el de revestimiento, el polimetacrilato de metilo (PMMA) . La longitud de la fibra era de 5 cm. Como fotodetectores se utilizaron SiPMs (2) , concretamente se probaron los modelos ASD-NUV4S-P y ASD-RGB4S-P de 4x4 mm2 de área sensible y los modelos ASD-NUV1S-P y ASD-RGB1S-P de 1 x 1 mm2 de área sensible de AdvanSiD. El acoplamiento entre la fibra centelleadora (1) y el SiPM (2) se realizó mediante grasa óptica BC-630 de Saint Gobain. Se utilizó una lámina de Tediar® (que es un fluoropolímero) para aislar ópticamente la fibra centelleadora (1) del exterior. Como sustento mecánico del dispositivo detector se dispuso de una carcasa de plástico construida mediante impresión 3D. Para la amplificación y conformación de los pulsos electrónicos se utilizó la placa electrónica (3) ASD-EP-EB-PZ, de AdvanSiD. Los pulsos eléctricos generados por la radiación detectada se registraron mediante un sistema de digitalización de la señal (4) que, en estos ejemplos, fue un osciloscopio digital del modelo PicoScope 3403D, de cuatro canales y un ancho de banda de 50 MHz. La adquisición de datos se controló desde un ordenador, como sistema de procesamiento de datos (5) , utilizando un software que gestiona y procesa los datos medidos con el osciloscopio. Para comprobar el correcto funcionamiento del detector se situó una fuente puntual de 22Na y 10 Ci de actividad a 1 mm de distancia de la fibra centelleadora (1) . En la tabla 1 se muestran las tasas de eventos medidos con la fibra centelleadora (1) SCFSF-81J acoplada, en ensayos independientes, a cada uno de los SiPMs (2) mencionados en este ejemplo. Así mismo, se muestran los resultados obtenidos utilizando el SiPM ASD-NUV4S-P acoplado a las distintas fibras centelleadoras (1) mencionadas en este ejemplo. De todas la pruebas realizadas, la que ofrece mejores resultados es la prueba en la que utilizamos el SiPM (2) ASD-NUV4S-P de 4x4 mm2 de área sensible y la fibra centelleadora (1) SCSF-78J SQ con sección de forma cuadrada de 1x1 mm2. Tabla 1 Ejemplo 2.2. Versión 1 del dispositivo detector Se realizaron dispositivos detectores como los descritos en el ejemplo 2.1 y se añadió na segunda fibra centelleadora (1) conectada a un segundo SiPM (2) . En cada detector, ambas fibras tenían 7 cm de longitud y se dispusieron contiguas y paralelas entre sí a una distancia 3 mm. Una de las fibras se blindó de la radiación beta rodeándola con un cilindro de cobre de 500m de grosor que constituyó el blindaje (10) (Figuras 2 y 3C) . Ejemplo 2.3. Versión 2 del dispositivo detector En el caso de aplicación en humanos, el tamaño del vaso sanguíneo y la distancia entre la fibra centelleadora (1) y el vaso está en torno a los 2 mm de diámetro y 2 mm de profundidad, respectivamente, lo cual es mucho más que para ratones. Por tanto, en humanos podemos utilizar fibras centelleadoras (1) de mayor tamaño transversal. Como ejemplo hemos simulado distinto número de fibras centelleadoras de sección cuadrada situadas a 2 mm de la superficie de un vaso de 2 mm de diámetro en el que se sitúa una distribución uniforme de radiofármaco marcado con Ga-68. Se han simulado entre 1 y 4 fibras centelleadoras de 1x1 mm2 de sección y 5 cm de longitud, dispuestas de manera contigua y en un único plano (figura 3A) y de forma esencialmente rectilínea. Las simulaciones nos permiten concluir que un número mayor de fibras da lugar a una mayor sensibilidad de detección obteniendo valores de 1, 6, 2, 7, 3, 7 y 4, 4 % para 1, 2, 3 y 4 fibras centelleadoras (ver figura 3) . Todas las fibras centelleadoras (1) pueden acoplarse a un solo SiPM (2) lo que permite simplificar la electrónica de lectura. Para validar experimentalmente estas medidas se implementaron 3 detectores con 1, 2 y 4 fibras SCSF-78J SQ con 7cm de longitud acopladas a un SiPM ASD-RGB4S-P. Se situó una fuente puntual de Na-22 a 2 mm de las fibras registrando 2179, 3412 y 8837 cuentas por segundo para los detectores de 1, 2 y 4 fibras respectivamente. Basándonos en los detectores descritos más arriba en este mismo ejemplo, realizamos un detector en el que se incluyó una fibra centelleadora (1) con blindaje (10) para la medida de fondo por cada una de las fibras centelleadoras (1) de la parte detectora de partículas beta, cada fibra centelleadora (1) se acopló a un SiPM (2) distinto para su lectura de manera independiente y el blindaje (10) se consiguió rodeando la fibra centelleadora (1) con un material que impide la llegada de partículas beta. En este ejemplo, el detector incluyó una fibra SCSF-78J SQ con 7cm de longitud acoplada a un SiPM ASD-RGB4S-P. La fibra centelleadora (1) se introdujo dentro de un cilindro ueco de cobre con 1.5 mm de grosor y 7 cm de longitud como blindaje (10) . Con este detector, se realizaron medidas utilizando una fuente de Na-22 situada a 2 mm del detector, obteniendo una tasa de eventos de 287. Como control, para frenar todos los positrones antes de que alcancen el detector, se intercaló una lámina de aluminio de 2 mm de grosor entre la fuente y el detector, obteniendo en este caso una tasa de eventos de 284. Por tanto, se comprobó que el detector detecta en ambos casos únicamente fotones gamma que emite la fuente y el blindaje (10) de cobre funciona correctamente. Ejemplo 2.4 Se elaboró un nuevo dispositivo detector en el que se incluyó un sistema de apoyo para el posicionamiento del propio dispositivo detector de manera que la fibra centelleadora (1) esencialmente rectilínea esté situada lo más próxima posible al vaso sanguíneo del que se desea medir la concentración de radiofármaco. Para conseguir esto, se incluyó una luz LED que podía seleccionarse entre el color naranja, el infrarrojo y el rojo dispuesta de tal manera que incidiera sobre la piel del sujeto, facilitando la identificación visual de los vasos sanguíneos. Es conocido que la luz reflejada por la sangre venosa, la sangre arterial y otros tejidos difiere, lo que ayuda a localizar el vaso que se desea monitorizar. Se elaboraron detectores como los descritos en los ejemplos 2.2 y 2.3, para su utilización en animales que, a continuación de la fibra centelleadora (1) incluían LED de color rojo con los que se ilumina la región de la cola donde se inyecta el radiotrazador y que permiten localizar con facilidad los vasos sanguíneos tanto para el posicionamiento del detector como para la inyección (figura 4) .
Publicaciones:
ES2957299 (16/01/2024) - A1 Solicitud de patente con informe sobre el estado de la técnica
Eventos:
En fecha 28/06/2023 se realizó Registro Instancia de Solicitud
En fecha 29/06/2023 se realizó Admisión a Trámite
En fecha 29/06/2023 se realizó Aceptación Tramitación CAP
En fecha 29/06/2023 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 06/07/2023 se realizó Superado examen de oficio
En fecha 16/10/2023 se realizó Registro Documentación no Identificada
En fecha 16/10/2023 se realizó 3406X_Solicitud Correcciones
En fecha 14/11/2023 se realizó 1550X_Notificación Rechazo Correcciones
En fecha 20/11/2023 se realizó Publicación Rechazo Correcciones
En fecha 25/12/2023 se realizó Realizado IET
En fecha 08/01/2024 se realizó 1109P_Comunicación Traslado del IET
En fecha 16/01/2024 se realizó Publicación Solicitud
En fecha 16/01/2024 se realizó Publicación Folleto Solicitud con IET (A1)
Pagos:
20/06/2023 - Pago Tasas IET
20/06/2023 - Pago Tasas IET
Fuente de la información
Parte de la información aquí publicada es pública puesto que ha sido obtenida de la Oficina de Propiedad Industrial de los diferentes países el 28/04/2024 y por lo tanto puede ser que la información no esté actualizada.Parte de la información aquí mostrada ha sido calculada por nuestro sistema informático y puede no ser veraz.
Privacidad
Si considera que al información aquí publicada afecta a su privacidad y desea que eliminemos la información aquí publicada envíe un email a info@patentes-y-marcas.com o rellene el formulario que encontrará aquí.Información sobre el registro de patente nacional por DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541
El registro de patente nacional por DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541 fue solicitada el 28/06/2023. Se trata de un registro en España por lo que este registro no ofrece protección en el resto de países. El registro DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541 fue solicitada por UNIVERSIDAD COMPLUTENSE DE MADRID. El registro [modality] por DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541 está clasificado como G01T 1/20,G01T 1/161,A61B 6/00 según la clasificación internacional de patentes.
Otras invenciones solicitadas en la clasificación internacional de patentes G01T 1/20,G01T 1/161,A61B 6/00.
Es posible conocer invenciones similares al campo de la técnica se refiere. El registro de patente nacional por DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541 está clasificado con la clasificación G01T 1/20,G01T 1/161,A61B 6/00 por lo que si se desea conocer más registros con la clasificación G01T 1/20,G01T 1/161,A61B 6/00 clicar aquí.Patentes en España
Es posible conocer todas las invenciones publicadas en España entre las que se encuentra el registro patente nacional por DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL. Nuestro portal www.patentes-y-marcas.com ofrece acceso a las publicaciones de patentes en España. Conocer las patentes registradas en un país es importante para saber las posibilidades de fabricar, vender o explotar una invención en España.Patentes registradas en la clase G
Es posible conocer todas las patentes registradas en la clase G (FISICA) entre las que se encuentra la patente DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase G01
Es posible conocer todas las patentes registradas en la clase G01 (METROLOGIA; ENSAYOS) entre las que se encuentra la patente DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase G01T
Es posible conocer todas las patentes registradas en la clase G01T (MEDIDA DE RADIACIONES NUCLEARES O DE RAYOS X ) entre las que se encuentra la patente DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A
Es posible conocer todas las patentes registradas en la clase A (NECESIDADES CORRIENTES DE LA VIDA) entre las que se encuentra la patente DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61
Es posible conocer todas las patentes registradas en la clase A61 (CIENCIAS MEDICAS O VETERINARIAS; HIGIENE) entre las que se encuentra la patente DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61B
Es posible conocer todas las patentes registradas en la clase A61B (DIAGNOSTICO; CIRUGIA; IDENTIFICACION) entre las que se encuentra la patente DETECTOR PARA LA MEDIDA NO INVASIVA DE LA FUNCIÓN DE ENTRADA ARTERIAL con el número P202330541. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.
¿Tienes alguna duda?
Escribe tu consulta y te responderemos rápida y gratuitamente.


 P202330519
P202330519