- Home /
- Publicaciones de patentes /
- Recubrimientos antimicrobianos
Recubrimientos antimicrobianos
Patente nacional por "Recubrimientos antimicrobianos"
Este registro ha sido solicitado por
Persona física
a través del representanteJORGE ISERN JARA
Contacto
- Estado: Vigente
- País:
- España
- Fecha solicitud:
- 14/07/2023
- Número solicitud:
-
P202330594
- Número publicación:
-
ES2956957
- Fecha de concesión:
-
- Inventores:
-
Persona física
- Datos del titular:
-
Persona física
- Datos del representante:
-
Jorge Isern Jara
- Clasificación Internacional de Patentes:
- C09D 183/08,A01N 25/34,A01N 25/10,C08G 77/38,C08G 85/00,C23C 18/12,C23C 22/83,A61L 29/08,A61L 31/08
- Clasificación Internacional de Patentes de la publicación:
- C09D 183/08,A01N 25/34,A01N 25/10,C08G 77/38,C08G 85/00,C23C 18/12,C23C 22/83,A61L 29/08,A61L 31/08
- Fecha de vencimiento:
Quiero registrar una patente
Reivindicaciones:
+ ES-2956957_A11. Un recubrimiento antimicrobiano que comprende una capa de sílice y moléculas bioactivas funcionalizadas con una molécula de enlace, donde las moléculas bioactivas funcionalizadas están unidas a la superficie de la sílice mediante enlaces covalentes. 2. El recubrimiento antimicrobiano de acuerdo a la reivindicación anterior, donde la moléculas bioactiva se selecciona del grupo de componentes de aceites esenciales (CAE) , ácidos orgánicos polímeros naturales, bacteriocinas, enzimas, preferiblemente la molécula bioactiva es un aceite esencial, más preferiblemente la molécula bioactiva es un componente de aceite esencial (CAE) seleccionado del grupo constituido por carvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. 3. El recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones anteriores, donde la molécula de enlace es un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano, clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato, más preferiblemente la molécula de enlace es 3-aminopropil trietoxisilano. 4. El recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones anteriores, aplicado al menos parcialmente sobre un sustrato seleccionado del siguiente grupo: metales, polímeros, materiales cerámicos y/o vidrio. 5. El recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones anteriores, donde las moléculas bioactivas funcionalizadas están unidas a la sílice mediante enlaces covalentes silicio-oxigeno-silicio (Si-O-Si) . 6. Proceso para depositar un recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones 1 a 5 en sustratos que comprende las siguientes etapas: a) proporcionar un sustrato; b) activación de la superficie del sustrato mediante el tratamiento del sustrato con una solución activadora; c) deposición de una capa de sílice en la superficie del sustrato mediante la polimerización de precursores de sílice en medio alcalino; d) funcionalización de las moléculas bioactivas mediante su reacción con la molécula de enlace en fase liquida; e) inmovilización covalente de las moléculas bioactivas funcionalizadas obtenidas en la etapa d) sobre la capa de sílice generada en la etapa c) mediante la deposición de una solución que comprende las moléculas bioactivas funcionalizadas; y f) secado de la superficie. 7. El proceso de acuerdo a la reivindicación 6, donde la deposición de la capa de sílice de la etapa c) se produce mediante la generación in situ de sílice a partir de un precursor seleccionado del grupo de ortosilicato de tetrametilo (TMOS) , ortosilicato de tetraetilo (TEOS) , metiltrimetoxisilano (MTMS) , feniltrimetoxisilano (PTMS) , dimetildimetoxisilano (DMDMS) y metacriloxipropiltrimetoxisilano (MPTMS) , más preferiblemente a partir de ortosilicato de tetraetilo (TEOS) . 8. El proceso de acuerdo a las reivindicaciones 6 a 7, donde la molécula bioactiva se selecciona del grupo de componentes de aceites esenciales, ácidos orgánicos polímeros naturales, bacteriocinas, enzimas, preferiblemente la molécula bioactiva es un aceite esencial, más preferiblemente la molécula bioactiva es un componente de aceite esencial seleccionado del grupo constituido por carvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. 9. El proceso de acuerdo a las reivindicaciones 6 a 8, donde la molécula de enlace empleada en la etapa d) es un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano, clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato, más preferiblemente la molécula de enlace es 3-aminopropil trietoxisilano. 10. Un elemento o superficie que comprende al menos parcialmente un recubrimiento antimicrobiano de acuerdo a cualquier de las reivindicaciones anteriores 1 a 5 o un recubrimiento preparado de acuerdo a la reivindicación 6 a 9. 11. El uso de un recubrimiento antimicrobiano de acuerdo a las reivindicaciones 1 a 5, un recubrimiento antimicrobiano preparado de acuerdo a la reivindicación 6 a 9 o de un elemento o superficie de acuerdo a la reivindicación 10 en la prevención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo.
Los productos y servicios protegidos por este registro son:
C09D 183/08 - A01N 25/34 - A01N 25/10 - C08G 77/38 - C08G 85/00 - C23C 18/12 - C23C 22/83 - A61L 29/08 - A61L 31/08
Descripciones:
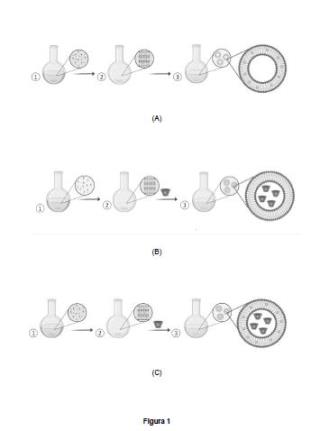
+ ES-2956957_A1 Recubrimientos antimicrobianos Campo Técnico La presente invención se refiere a un recubrimiento antimicrobiano, a su proceso de preparación y su uso en la prevención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo. Antecedentes de la Invención Las infecciones nosocomiales constituyen uno de los problemas más importantes que se presentan en el sistema de salud, siendo una de las principales causas de mortalidad y aumento de la morbilidad en los pacientes hospitalizados. Una de las principales razones de estas infecciones es la capacidad microbiana de adherirse a superficies sólidas (bióticas o abióticas) . Esta capacidad provoca la formación de estructuras poliméricas denominadas biopelículas. La función de las biopelículas es actuar como una trampa para los nutrientes y como una barrera física que impide la penetración y difusión de antibióticos y desinfectantes comunes. La formación de biopelículas comienza con la adhesión de células planctónicas individuales a una superficie. Estas células adherentes se convierten en micro colonias que luego proliferan en biopelículas maduras. Las biopelículas maduras producen componentes de matriz extracelular (ECM) que son críticos para mantener las estructuras distintivas de los agregados celulares. Una estrategia efectiva para prevenir la formación de biopelículas en superficies bióticas y abióticas es depositar una capa antimicrobiana en la superficie del material. Existen varios estudios basados en la inmovilización o liberación de sustancias antimicrobianas sobre diferentes superficies, sin embargo, dependiendo de la aplicación, no son completamente exitosos debido a su limitada eficacia o toxicidad. La inmovilización o liberación de sustancias antimicrobianas, como derivados de metales, sales de poliamonio y antibióticos, ha mostrado resultados alentadores. Aun así, su uso puede estar asociado con efectos secundarios como citotoxicidad, hipersensibilidad y espuestas inflamatorias. Además, el uso indiscriminado de estas sustancias ha generado un problema mayor, que es la resistencia antimicrobiana. La resistencia a los antimicrobianos (RAM) ocurre cuando las bacterias, los virus, los hongos y/o los parásitos cambian con el tiempo y ya no responden a los medicamentos, lo que hace que las infecciones sean más difíciles de tratar y aumenta el riesgo de propagación de enfermedades, enfermedades graves y muerte. Como resultado de la resistencia a los medicamentos, los antibióticos y otros medicamentos antimicrobianos se vuelven ineficaces y las infecciones se vuelven cada vez más difíciles o imposibles de tratar. Se han empleado varios enfoques en la búsqueda de superficies antimicrobianas efectivas, incluida la resistencia a la adhesión, la destrucción por contacto y la lixiviación de biocidas. Entre estos enfoques, la muerte bacteriana por contacto parece ser la ruta más prometedora; este enfoque implica modificaciones químicas o físicas para unir un agente antimicrobiano a la superficie. Entre las estrategias más comúnmente aplicadas para la modificación de superficies se encuentran la adsorción (a través de interacciones electrostáticas) , el acoplamiento ligando-receptor y la unión covalente (Vasilev K, Cook J, Griesser HJ. Antibacterial surfaces for biomedical devices. Expert Rev Med Devices. 2009;6 (5) :553-567) . La unión covalente ofrece varias ventajas al proporcionar los enlaces más estables entre el compuesto bioactivo y la superficie. Algunos estudios han reportado la inmovilización sobre superficies de acero inoxidable u otras superficies (plástico, titanio y otras) de ciertas moléculas bioactivas como péptidos antibacterianos como magainina, nisina y lisozima o la inmovilización de biopolímeros como el quitosano. Algunas de las estrategias desarrolladas recientemente se describen a continuación. La solicitud de patente española EP3326971A1, "Sistema antimicrobiano", divulga la funcionalización de antimicrobianos naturales con grupos trialcoxisilano sobre la superficie de un soporte mesoporoso de sílice. El artículo "Antibacterial isoeugenol coating on stainless Steel and polyethylene surfaces prevenís biofilm growth" (Nielsen, C. K., et al. "Antibacterial isoeugenol coating on stainless Steel and polyethylene surfaces prevenís biofilm growth". Journal of applied microbiology 124.1 (2018) : 179-187) divulga recubrimientos de superficies de acero inoxidable y de polietileno con eugenol, para evitar el crecimiento de biofilms. El documento "Enhanced antimicrobial activity of essential oil components immobilized on silica partióles" (Ruiz-Rico, María, et al. "Enhanced antimicrobial activity of essential oil components immobilized on silica partióles." Food chemistr y 233 (2017) : 228-236.) divulga la inmovilización de aceites esenciales mediante 3-aminopropil trietoxisilano, sobre tres soportes distintos de silicio. El documento "Métodos y soportes para la inmovilización de componentes de aceites esenciales y su efecto sobre la actividad antimicrobiana y antioxidante" (Cebrián Cabo, Santiago. "Métodos y soportes para la inmovilización de componentes de aceites esenciales y su efecto sobre la actividad antimicrobiana y antioxidante." (2020) ) describe la inmovilización de componentes de aceites esenciales en nanopartículas de sílice. La solicitud de patente internacional WO2021107870A1 divulga un polímero antimicrobiano y la preparación de recubrimientos de superficies para aplicaciones antimicrobianas. No obstante, las estrategias descritas en estado de la técnica presentan varios inconvenientes tales como la poca robustez de la unión con la molécula bioactiva que eventualmente resulta en una baja actividad microbiana y potencial de reutilización de la superficie bajo. Además, los sistemas descritos no son fácilmente aplicables a distintas superficies, por ejemplo, paredes o encimeras, y/o elementos, por ejemplo, material quirúrgico o prótesis. La presente invención proporciona una solución a ese problema. Sumario de la invención En un primer aspecto, la invención se refiere a un recubrimiento antimicrobiano que comprende una capa de sílice y moléculas bioactivas funcionalizadas con una molécula de enlace, donde las moléculas bioactivas funcionalizadas están inmovilizadas covalentemente a la superficie de la sílice mediante enlaces covalentes. En un segundo aspecto, la invención se refiere a un proceso para depositar un recubrimiento antimicrobiano de acuerdo al primer aspecto de la invención que comprende las siguientes etapas: a) proporcionar un sustrato, b) activación de la superficie del sustrato mediante el tratamiento del sustrato con una solución de ácido sulfúrico y peróxido de hidrogeno. c) deposición de una capa de sílice en la superficie del sustrato mediante la polimerización de precursores de sílice en medio alcalino, d) funcionalización de las moléculas bioactivas mediante su reacción con la molécula de enlace en fase liquida, e) inmovilización covalente de las moléculas bioactivas funcionalizadas obtenidas en la etapa d) sobre la capa de sílice generada en la etapa c) mediante la deposición de una solución alcohólica que comprende las moléculas bioactivas funcionalizadas, y f) secado de la superficie a temperatura ambiente. En un tercer aspecto, la invención se refiere a un elemento, por ejemplo, herramientas quirúrgicas, o superficies, por ejemplo, paredes o suelos, que comprende al menos parcialmente un recubrimiento antimicrobiano de acuerdo al primer aspecto o un recubrimiento preparado de acuerdo al segundo aspecto de la invención. En un cuarto aspecto, la invención se refiere al uso de un recubrimiento antimicrobiano de acuerdo al primer aspecto, un recubrimiento antimicrobiano preparado de acuerdo al segundo aspecto o de un elemento o superficie de acuerdo al tercer aspecto de la invención en la prevención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo. Descripción de las figuras Figura 1. Comparativa de recuentos (UFC, %) de la bacteria S. epidermidis después del contacto con superficies funcionalizadas (SS-SiO2 -Van) y no funcionalizadas (SS, SS-OH y SS-SiO2) en función del tiempo. Figura 2. Robustez del efecto antimicrobiano de las superficies SS-SiO2-Van frente a S. epidermidis tras varios test sucesivos. Figura 3. Comparativa de recuentos (log CFU/ml, %) de la bacteria E. coli después del contacto con superficies funcionalizadas (PP-SiO2 -Van) y no funcionalizadas (PP, PP-OH y PP-SiO2) después de 24h. Figura 4. Capacidad inhibitoria para la formación de biopelículas de superficies SS-SiO2-Van frente a S. epidermidis después de 24h. Descripción detallada de la invención La presente invención proporciona un recubrimiento antimicrobiano que comprende una capa de sílice y moléculas bioactivas funcionalizadas con una molécula de enlace, donde las moléculas bioactivas funcionalizadas están inmovilizadas covalentemente a la superficie de la sílice mediante enlaces covalentes. El uso de recubrimientos antimicrobianos mejorados por una inmovilización covalente de una molécula antimicrobiana bioactiva en la superficie mediante una capa intermedia de sílice, supone una novedad en este campo técnico. En particular en lo que se refiere a la bacteria S. epidermidis, considerada una de las causas más frecuentes de infecciones nosocomiales y principal patógeno responsable de las infecciones crónicas asociadas al biopeliculas en tejidos como la piel, las vías respiratorias y los dispositivos médicos. El término "antimicrobiano" se refiere a un elemento que impide la formación o el desarrollo de los microorganismos. En particular, se refiere a un recubrimiento que previene el crecimiento microbiano, la formación de biopelículas, inhibe la adhesión microbiana y/o elimina las células microbianas adheridas al mismo. El término "molécula bioactiva" se refiere a moléculas que poseen actividad antimicrobiana, en particular antibacteriana, antifúngica y/o antiviral. El término "polímero (s) " en el contexto de esta solicitud significa oligómero (s) , polímero (s) y copolímero (s) , sus mezclas y principalmente también su formación de composites con base orgánica y/o sustancialmente orgánica. Habitualmente, el (los) "polímero (s) " en el contexto de esta solicitud se presenta (n) predominantemente o completamente en forma de polímero (s) y/o copolímero (s) . El término "funcionalizar" se refiere a la modificación de una superficie o molécula para incorporar ciertos elementos, por ejemplo, grupos funcionales o moléculas, que doten dicha superficie de propiedades fisicoquímicas particulares. El término "activar" se refiere a la capacidad, en un paso procedimental posterior, por ejemplo, una etapa de inmersión, de una solución y/o una dispersión acuosa, cerca de la superficie del sustrato, de generar grupos hidroxilo. En el procedimiento de acuerdo con la invención se crea de esta manera una condición de que puede formarse una capa secuencial sobre el sustrato. El término "inmovilización covalente" se refiere a la unión mediante un enlace covalente. En particular se refiere a la unión entre sustrato y sílice y a la unión sílice y molécula bioactiva mediante enlaces covalentes. Más específicamente, la presente invención se basa en la mejora y superación de los inconvenientes y desventajas que presentan los métodos ya conocidos. La invención se representa esquemáticamente en la Fig. 1, particularmente en el panel B, donde puede apreciarse el efecto del recubrimiento antimicrobiano (en este caso, S. epidermidis) , que comprende una capa de sílice funcionalizada con moléculas bioactivas (en este caso, Vainillina) . Este recubrimiento antimicrobiano puede actuar frente a los microorganismos que se desee, ya sean bacterias, virus o también hongos microscópicos, levaduras o protozoos. Así, el recubrimiento testado en S. epidermidis constituye un modelo para otros microorganismos. El recubrimiento del primer aspecto se une de manera covalente a la superficie del sustrato (S) mediante enlaces S-O-Si entre el sustrato y la capa de sílice. La unión covalente entre sustrato y recubrimiento mediante una capa de sílice dota el recubrimiento de gran robustez y permite que las moléculas bioactivas se mantengan ancladas en el sustrato durante un periodo prolongado de tiempo y por tanto se mantenga la eficacia antimicrobiana de la superficie recubierta. Los sustratos que pueden ser recubiertos por los recubrimientos de la invención son muy variados, como, por ejemplo, metales, polímeros, materiales cerámicos y/o vidrio. Los metales adecuados incluyen, entre otros, titanio, cobre, oro, estaño, níquel, aluminio, ierro, cobalto, plata, platino, magnesio, manganeso, zinc y aleaciones de metales como aceros, bronce o latón. En el grupo de los polímeros se incluyen polímeros convencionales, como, por ejemplo, cloruro de polivinilo (PVC) , ácido de polivinilo (PVA) , polietileno (PE) , poliestireno (PS) , polipropileno (PP) , policarbonato (PC) , tereftalato de polietileno (PET) , poliamida (PA) , poliuretano (PU) , estireno, butadieno, acrilonitrilo (ABS) , o polímeros biodegradables, como, por ejemplo, ácido poli láctico (PLA) , colágeno, biogomas, o celulosa. Los materiales cerámicos de interés incluyen, a modo de ejemplo, TiO2 , Al2O3 , materiales tipo cermet, por ejemplo, WC-Co o WC-Co-Cr, o materiales bi-componente como pueden ser TiO2 + NiAl. Los recubrimientos de la invención pueden recubrir la superficie del sustrato de manera total o parcial según sea necesario. En dichos recubrimientos antimicrobianos, se prefiere que las moléculas bioactivas se seleccionen del grupo de componentes de aceites esenciales (CAE) , ácidos orgánicos, polímeros naturales, bacteriocinas, y/o enzimas. En una realización preferida, la molécula bioactiva es un componente de aceite esencial. En la realización más preferida la molécula bioactiva se selecciona del grupo de componentes de aceites esenciales siguiente: carvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. En la realización aún más preferida la molécula bioactiva es vainillina. La actividad antimicrobiana de los CAE no se atribuye a un único mecanismo, sino que es una cascada de reacciones (degradación de la pared celular, daño de la membrana citoplásmica, daño de la proteína de la membrana, coagulación del citoplasma y agotamiento del poder de los protones) que da como resultado la destrucción de las células de los microorganismos. Además, los CAE pueden penetrar en biopelículas formadas y matar los microorganismos protegidos. En los recubrimientos de la invención, la molécula bioactiva se encuentra presente en un rango de concentraciones de 0, 5 a 1, 5 mg/cm2, preferiblemente en un rango de 0, 8 a 1, 05 mg/cm2. La molécula bioactiva en estos rangos de concentración asegura se produzca el efecto antimicrobiano deseado. En lo que se refiere a la molécula espadadora, se prefiere que la molécula de enlace sea un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano (APTES) , clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato, más preferiblemente la molécula de enlace es 3-aminopropil trietoxisilano (APTES) . En la realización preferida del primer aspecto las moléculas bioactivas funcionalizadas están unidas a la sílice mediante enlaces covalentes silicio-oxigeno-silicio (Si-O-Si) . Este enlace covalente Si-O-Si entre molécula bioactiva y sílice asegura una unión fuerte y duradera, de manera que el recubrimiento es resistente al paso del tiempo y a múltiples lavados, manteniendo su actividad antimicrobiana. En su segundo aspecto, la invención se refiere a un proceso para depositar un recubrimiento antimicrobiano de acuerdo al primer aspecto en sustratos que comprende las siguientes etapas: a) proporcionar un sustrato; b) activación de la superficie del sustrato mediante el tratamiento del sustrato con una solución activadora; c) deposición de una capa de sílice en la superficie del sustrato mediante la polimerización de precursores de sílice en medio alcalino; d) funcionalización de las moléculas bioactivas mediante su reacción con la molécula de enlace en fase liquida; e) inmovilización covalente de las moléculas bioactivas funcionalizadas obtenidas en la etapa d) sobre la capa de sílice generada en la etapa c) mediante la aplicación de una solución que comprende la molécula bioactiva funcionalizadas, y, f) secado de la superficie. En una realización preferida del segundo aspecto, los sustratos que pueden ser recubiertos por la invención son muy variados, como, por ejemplo, metales, polímeros, materiales cerámicos y/o vidrio. Los metales adecuados incluyen, entre otros, titanio, cobre, oro, estaño, níquel, aluminio, hierro, cobalto, plata, platino, magnesio, manganeso, zinc y aleaciones de metales como aceros, bronce o latón. En el grupo de los polímeros se incluyen, entre otros, cloruro de polivinilo (PVC) , ácido de polivinilo (PVA) , polietileno (PE) , poliestireno (PS) , polipropileno (PP) , policarbonato (PC) , tereftalato de polietileno (PET) , oliamida (PA) , poliuretano (PU) , estireno, butadieno, acrilonitrilo (ABS) , ácido poli láctico (PLA) , colágeno, biogoma, o celulosa. Los materiales cerámicos de interés incluyen, a modo de ejemplo, TiO2 , Al2O3 , materiales tipo cermet, por ejemplo, WC-Co o WC-C0-Cr, o materiales bi-componente como pueden ser T¡O2 + NiAl. En la realización del segundo aspecto, la solución activadora de la etapa b) es una solución ácida y/u oxidante. En una realización preferida del segundo aspecto, la superficie del sustrato se activa mediante una solución activadora que consiste en una solución acuosa de ácido sulfúrico, ácido nítrico, persulfato de potasio, peróxido de oxígeno o una mezcla de los mismos. La activación de la superficie se lleva a cabo durante menos de 15 min, preferiblemente 10 min. El contacto entre la solución acuosa y la superficie del sustrato debe ser corta para evitar los efectos corrosivos de la misma y a la vez generar suficientes grupos hidroxilos en la superficie del sustrato. En una realización preferida del segundo aspecto, la deposición de la capa de sílice de la etapa c) se produce mediante la generación in situ de sílice a partir de un precursor seleccionado del grupo de ortosilicato de tetrametilo (TMOS) , ortosilicato de tetraetilo (TEOS) , metiltrimetoxisilano (MTMS) , feniltrimetoxisilano (PTMS) , dimetildimetoxisilano (DMDMS) y metacriloxipropiltrimetoxisilano (MPTMS) . La opción más preferida de precursor es el ortosilicato de tetraetilo (TEOS) . En una realización preferida del segundo aspecto, la molécula bioactiva se selecciona del grupo de aceites esenciales, ácidos orgánicos polímeros naturales, bacteriocinas, enzimas, preferiblemente la molécula bioactiva es un aceite esencial. En una realización más preferida la molécula bioactiva es un componente de aceite esencial. En una realización aún más preferida la molécula bioactiva se selecciona del grupo de componentes de aceites esenciales (CAE) constituido porcarvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. En la realización más preferida la molécula bioactiva es vainillina. En una realización preferida del segundo aspecto, la molécula de enlace empleada en la etapa d) es un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano, clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato. En la realización más preferida la molécula de enlace es 3-aminopropil trietoxisilano. En una realización preferida del segundo aspecto, la solución de la etapa e) que comprende la molécula bioactiva funcionalizada es una solución de pentano, ciclopentano, hexano, ciclohexano, benceno, tolueno, 1, 4-dioxano, cloroformo, éter dietílico, diclorometano (DCM) , tetrahidrofurano (THF) , acetona, dimetilformamida (DMF) , acetonitrilo (MeCN) , dimetilsulfóxido (DMSO) , ácido fórmico, n-butanol, alcohol isopropílico (IPA) , metanol, etanol, agua o sus mezclas. En una realización más preferida, la solución es una solución acuosa alcohólica, preferiblemente una solución de etanol y agua. En una realización preferente el secado de la etapa d) se produce a temperatura ambiente. En su tercer aspecto, la invención se refiere a un elemento o superficie que comprende al menos parcialmente un recubrimiento antimicrobiano de acuerdo al primer aspecto o un recubrimiento preparado de acuerdo al segundo aspecto de la invención. Los elementos o superficies que pueden comprender el recubrimiento de la invención pueden ser distintos materiales, en particular pueden ser de metal, polímeros, materiales cerámicos y/o vidrio. Los metales adecuados incluyen, entre otros, titanio, cobre, oro, estaño, níquel, aluminio, hierro, cobalto, plata, platino, magnesio, manganeso, zinc y aleaciones de metales como aceros, bronce o latón. En el grupo de los polímeros se incluyen, entre otros, cloruro de polivinilo (PVC) , ácido de polivinilo (PVA) , polietileno (PE) , poliestireno (PS) , polipropileno (PP) , policarbonato (PC) , tereftalato de polietileno (PET) , poliamida (PA) , poliuretano (PU) , estireno, butadieno, acrilonitrilo (ABS) , ácido poli láctico (PLA) , colágeno, biogoma, o celulosa. Los materiales cerámicos de interés incluyen, a modo de ejemplo, TiO2 , Al2O3 , materiales tipo cermet, por ejemplo, WC-Co o WC-C0-Cr, o materiales bi-componente como pueden ser T¡O2 + NiAl. Entre los elementos cuya superficie tendría mayor interés recubrir, pueden citarse: una mascarilla higiénica, un tejido, una tela, instrumental de uso clínico, una pared, un suelo, un mueble, un pasamanos, un dispositivo móvil, una pantalla táctil o un filtro de aire. En general, puede tener interés cualquier superficie de cualquier objeto presente en un lugar donde debe predominar la higiene y debe hacerse lo posible por mantenerla, pero donde, desgraciadamente, es habitual la presencia de distintos microorganismos. En su cuarto aspecto la invención se refiere a uso de un recubrimiento antimicrobiano de acuerdo al primer aspecto, un recubrimiento antimicrobiano preparado de acuerdo al segundo aspecto o de un elemento o superficie de acuerdo al tercer aspecto en la revención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo. El microorganismo puede ser una bacteria, pero también un virus, un hongo microscópico, levaduras o un protozoo. Se tiene preferencia por una bacteria. La invención se explicará ahora con mayor detalle mediante los Ejemplos y Figuras que aparecen a continuación. Ejemplos Ejemplo 1. Funcionalización de moléculas bioactivas Ejemplo 1.1. Funcionalización de moléculas bioactivas - vainillina Para funcionalizar la molécula bioactiva, en este caso la vainillina, primeramente, se suspendió 1 g de vainillina en 25 mL de diclorometano y luego se añadieron a la mezcla 1, 2 mL de 3-aminopropil trietoxisilano (APTES) . La relación molar entre los reactivos fue de 1:1 de vainillina:APTES (Esquema 1) . La mezcla se agitó durante 2 h, y después de esto, la suspensión se evaporó a presión reducida para obtener el correspondiente derivado de alcoxisilano, (E) -2-metoxi-4- ( ( (3-trietoxisilil) propil) imino) metil) fenol. En este primer paso, la reacción entre la vainillina y APTES da lugar al producto 3 en el que la vainillina se une al grupo etoxi por medio de un enlace imina (Esquema 1) . En un segundo paso, 5 mmol de derivado de alcoxisilano (producto 3) se solubilizaron en etanol y se añadieron 340 mg de Pd/C. Posteriormente, se pasó un flujo de gas N2 a través del matraz de reacción para desplazar el O2. Luego, se agregó flujo de H2. La mezcla se gitó durante 3 h en atmósfera inerte. Finalmente, el derivado reducido, 2-metoxi-4- ( ( (3- (trietoxisilil) propil) amino) metil) fenol (Van-APTES) , producto 4, se filtró y evaporó a presión reducida para obtener el compuesto puro como un sólido amarillo pálido. El enlace imina formado entre el grupo aldehido de vainillina y el grupo amina de APTES (3) se redujo para estabilizar la unión del grupo vainillina al grupo trialcoxisilano (4) , Van-APTES. La reacción de reducción del enlace imina se llevó a cabo mediante una hidrogenación química utilizando H2 y paladio sobre carbono (Pd/C) como catalizador (Esquema 2) . Ejemplo 1.2. Funcionalización de moléculas bioactivas - carvacrol, el eugenol y el timol Para funcionalizar otras moléculas bioactivas, en este caso carvacrol, el eugenol y el timol, primeramente, se transformaron en derivados de aldehido. En un segundo paso, los aldehidos de carvacrol, eugenol y timol reaccionaron con 3-aminopropiltrietoxisilano (APTES) para producir los derivados de alcoxisilano correspondientes. Los aldehidos del carvacrol y del timol se sintetizaron por formilación directa utilizando paraformaldehído. En una síntesis típica, se colocaron 150 ml de acetonitrilo, 40 mmol de carvacrol o timol, 150 mmol de trimetilamina y 40 mmol de MgSO4 anhidro dentro de un matraz de fondo redondo. La mezcla se colocó en una atmósfera de argón y se agitó durante 15 minutos a temperatura ambiente. Posteriormente, se añadieron 270 mmol de paraformaldehído y la mezcla de reacción se calentó a reflujo durante 3, 5 h a 83 °C. Luego se dejó enfriar la mezcla a temperatura ambiente. La solución se acidificó con una solución de HCl al 5% (320 mi) y se agitó durante 30 min en atmósfera inerte. Finalmente, la porción orgánica se xtrajo con éter dietílico y los disolventes se eliminaron a presión reducida para obtener el aldehido de carvacrol o del timol. El aldehido del eugenol se sintetizó mediante una reacción de Reimer-Tiemann. En una síntesis típica, 150 ml de agua se calentaron a 80 °C, en un matraz de fondo redondo, y 22 mmol de eugenol se disolvieron en el agua. El calor se redujo a 60 °C, luego se agregaron 400 mmol de KOH y 88 mmol de cloroformo. Como la reacción fue exotérmica, se añadió cloroformo a una velocidad de 1 ml/h durante un período de 7 horas por razones de seguridad. La mezcla de reacción se mantuvo a 60 °C durante un período adicional de 8 horas. Luego, la solución se acidificó con una solución de H2SO4 al 10%. La porción orgánica se extrajo con n-butanona y los disolventes se eliminaron a presión reducida. Para facilitar la inmovilización covalente de los componentes de aceites esenciales a la capa de sílice, se sintetizaron los correspondientes derivados de aceites esenciales. Para ello se hicieron reaccionar 2 mi de los aldehidos de carvacrol, timol o eugenol con 2, 3 mi (10 mmol) de (3-aminopropil) trietoxisilano (APTES) en presencia de diclorometano (20 mi) y MgSO4 , dando lugar a las correspondientes iminas, que posteriormente se reducen de la misma manera que lo descrito para Van-APTES en el ejemplo 1.1. La mezcla se calentó a reflujo durante 1 h, luego se filtró y se evaporó a presión reducida para obtener un líquido transparente. Ejemplo 2. Preparación del recubrimiento antimicrobiano A continuación, se describe la preparación de los recubrimientos de la invención. Ejemplo 2.1 Activación del sustrato - acero inoxidable (SS) El primer paso en la funcionalización de SS es la preparación de la superficie de acero inoxidable. Antes de depositar la capa de sílice, la superficie del material SS debe desengrasarse adecuadamente mediante ultrasonidos en varios solventes como etanol y acetona, y luego con agua. Para ese fin, se colocaron placas de acero inoxidable (placas SS) en un vaso de precipitados (1 placa en 1 vaso de precipitados) y se sonicaron durante 10 min en cada uno de los siguientes productos químicos en sucesión: acetona (70 % v/v) , etanol y agua desionizada. Después del procedimiento de lavado, la superficie SS debe tratarse químicamente con una solución ácida o alcalina para activar la superficie metálica y exponer los grupos hidroxilo de la superficie. Los grupos hidroxilo se forman por quimisorción disociativa de moléculas de agua y, en general, se considera que la hidratación y la hidroxilación se producen en los sitios de iones metálicos reticulares expuestos en la superficie. Esta activación es importante porque la cantidad de grupos hidroxilo obtenidos durante el proceso de activación influye fuertemente en el inicio de la unión del silano y, por lo tanto, en la formación de la película de sílice. Luego, para el procedimiento de activación, los materiales SS lavados se trataron con solución piraña y se obtuvieron los materiales SS-OH. La solución piraña correspondiente consistió en la adición de peróxido de hidrógeno en un vaso de precipitados, al cual se le añadió lentamente ácido sulfúrico concentrado, en una proporción de ácido sulfúrico a peróxido de hidrógeno de 7:3 (v/v) . A continuación, la mezcla resultante se agitó suavemente antes de su uso. Las placas SS limpias se sumergieron en la solución de piraña durante 10 min. Pasado este tiempo, las placas se retiraron y se colocaron en una segunda solución de piraña durante 5 min. Después del segundo tratamiento con piraña, las placas SS se enjuagaron dos veces en agua ultrapura antes de colocarlas en un baño de agua ultrapura durante 24 h. Las placas resultantes se denominarán SS-OH. Así, las superficies de SS y SS-OH, difieren únicamente en la presencia en las superficies SS-OH de los grupos hidroxilo generados. Los grupos hidroxilo son esenciales en la formación de fuertes enlaces covalentes con los grupos silanol de la sílice del recubrimiento. Ejemplo 2.2 Deposición de la capa de sílice sobre el soporte Las placas SS-OH se trataron con TEOS mediante un procedimiento sol-gel. Las placas de SS-OH se colocaron en una solución acuosa básica, se calentaron a 80 °C y luego se añadieron gota a gota 5 mL de TEOS y la mezcla se agitó durante treinta minutos. Las placas se enjuagaron dos veces en agua ultrapura y se secaron a 100 °C durante la noche. La hidrólisis del TEOS produce grupos silanol (Si-OH) en presencia de agua y facilita la rápida adsorción de las entidades de silicato en la superficie del SS- material OH a través e enlaces de hidrógeno, para condensar aún más y formar un enlace covalente metalsiloxano (Me-O-Si-OH) . Los grupos silanol facilitan la unión covalente de moléculas orgánicas a la superficie, lo que resulta en una funcionalización estable debido a su excelente estabilidad térmica, mecánica y química. Ejemplo 2.3 Funcionalización de la capa de sílice con las moléculas bioactivas - vainillina Para la funcionalización la superficie de SS-SiO2 , este material se puso en contacto con el derivado de vainillina (Van-APTES) previamente sintetizado formando así los materiales SS-SiO2-Van. La unión a las superficies se produce por hidrólisis de los grupos etoxi del derivado Van-APTES que conduce a la formación de silanoles. Los silanoles de Van-APTES se condensan con los silanoles de la superficie SS-Si02 y conducen a la formación de enlaces covalentes Si-O-Si. Se solubilizó 1 g de Van-APTES en etanol. La solución se vertió en las placas de SS-SiO2 y las placas se agitaron durante 5, 5 horas a temperatura ambiente. Luego, las placas se lavaron con etanol y se secaron a temperatura ambiente, dando lugar a las superficies SS-SiO2-Van Ejemplo 2.4 Activación del sustrato - polipropileno (PP) Enfocándonos en lo citado anteriormente, esta invención presenta también como ejemplo la inmovilización de un aceite esencial funcionalizado con un alcoxisilano (aminopropiltrietoxisilinao, APTES) , como pueda ser la molécula bioactiva antimicrobiana Vainillina, sobre una superficie, como puede ser por ejemplo el polipropileno (PP) . El primer paso en la funcionalización de PP es la preparación de la superficie de polipropileno. La superficie PP debe tratarse químicamente para exponer los grupos hidroxilo de la superficie. Para ello, se trató la superficie del plástico polipropileno (PP) con un agente oxidante (peroxidisulfato de potasio) para generar grupo hidroxilo (PP-OH) , importante para la funcionalización. El peroxidisulfato de potasio se utiliza como fuente de radicales en solución acuosa, es bien conocido como iniciador de la polimerización por radicales libres y como agente oxidante. Los grupos hidroxilo del PP se forman por la extracción de un hidrógeno (del carbono terciario presente en cada unidad de repetición del polímero) que conduce a la formación de un macroradical que posteriormente reacciona con un segundo radical hidroxilo, dando lugar a la introducción de grupos hidroxilo en la superficie del PP. Esta activación es importante porque la cantidad de grupos hidroxilo obtenidos durante el proceso de activación influye fuertemente en el inicio de la unión del silano y, por lo tanto, en la formación de la película de sílice. Los grupos hidroxilo son esenciales en la formación de fuertes enlaces covalentes con los grupos silanol de la sílice del recubrimiento. A continuación, se depositó un recubrimiento de capa de sílice e inmovilizó covalentemente con molécula bioactiva funcionalizada con APTES como los llevados a cabo en los procesos descritos en los ejemplos Ejemplo 2.2 y 2.3, dando lugar a las superficies PP-SiO2yfinalm ente PP-SiO2-Van. Ejemplo 3. Cuantificación de la funcionalización con las moléculas bioactivas - SS-SiO?-Van. Para cuantificar la funcionalización de la superficie SS-SiO2-Van, se realizó un ensayo colorimétrico de superficie. Para este propósito, se usó ninhidrina como agente de prueba colorimétrica. Generalmente, la ninhidrina se usa en ensayos colorimétricos para el reconocimiento de grupos amina, en estos ensayos se observa un cambio de color de amarillo a púrpura intenso solo en el caso de la presencia de grupos amino en la solución. El color púrpura intenso, conocido como violeta de Ruhemann, se produce cuando dos moléculas del compuesto ninhidrina (2, 2-dihidroxiindano-1, 3-diona) reaccionan con una amina primaria, una amina secundaria o un aminoácido. Considerando esto, el ensayo de ninhidrina se desarrolló sumergiendo placas de SS, SS-OH, SS-SiO2 y SS-SiO2-Van en la solución de ninhidrina y las placas se dejaron en contacto con la solución durante 10 min a 80 °C. Después de este tiempo, se observó que solo las placas de SS-SiO2 -Van se tornaron de color púrpura, lo que confirma el proceso de uncionalización de la vainillina en la superficie. Después de eso, las placas de SS-SiO2-Van se sumergieron en 5 mi de etanol y se sonicaron durante varias horas para separar el complejo Van-ninhidrina de la superficie. Cuando se liberó todo el color de las placas SS debido a la ninhidrina unida, se cuantificó el contenido de Van-ninhidrina del disolvente de etanol midiendo su absorbancia a 400 nm. Previamente se preparó una curva de calibración con el complejo Van-ninhidrina obtenido al hacer reaccionar la ninhidrina con el derivado Van-APTES en etanol (de 0, 9 a 10, 5 mg/mL) y se utilizó para la cuantificación. La misma metodología se realizó para las superficies desnudas y de control: placas SS (superficie desnuda) , placas SS-OH y SS-SiO2 (superficies de control) . El resultado obtenido fue de 0, 95 ±0, 1 mg/cm2 de funcionalización sobre cada superficie de acero SS-SiO2-Van. Para las placas de SS, SS-OH y SS-SiO2 el resultado obtenido fue de 0 mg/cm2. Ejemplo 4. Evaluación de la viabilidad microbiana - SS-SiOp-Van v PP-SiOp-Van. La actividad antimicrobiana de los recubrimientos de la invención, en particular los del ejemplo 2 (SS-SiO2-Van) , frente a los microrganismos se evaluó mediante ensayos in-vitro con S. epidermidis. La evaluación de la viabilidad microbiana se realizó en medio líquido, para permitir el contacto entre las bacterias y las superficies funcionalizadas y no funcionalizadas durante la incubación, seguido de placas para enumerar las unidades formadoras de colonias (UFC) viables restantes. Se compararon materiales recubiertos con el recubrimiento de la invención con materiales como el acero inoxidable (SS) , acero inoxidable activado (SS-OH) y acero inoxidable recubierto con sílice (SS-SiO2) , estos fueron considerados como controles negativos. La eficacia antimicrobiana se realizó en medio líquido, en solución de fosfato (PBS) . Se prepararon diluciones inoculadas con S. epidermidis en PBS para obtener una concentración de 104 células/mL. Un matraz que contenía las superficies SS-SiO2-Van funcionalizadas, se inoculó con 1 mL de suspensión de S. epidermidis para obtener una concentración final de 103 células/mL. Las placas de SS, SS-OH y SS-SiO2 se trataron siguiendo el mismo procedimiento que SS-SiO2-Van. Finalmente, todas las muestras se incubaron con agitación orbital (120 rpm) a 37 °C durante 24 h. Para contabilizar las células viables, se tomaron alícuotas de 100 l de cada suspensión de muestra (SS, SS-OH, SS-SiO2 y SS-SiC>2-Van) y se distribuyeron en placas de agar soja triptona (TSA, por sus siglas en inglés) . Después de la incubación de la placa a 37 °C durante 24 h, se contaron las colonias y los resultados obtenidos se expresaron como porcentaje de log UFC/mL. Todos los tratamientos se probaron por triplicado. Las superficies SS-SiO2-Van mostraron un efecto antimicrobiano contra S. epidermidis, lo que llevó a la eliminación total del microorganismo después de 24 h de tratamiento en comparación con las superficies no tratadas (SS, SS-OH y SS-SiO2) . Los resultados pueden observarse en la figura 1. Adicionalmente, se comprobó la robustez de la actividad antimicrobiana con sucesivos ciclos. Se evaluó el efecto antimicrobiano de las mismas placas ya utilizadas para confirmar la presencia de la molécula antimicrobiana (Van-APTES) en las superficies. La eficacia de la actividad antimicrobiana (Figura 2) se mantuvo en los dos ensayos siguientes (Ensayo II y Ensayo III) y se obtuvo una reducción total de la viabilidad bacteriana después de un tratamiento de 72 horas. Sin embargo, se observó una disminución en la actividad antimicrobiana de los materiales SS-SiO2-Van en los siguientes ciclos de prueba. Así, la eficacia de las placas alcanzó un 80% en el caso del Ensayo IV y un 40% en el Ensayo V (Figura 2) tras 72 horas de incubación en presencia de bacterias. A pesar de esta disminución, la actividad antimicrobiana de las placas es notable. La actividad antimicrobiana de los recubrimientos de la invención, en particular los del ejemplo 2.4 (PP-SiO2-Van) , frente a los microrganismos se evaluó mediante ensayos invitro con Escherichia coli, lo que llevó a la eliminación total del microorganismo después de 24 h de tratamiento en comparación con las superficies no tratadas (PP, PP-OH y PP-SiO2) . Los resultados pueden observarse en la figura 3. Los resultados mostraron que las superficies de polipropileno funcionalizadas con un CAEs, como es la Vainillina, redujeron la viabilidad bacteriana de un 100% (Figura 3) . Ejemplo 5. Comprobación de la adhesión microbiana- SS-SiO2-Van. Los ensayos de adhesión bacteriana con SS-SiO2-Van se realizaron en medio líquido, caldo de triptona y soja (TSB, por sus siglas en inglés Tr y ptic Soy Broth) . Se prepararon diluciones de S. epidermidis en TSB para obtener una concentración de 104 células/mL. Un matraz que contenía las placas SS-SiO2-Van funcionalizadas se inoculó con 1 mL de suspensión de S. epidermidis para obtener una concentración final de 103 células/mL. Finalmente, todas las muestras se incubaron a 370C durante 24 h. Las placas de SS, SS-OH y SS-SiO2 también se sumergieron en una suspensión bacteriana similar como control. Después de la incubación, las bacterias no adheridas se eliminaron lavando suavemente las placas con una solución de fosfato (PBS) estéril (pH 7, 4) . Cada placa con bacterias adheridas se colocó en un matraz que contenía 3 mi de PBS estéril y se sonicó durante 5 min. Las soluciones sonicadas, que contenían las bacterias recuperadas, se diluyeron en serie y se distribuyeron 100 L de cada dilución en placas de Tr y ptic Soy Agar (TSA) . Las placas se incubaron durante la noche a 37 °C y el número de colonias se contó al día siguiente. La viabilidad de las bacterias se expresó como % de UFC. Todos los tratamientos se ensayaron por triplicado. Los resultados en la figura 4 mostraron que las superficies SS-SiO2 -Van pudieron inhibir el 75 % de la formación de biopelículas en comparación con las placas SS, SS-OH y SS-S iO2.
Publicaciones:
ES2956957 (04/01/2024) - A1 Solicitud de patente con informe sobre el estado de la técnica
Eventos:
En fecha 14/07/2023 se realizó Registro Instancia de Solicitud
En fecha 14/07/2023 se realizó Admisión a Trámite
En fecha 14/07/2023 se realizó Aceptación Tramitación CAP
En fecha 14/07/2023 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 17/07/2023 se realizó Superado examen de oficio
En fecha 19/12/2023 se realizó Realizado IET
En fecha 22/12/2023 se realizó 1109P_Comunicación Traslado del IET
En fecha 04/01/2024 se realizó Publicación Solicitud
En fecha 04/01/2024 se realizó Publicación Folleto Solicitud con IET (A1)
En fecha 28/03/2024 se realizó 5215P_Observaciones del solicitante al IET, Opinión Escrita y/o alegaciones a observaciones de terceros
En fecha 08/04/2024 se realizó Validación petición y/o pago de examen sustantivo conforme
Pagos:
14/07/2023 - Pago Tasas IET
+ ES-2956957_A11. Un recubrimiento antimicrobiano que comprende una capa de sílice y moléculas bioactivas funcionalizadas con una molécula de enlace, donde las moléculas bioactivas funcionalizadas están unidas a la superficie de la sílice mediante enlaces covalentes. 2. El recubrimiento antimicrobiano de acuerdo a la reivindicación anterior, donde la moléculas bioactiva se selecciona del grupo de componentes de aceites esenciales (CAE) , ácidos orgánicos polímeros naturales, bacteriocinas, enzimas, preferiblemente la molécula bioactiva es un aceite esencial, más preferiblemente la molécula bioactiva es un componente de aceite esencial (CAE) seleccionado del grupo constituido por carvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. 3. El recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones anteriores, donde la molécula de enlace es un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano, clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato, más preferiblemente la molécula de enlace es 3-aminopropil trietoxisilano. 4. El recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones anteriores, aplicado al menos parcialmente sobre un sustrato seleccionado del siguiente grupo: metales, polímeros, materiales cerámicos y/o vidrio. 5. El recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones anteriores, donde las moléculas bioactivas funcionalizadas están unidas a la sílice mediante enlaces covalentes silicio-oxigeno-silicio (Si-O-Si) . 6. Proceso para depositar un recubrimiento antimicrobiano de acuerdo a cualquiera de las reivindicaciones 1 a 5 en sustratos que comprende las siguientes etapas: a) proporcionar un sustrato; b) activación de la superficie del sustrato mediante el tratamiento del sustrato con una solución activadora; c) deposición de una capa de sílice en la superficie del sustrato mediante la polimerización de precursores de sílice en medio alcalino; d) funcionalización de las moléculas bioactivas mediante su reacción con la molécula de enlace en fase liquida; e) inmovilización covalente de las moléculas bioactivas funcionalizadas obtenidas en la etapa d) sobre la capa de sílice generada en la etapa c) mediante la deposición de una solución que comprende las moléculas bioactivas funcionalizadas; y f) secado de la superficie. 7. El proceso de acuerdo a la reivindicación 6, donde la deposición de la capa de sílice de la etapa c) se produce mediante la generación in situ de sílice a partir de un precursor seleccionado del grupo de ortosilicato de tetrametilo (TMOS) , ortosilicato de tetraetilo (TEOS) , metiltrimetoxisilano (MTMS) , feniltrimetoxisilano (PTMS) , dimetildimetoxisilano (DMDMS) y metacriloxipropiltrimetoxisilano (MPTMS) , más preferiblemente a partir de ortosilicato de tetraetilo (TEOS) . 8. El proceso de acuerdo a las reivindicaciones 6 a 7, donde la molécula bioactiva se selecciona del grupo de componentes de aceites esenciales, ácidos orgánicos polímeros naturales, bacteriocinas, enzimas, preferiblemente la molécula bioactiva es un aceite esencial, más preferiblemente la molécula bioactiva es un componente de aceite esencial seleccionado del grupo constituido por carvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. 9. El proceso de acuerdo a las reivindicaciones 6 a 8, donde la molécula de enlace empleada en la etapa d) es un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano, clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato, más preferiblemente la molécula de enlace es 3-aminopropil trietoxisilano. 10. Un elemento o superficie que comprende al menos parcialmente un recubrimiento antimicrobiano de acuerdo a cualquier de las reivindicaciones anteriores 1 a 5 o un recubrimiento preparado de acuerdo a la reivindicación 6 a 9. 11. El uso de un recubrimiento antimicrobiano de acuerdo a las reivindicaciones 1 a 5, un recubrimiento antimicrobiano preparado de acuerdo a la reivindicación 6 a 9 o de un elemento o superficie de acuerdo a la reivindicación 10 en la prevención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo.
Los productos y servicios protegidos por este registro son:
C09D 183/08 - A01N 25/34 - A01N 25/10 - C08G 77/38 - C08G 85/00 - C23C 18/12 - C23C 22/83 - A61L 29/08 - A61L 31/08
Descripciones:
+ ES-2956957_A1 Recubrimientos antimicrobianos Campo Técnico La presente invención se refiere a un recubrimiento antimicrobiano, a su proceso de preparación y su uso en la prevención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo. Antecedentes de la Invención Las infecciones nosocomiales constituyen uno de los problemas más importantes que se presentan en el sistema de salud, siendo una de las principales causas de mortalidad y aumento de la morbilidad en los pacientes hospitalizados. Una de las principales razones de estas infecciones es la capacidad microbiana de adherirse a superficies sólidas (bióticas o abióticas) . Esta capacidad provoca la formación de estructuras poliméricas denominadas biopelículas. La función de las biopelículas es actuar como una trampa para los nutrientes y como una barrera física que impide la penetración y difusión de antibióticos y desinfectantes comunes. La formación de biopelículas comienza con la adhesión de células planctónicas individuales a una superficie. Estas células adherentes se convierten en micro colonias que luego proliferan en biopelículas maduras. Las biopelículas maduras producen componentes de matriz extracelular (ECM) que son críticos para mantener las estructuras distintivas de los agregados celulares. Una estrategia efectiva para prevenir la formación de biopelículas en superficies bióticas y abióticas es depositar una capa antimicrobiana en la superficie del material. Existen varios estudios basados en la inmovilización o liberación de sustancias antimicrobianas sobre diferentes superficies, sin embargo, dependiendo de la aplicación, no son completamente exitosos debido a su limitada eficacia o toxicidad. La inmovilización o liberación de sustancias antimicrobianas, como derivados de metales, sales de poliamonio y antibióticos, ha mostrado resultados alentadores. Aun así, su uso puede estar asociado con efectos secundarios como citotoxicidad, hipersensibilidad y espuestas inflamatorias. Además, el uso indiscriminado de estas sustancias ha generado un problema mayor, que es la resistencia antimicrobiana. La resistencia a los antimicrobianos (RAM) ocurre cuando las bacterias, los virus, los hongos y/o los parásitos cambian con el tiempo y ya no responden a los medicamentos, lo que hace que las infecciones sean más difíciles de tratar y aumenta el riesgo de propagación de enfermedades, enfermedades graves y muerte. Como resultado de la resistencia a los medicamentos, los antibióticos y otros medicamentos antimicrobianos se vuelven ineficaces y las infecciones se vuelven cada vez más difíciles o imposibles de tratar. Se han empleado varios enfoques en la búsqueda de superficies antimicrobianas efectivas, incluida la resistencia a la adhesión, la destrucción por contacto y la lixiviación de biocidas. Entre estos enfoques, la muerte bacteriana por contacto parece ser la ruta más prometedora; este enfoque implica modificaciones químicas o físicas para unir un agente antimicrobiano a la superficie. Entre las estrategias más comúnmente aplicadas para la modificación de superficies se encuentran la adsorción (a través de interacciones electrostáticas) , el acoplamiento ligando-receptor y la unión covalente (Vasilev K, Cook J, Griesser HJ. Antibacterial surfaces for biomedical devices. Expert Rev Med Devices. 2009;6 (5) :553-567) . La unión covalente ofrece varias ventajas al proporcionar los enlaces más estables entre el compuesto bioactivo y la superficie. Algunos estudios han reportado la inmovilización sobre superficies de acero inoxidable u otras superficies (plástico, titanio y otras) de ciertas moléculas bioactivas como péptidos antibacterianos como magainina, nisina y lisozima o la inmovilización de biopolímeros como el quitosano. Algunas de las estrategias desarrolladas recientemente se describen a continuación. La solicitud de patente española EP3326971A1, "Sistema antimicrobiano", divulga la funcionalización de antimicrobianos naturales con grupos trialcoxisilano sobre la superficie de un soporte mesoporoso de sílice. El artículo "Antibacterial isoeugenol coating on stainless Steel and polyethylene surfaces prevenís biofilm growth" (Nielsen, C. K., et al. "Antibacterial isoeugenol coating on stainless Steel and polyethylene surfaces prevenís biofilm growth". Journal of applied microbiology 124.1 (2018) : 179-187) divulga recubrimientos de superficies de acero inoxidable y de polietileno con eugenol, para evitar el crecimiento de biofilms. El documento "Enhanced antimicrobial activity of essential oil components immobilized on silica partióles" (Ruiz-Rico, María, et al. "Enhanced antimicrobial activity of essential oil components immobilized on silica partióles." Food chemistr y 233 (2017) : 228-236.) divulga la inmovilización de aceites esenciales mediante 3-aminopropil trietoxisilano, sobre tres soportes distintos de silicio. El documento "Métodos y soportes para la inmovilización de componentes de aceites esenciales y su efecto sobre la actividad antimicrobiana y antioxidante" (Cebrián Cabo, Santiago. "Métodos y soportes para la inmovilización de componentes de aceites esenciales y su efecto sobre la actividad antimicrobiana y antioxidante." (2020) ) describe la inmovilización de componentes de aceites esenciales en nanopartículas de sílice. La solicitud de patente internacional WO2021107870A1 divulga un polímero antimicrobiano y la preparación de recubrimientos de superficies para aplicaciones antimicrobianas. No obstante, las estrategias descritas en estado de la técnica presentan varios inconvenientes tales como la poca robustez de la unión con la molécula bioactiva que eventualmente resulta en una baja actividad microbiana y potencial de reutilización de la superficie bajo. Además, los sistemas descritos no son fácilmente aplicables a distintas superficies, por ejemplo, paredes o encimeras, y/o elementos, por ejemplo, material quirúrgico o prótesis. La presente invención proporciona una solución a ese problema. Sumario de la invención En un primer aspecto, la invención se refiere a un recubrimiento antimicrobiano que comprende una capa de sílice y moléculas bioactivas funcionalizadas con una molécula de enlace, donde las moléculas bioactivas funcionalizadas están inmovilizadas covalentemente a la superficie de la sílice mediante enlaces covalentes. En un segundo aspecto, la invención se refiere a un proceso para depositar un recubrimiento antimicrobiano de acuerdo al primer aspecto de la invención que comprende las siguientes etapas: a) proporcionar un sustrato, b) activación de la superficie del sustrato mediante el tratamiento del sustrato con una solución de ácido sulfúrico y peróxido de hidrogeno. c) deposición de una capa de sílice en la superficie del sustrato mediante la polimerización de precursores de sílice en medio alcalino, d) funcionalización de las moléculas bioactivas mediante su reacción con la molécula de enlace en fase liquida, e) inmovilización covalente de las moléculas bioactivas funcionalizadas obtenidas en la etapa d) sobre la capa de sílice generada en la etapa c) mediante la deposición de una solución alcohólica que comprende las moléculas bioactivas funcionalizadas, y f) secado de la superficie a temperatura ambiente. En un tercer aspecto, la invención se refiere a un elemento, por ejemplo, herramientas quirúrgicas, o superficies, por ejemplo, paredes o suelos, que comprende al menos parcialmente un recubrimiento antimicrobiano de acuerdo al primer aspecto o un recubrimiento preparado de acuerdo al segundo aspecto de la invención. En un cuarto aspecto, la invención se refiere al uso de un recubrimiento antimicrobiano de acuerdo al primer aspecto, un recubrimiento antimicrobiano preparado de acuerdo al segundo aspecto o de un elemento o superficie de acuerdo al tercer aspecto de la invención en la prevención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo. Descripción de las figuras Figura 1. Comparativa de recuentos (UFC, %) de la bacteria S. epidermidis después del contacto con superficies funcionalizadas (SS-SiO2 -Van) y no funcionalizadas (SS, SS-OH y SS-SiO2) en función del tiempo. Figura 2. Robustez del efecto antimicrobiano de las superficies SS-SiO2-Van frente a S. epidermidis tras varios test sucesivos. Figura 3. Comparativa de recuentos (log CFU/ml, %) de la bacteria E. coli después del contacto con superficies funcionalizadas (PP-SiO2 -Van) y no funcionalizadas (PP, PP-OH y PP-SiO2) después de 24h. Figura 4. Capacidad inhibitoria para la formación de biopelículas de superficies SS-SiO2-Van frente a S. epidermidis después de 24h. Descripción detallada de la invención La presente invención proporciona un recubrimiento antimicrobiano que comprende una capa de sílice y moléculas bioactivas funcionalizadas con una molécula de enlace, donde las moléculas bioactivas funcionalizadas están inmovilizadas covalentemente a la superficie de la sílice mediante enlaces covalentes. El uso de recubrimientos antimicrobianos mejorados por una inmovilización covalente de una molécula antimicrobiana bioactiva en la superficie mediante una capa intermedia de sílice, supone una novedad en este campo técnico. En particular en lo que se refiere a la bacteria S. epidermidis, considerada una de las causas más frecuentes de infecciones nosocomiales y principal patógeno responsable de las infecciones crónicas asociadas al biopeliculas en tejidos como la piel, las vías respiratorias y los dispositivos médicos. El término "antimicrobiano" se refiere a un elemento que impide la formación o el desarrollo de los microorganismos. En particular, se refiere a un recubrimiento que previene el crecimiento microbiano, la formación de biopelículas, inhibe la adhesión microbiana y/o elimina las células microbianas adheridas al mismo. El término "molécula bioactiva" se refiere a moléculas que poseen actividad antimicrobiana, en particular antibacteriana, antifúngica y/o antiviral. El término "polímero (s) " en el contexto de esta solicitud significa oligómero (s) , polímero (s) y copolímero (s) , sus mezclas y principalmente también su formación de composites con base orgánica y/o sustancialmente orgánica. Habitualmente, el (los) "polímero (s) " en el contexto de esta solicitud se presenta (n) predominantemente o completamente en forma de polímero (s) y/o copolímero (s) . El término "funcionalizar" se refiere a la modificación de una superficie o molécula para incorporar ciertos elementos, por ejemplo, grupos funcionales o moléculas, que doten dicha superficie de propiedades fisicoquímicas particulares. El término "activar" se refiere a la capacidad, en un paso procedimental posterior, por ejemplo, una etapa de inmersión, de una solución y/o una dispersión acuosa, cerca de la superficie del sustrato, de generar grupos hidroxilo. En el procedimiento de acuerdo con la invención se crea de esta manera una condición de que puede formarse una capa secuencial sobre el sustrato. El término "inmovilización covalente" se refiere a la unión mediante un enlace covalente. En particular se refiere a la unión entre sustrato y sílice y a la unión sílice y molécula bioactiva mediante enlaces covalentes. Más específicamente, la presente invención se basa en la mejora y superación de los inconvenientes y desventajas que presentan los métodos ya conocidos. La invención se representa esquemáticamente en la Fig. 1, particularmente en el panel B, donde puede apreciarse el efecto del recubrimiento antimicrobiano (en este caso, S. epidermidis) , que comprende una capa de sílice funcionalizada con moléculas bioactivas (en este caso, Vainillina) . Este recubrimiento antimicrobiano puede actuar frente a los microorganismos que se desee, ya sean bacterias, virus o también hongos microscópicos, levaduras o protozoos. Así, el recubrimiento testado en S. epidermidis constituye un modelo para otros microorganismos. El recubrimiento del primer aspecto se une de manera covalente a la superficie del sustrato (S) mediante enlaces S-O-Si entre el sustrato y la capa de sílice. La unión covalente entre sustrato y recubrimiento mediante una capa de sílice dota el recubrimiento de gran robustez y permite que las moléculas bioactivas se mantengan ancladas en el sustrato durante un periodo prolongado de tiempo y por tanto se mantenga la eficacia antimicrobiana de la superficie recubierta. Los sustratos que pueden ser recubiertos por los recubrimientos de la invención son muy variados, como, por ejemplo, metales, polímeros, materiales cerámicos y/o vidrio. Los metales adecuados incluyen, entre otros, titanio, cobre, oro, estaño, níquel, aluminio, ierro, cobalto, plata, platino, magnesio, manganeso, zinc y aleaciones de metales como aceros, bronce o latón. En el grupo de los polímeros se incluyen polímeros convencionales, como, por ejemplo, cloruro de polivinilo (PVC) , ácido de polivinilo (PVA) , polietileno (PE) , poliestireno (PS) , polipropileno (PP) , policarbonato (PC) , tereftalato de polietileno (PET) , poliamida (PA) , poliuretano (PU) , estireno, butadieno, acrilonitrilo (ABS) , o polímeros biodegradables, como, por ejemplo, ácido poli láctico (PLA) , colágeno, biogomas, o celulosa. Los materiales cerámicos de interés incluyen, a modo de ejemplo, TiO2 , Al2O3 , materiales tipo cermet, por ejemplo, WC-Co o WC-Co-Cr, o materiales bi-componente como pueden ser TiO2 + NiAl. Los recubrimientos de la invención pueden recubrir la superficie del sustrato de manera total o parcial según sea necesario. En dichos recubrimientos antimicrobianos, se prefiere que las moléculas bioactivas se seleccionen del grupo de componentes de aceites esenciales (CAE) , ácidos orgánicos, polímeros naturales, bacteriocinas, y/o enzimas. En una realización preferida, la molécula bioactiva es un componente de aceite esencial. En la realización más preferida la molécula bioactiva se selecciona del grupo de componentes de aceites esenciales siguiente: carvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. En la realización aún más preferida la molécula bioactiva es vainillina. La actividad antimicrobiana de los CAE no se atribuye a un único mecanismo, sino que es una cascada de reacciones (degradación de la pared celular, daño de la membrana citoplásmica, daño de la proteína de la membrana, coagulación del citoplasma y agotamiento del poder de los protones) que da como resultado la destrucción de las células de los microorganismos. Además, los CAE pueden penetrar en biopelículas formadas y matar los microorganismos protegidos. En los recubrimientos de la invención, la molécula bioactiva se encuentra presente en un rango de concentraciones de 0, 5 a 1, 5 mg/cm2, preferiblemente en un rango de 0, 8 a 1, 05 mg/cm2. La molécula bioactiva en estos rangos de concentración asegura se produzca el efecto antimicrobiano deseado. En lo que se refiere a la molécula espadadora, se prefiere que la molécula de enlace sea un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano (APTES) , clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato, más preferiblemente la molécula de enlace es 3-aminopropil trietoxisilano (APTES) . En la realización preferida del primer aspecto las moléculas bioactivas funcionalizadas están unidas a la sílice mediante enlaces covalentes silicio-oxigeno-silicio (Si-O-Si) . Este enlace covalente Si-O-Si entre molécula bioactiva y sílice asegura una unión fuerte y duradera, de manera que el recubrimiento es resistente al paso del tiempo y a múltiples lavados, manteniendo su actividad antimicrobiana. En su segundo aspecto, la invención se refiere a un proceso para depositar un recubrimiento antimicrobiano de acuerdo al primer aspecto en sustratos que comprende las siguientes etapas: a) proporcionar un sustrato; b) activación de la superficie del sustrato mediante el tratamiento del sustrato con una solución activadora; c) deposición de una capa de sílice en la superficie del sustrato mediante la polimerización de precursores de sílice en medio alcalino; d) funcionalización de las moléculas bioactivas mediante su reacción con la molécula de enlace en fase liquida; e) inmovilización covalente de las moléculas bioactivas funcionalizadas obtenidas en la etapa d) sobre la capa de sílice generada en la etapa c) mediante la aplicación de una solución que comprende la molécula bioactiva funcionalizadas, y, f) secado de la superficie. En una realización preferida del segundo aspecto, los sustratos que pueden ser recubiertos por la invención son muy variados, como, por ejemplo, metales, polímeros, materiales cerámicos y/o vidrio. Los metales adecuados incluyen, entre otros, titanio, cobre, oro, estaño, níquel, aluminio, hierro, cobalto, plata, platino, magnesio, manganeso, zinc y aleaciones de metales como aceros, bronce o latón. En el grupo de los polímeros se incluyen, entre otros, cloruro de polivinilo (PVC) , ácido de polivinilo (PVA) , polietileno (PE) , poliestireno (PS) , polipropileno (PP) , policarbonato (PC) , tereftalato de polietileno (PET) , oliamida (PA) , poliuretano (PU) , estireno, butadieno, acrilonitrilo (ABS) , ácido poli láctico (PLA) , colágeno, biogoma, o celulosa. Los materiales cerámicos de interés incluyen, a modo de ejemplo, TiO2 , Al2O3 , materiales tipo cermet, por ejemplo, WC-Co o WC-C0-Cr, o materiales bi-componente como pueden ser T¡O2 + NiAl. En la realización del segundo aspecto, la solución activadora de la etapa b) es una solución ácida y/u oxidante. En una realización preferida del segundo aspecto, la superficie del sustrato se activa mediante una solución activadora que consiste en una solución acuosa de ácido sulfúrico, ácido nítrico, persulfato de potasio, peróxido de oxígeno o una mezcla de los mismos. La activación de la superficie se lleva a cabo durante menos de 15 min, preferiblemente 10 min. El contacto entre la solución acuosa y la superficie del sustrato debe ser corta para evitar los efectos corrosivos de la misma y a la vez generar suficientes grupos hidroxilos en la superficie del sustrato. En una realización preferida del segundo aspecto, la deposición de la capa de sílice de la etapa c) se produce mediante la generación in situ de sílice a partir de un precursor seleccionado del grupo de ortosilicato de tetrametilo (TMOS) , ortosilicato de tetraetilo (TEOS) , metiltrimetoxisilano (MTMS) , feniltrimetoxisilano (PTMS) , dimetildimetoxisilano (DMDMS) y metacriloxipropiltrimetoxisilano (MPTMS) . La opción más preferida de precursor es el ortosilicato de tetraetilo (TEOS) . En una realización preferida del segundo aspecto, la molécula bioactiva se selecciona del grupo de aceites esenciales, ácidos orgánicos polímeros naturales, bacteriocinas, enzimas, preferiblemente la molécula bioactiva es un aceite esencial. En una realización más preferida la molécula bioactiva es un componente de aceite esencial. En una realización aún más preferida la molécula bioactiva se selecciona del grupo de componentes de aceites esenciales (CAE) constituido porcarvacrol, cinamaldehído, perillaldehído, eugenol, timol, vainillina, geraniol, cafeno, timoquinona, dialiyldisulfito, alil isotiocianato o mezclas de los mismos. En la realización más preferida la molécula bioactiva es vainillina. En una realización preferida del segundo aspecto, la molécula de enlace empleada en la etapa d) es un alcoxisilano, preferiblemente la molécula de enlace se selecciona del siguiente grupo 3-aminopropil trietoxisilano, clorometil trietoxisilano, cloroetil trietoxisilano, cloropropiletil trietoxisilano, (3-mercaptopropil) trietoxisilano, (4-Clorofenil trietoxisilano, 3- (Trietoxisilil) propionitrilo, 3- (Trietoxisilil) propil isocianato. En la realización más preferida la molécula de enlace es 3-aminopropil trietoxisilano. En una realización preferida del segundo aspecto, la solución de la etapa e) que comprende la molécula bioactiva funcionalizada es una solución de pentano, ciclopentano, hexano, ciclohexano, benceno, tolueno, 1, 4-dioxano, cloroformo, éter dietílico, diclorometano (DCM) , tetrahidrofurano (THF) , acetona, dimetilformamida (DMF) , acetonitrilo (MeCN) , dimetilsulfóxido (DMSO) , ácido fórmico, n-butanol, alcohol isopropílico (IPA) , metanol, etanol, agua o sus mezclas. En una realización más preferida, la solución es una solución acuosa alcohólica, preferiblemente una solución de etanol y agua. En una realización preferente el secado de la etapa d) se produce a temperatura ambiente. En su tercer aspecto, la invención se refiere a un elemento o superficie que comprende al menos parcialmente un recubrimiento antimicrobiano de acuerdo al primer aspecto o un recubrimiento preparado de acuerdo al segundo aspecto de la invención. Los elementos o superficies que pueden comprender el recubrimiento de la invención pueden ser distintos materiales, en particular pueden ser de metal, polímeros, materiales cerámicos y/o vidrio. Los metales adecuados incluyen, entre otros, titanio, cobre, oro, estaño, níquel, aluminio, hierro, cobalto, plata, platino, magnesio, manganeso, zinc y aleaciones de metales como aceros, bronce o latón. En el grupo de los polímeros se incluyen, entre otros, cloruro de polivinilo (PVC) , ácido de polivinilo (PVA) , polietileno (PE) , poliestireno (PS) , polipropileno (PP) , policarbonato (PC) , tereftalato de polietileno (PET) , poliamida (PA) , poliuretano (PU) , estireno, butadieno, acrilonitrilo (ABS) , ácido poli láctico (PLA) , colágeno, biogoma, o celulosa. Los materiales cerámicos de interés incluyen, a modo de ejemplo, TiO2 , Al2O3 , materiales tipo cermet, por ejemplo, WC-Co o WC-C0-Cr, o materiales bi-componente como pueden ser T¡O2 + NiAl. Entre los elementos cuya superficie tendría mayor interés recubrir, pueden citarse: una mascarilla higiénica, un tejido, una tela, instrumental de uso clínico, una pared, un suelo, un mueble, un pasamanos, un dispositivo móvil, una pantalla táctil o un filtro de aire. En general, puede tener interés cualquier superficie de cualquier objeto presente en un lugar donde debe predominar la higiene y debe hacerse lo posible por mantenerla, pero donde, desgraciadamente, es habitual la presencia de distintos microorganismos. En su cuarto aspecto la invención se refiere a uso de un recubrimiento antimicrobiano de acuerdo al primer aspecto, un recubrimiento antimicrobiano preparado de acuerdo al segundo aspecto o de un elemento o superficie de acuerdo al tercer aspecto en la revención del crecimiento microbiano, formación de biopelículas, la inhibición de la adhesión microbiana y/o la eliminación de células microbianas adheridas al mismo. El microorganismo puede ser una bacteria, pero también un virus, un hongo microscópico, levaduras o un protozoo. Se tiene preferencia por una bacteria. La invención se explicará ahora con mayor detalle mediante los Ejemplos y Figuras que aparecen a continuación. Ejemplos Ejemplo 1. Funcionalización de moléculas bioactivas Ejemplo 1.1. Funcionalización de moléculas bioactivas - vainillina Para funcionalizar la molécula bioactiva, en este caso la vainillina, primeramente, se suspendió 1 g de vainillina en 25 mL de diclorometano y luego se añadieron a la mezcla 1, 2 mL de 3-aminopropil trietoxisilano (APTES) . La relación molar entre los reactivos fue de 1:1 de vainillina:APTES (Esquema 1) . La mezcla se agitó durante 2 h, y después de esto, la suspensión se evaporó a presión reducida para obtener el correspondiente derivado de alcoxisilano, (E) -2-metoxi-4- ( ( (3-trietoxisilil) propil) imino) metil) fenol. En este primer paso, la reacción entre la vainillina y APTES da lugar al producto 3 en el que la vainillina se une al grupo etoxi por medio de un enlace imina (Esquema 1) . En un segundo paso, 5 mmol de derivado de alcoxisilano (producto 3) se solubilizaron en etanol y se añadieron 340 mg de Pd/C. Posteriormente, se pasó un flujo de gas N2 a través del matraz de reacción para desplazar el O2. Luego, se agregó flujo de H2. La mezcla se gitó durante 3 h en atmósfera inerte. Finalmente, el derivado reducido, 2-metoxi-4- ( ( (3- (trietoxisilil) propil) amino) metil) fenol (Van-APTES) , producto 4, se filtró y evaporó a presión reducida para obtener el compuesto puro como un sólido amarillo pálido. El enlace imina formado entre el grupo aldehido de vainillina y el grupo amina de APTES (3) se redujo para estabilizar la unión del grupo vainillina al grupo trialcoxisilano (4) , Van-APTES. La reacción de reducción del enlace imina se llevó a cabo mediante una hidrogenación química utilizando H2 y paladio sobre carbono (Pd/C) como catalizador (Esquema 2) . Ejemplo 1.2. Funcionalización de moléculas bioactivas - carvacrol, el eugenol y el timol Para funcionalizar otras moléculas bioactivas, en este caso carvacrol, el eugenol y el timol, primeramente, se transformaron en derivados de aldehido. En un segundo paso, los aldehidos de carvacrol, eugenol y timol reaccionaron con 3-aminopropiltrietoxisilano (APTES) para producir los derivados de alcoxisilano correspondientes. Los aldehidos del carvacrol y del timol se sintetizaron por formilación directa utilizando paraformaldehído. En una síntesis típica, se colocaron 150 ml de acetonitrilo, 40 mmol de carvacrol o timol, 150 mmol de trimetilamina y 40 mmol de MgSO4 anhidro dentro de un matraz de fondo redondo. La mezcla se colocó en una atmósfera de argón y se agitó durante 15 minutos a temperatura ambiente. Posteriormente, se añadieron 270 mmol de paraformaldehído y la mezcla de reacción se calentó a reflujo durante 3, 5 h a 83 °C. Luego se dejó enfriar la mezcla a temperatura ambiente. La solución se acidificó con una solución de HCl al 5% (320 mi) y se agitó durante 30 min en atmósfera inerte. Finalmente, la porción orgánica se xtrajo con éter dietílico y los disolventes se eliminaron a presión reducida para obtener el aldehido de carvacrol o del timol. El aldehido del eugenol se sintetizó mediante una reacción de Reimer-Tiemann. En una síntesis típica, 150 ml de agua se calentaron a 80 °C, en un matraz de fondo redondo, y 22 mmol de eugenol se disolvieron en el agua. El calor se redujo a 60 °C, luego se agregaron 400 mmol de KOH y 88 mmol de cloroformo. Como la reacción fue exotérmica, se añadió cloroformo a una velocidad de 1 ml/h durante un período de 7 horas por razones de seguridad. La mezcla de reacción se mantuvo a 60 °C durante un período adicional de 8 horas. Luego, la solución se acidificó con una solución de H2SO4 al 10%. La porción orgánica se extrajo con n-butanona y los disolventes se eliminaron a presión reducida. Para facilitar la inmovilización covalente de los componentes de aceites esenciales a la capa de sílice, se sintetizaron los correspondientes derivados de aceites esenciales. Para ello se hicieron reaccionar 2 mi de los aldehidos de carvacrol, timol o eugenol con 2, 3 mi (10 mmol) de (3-aminopropil) trietoxisilano (APTES) en presencia de diclorometano (20 mi) y MgSO4 , dando lugar a las correspondientes iminas, que posteriormente se reducen de la misma manera que lo descrito para Van-APTES en el ejemplo 1.1. La mezcla se calentó a reflujo durante 1 h, luego se filtró y se evaporó a presión reducida para obtener un líquido transparente. Ejemplo 2. Preparación del recubrimiento antimicrobiano A continuación, se describe la preparación de los recubrimientos de la invención. Ejemplo 2.1 Activación del sustrato - acero inoxidable (SS) El primer paso en la funcionalización de SS es la preparación de la superficie de acero inoxidable. Antes de depositar la capa de sílice, la superficie del material SS debe desengrasarse adecuadamente mediante ultrasonidos en varios solventes como etanol y acetona, y luego con agua. Para ese fin, se colocaron placas de acero inoxidable (placas SS) en un vaso de precipitados (1 placa en 1 vaso de precipitados) y se sonicaron durante 10 min en cada uno de los siguientes productos químicos en sucesión: acetona (70 % v/v) , etanol y agua desionizada. Después del procedimiento de lavado, la superficie SS debe tratarse químicamente con una solución ácida o alcalina para activar la superficie metálica y exponer los grupos hidroxilo de la superficie. Los grupos hidroxilo se forman por quimisorción disociativa de moléculas de agua y, en general, se considera que la hidratación y la hidroxilación se producen en los sitios de iones metálicos reticulares expuestos en la superficie. Esta activación es importante porque la cantidad de grupos hidroxilo obtenidos durante el proceso de activación influye fuertemente en el inicio de la unión del silano y, por lo tanto, en la formación de la película de sílice. Luego, para el procedimiento de activación, los materiales SS lavados se trataron con solución piraña y se obtuvieron los materiales SS-OH. La solución piraña correspondiente consistió en la adición de peróxido de hidrógeno en un vaso de precipitados, al cual se le añadió lentamente ácido sulfúrico concentrado, en una proporción de ácido sulfúrico a peróxido de hidrógeno de 7:3 (v/v) . A continuación, la mezcla resultante se agitó suavemente antes de su uso. Las placas SS limpias se sumergieron en la solución de piraña durante 10 min. Pasado este tiempo, las placas se retiraron y se colocaron en una segunda solución de piraña durante 5 min. Después del segundo tratamiento con piraña, las placas SS se enjuagaron dos veces en agua ultrapura antes de colocarlas en un baño de agua ultrapura durante 24 h. Las placas resultantes se denominarán SS-OH. Así, las superficies de SS y SS-OH, difieren únicamente en la presencia en las superficies SS-OH de los grupos hidroxilo generados. Los grupos hidroxilo son esenciales en la formación de fuertes enlaces covalentes con los grupos silanol de la sílice del recubrimiento. Ejemplo 2.2 Deposición de la capa de sílice sobre el soporte Las placas SS-OH se trataron con TEOS mediante un procedimiento sol-gel. Las placas de SS-OH se colocaron en una solución acuosa básica, se calentaron a 80 °C y luego se añadieron gota a gota 5 mL de TEOS y la mezcla se agitó durante treinta minutos. Las placas se enjuagaron dos veces en agua ultrapura y se secaron a 100 °C durante la noche. La hidrólisis del TEOS produce grupos silanol (Si-OH) en presencia de agua y facilita la rápida adsorción de las entidades de silicato en la superficie del SS- material OH a través e enlaces de hidrógeno, para condensar aún más y formar un enlace covalente metalsiloxano (Me-O-Si-OH) . Los grupos silanol facilitan la unión covalente de moléculas orgánicas a la superficie, lo que resulta en una funcionalización estable debido a su excelente estabilidad térmica, mecánica y química. Ejemplo 2.3 Funcionalización de la capa de sílice con las moléculas bioactivas - vainillina Para la funcionalización la superficie de SS-SiO2 , este material se puso en contacto con el derivado de vainillina (Van-APTES) previamente sintetizado formando así los materiales SS-SiO2-Van. La unión a las superficies se produce por hidrólisis de los grupos etoxi del derivado Van-APTES que conduce a la formación de silanoles. Los silanoles de Van-APTES se condensan con los silanoles de la superficie SS-Si02 y conducen a la formación de enlaces covalentes Si-O-Si. Se solubilizó 1 g de Van-APTES en etanol. La solución se vertió en las placas de SS-SiO2 y las placas se agitaron durante 5, 5 horas a temperatura ambiente. Luego, las placas se lavaron con etanol y se secaron a temperatura ambiente, dando lugar a las superficies SS-SiO2-Van Ejemplo 2.4 Activación del sustrato - polipropileno (PP) Enfocándonos en lo citado anteriormente, esta invención presenta también como ejemplo la inmovilización de un aceite esencial funcionalizado con un alcoxisilano (aminopropiltrietoxisilinao, APTES) , como pueda ser la molécula bioactiva antimicrobiana Vainillina, sobre una superficie, como puede ser por ejemplo el polipropileno (PP) . El primer paso en la funcionalización de PP es la preparación de la superficie de polipropileno. La superficie PP debe tratarse químicamente para exponer los grupos hidroxilo de la superficie. Para ello, se trató la superficie del plástico polipropileno (PP) con un agente oxidante (peroxidisulfato de potasio) para generar grupo hidroxilo (PP-OH) , importante para la funcionalización. El peroxidisulfato de potasio se utiliza como fuente de radicales en solución acuosa, es bien conocido como iniciador de la polimerización por radicales libres y como agente oxidante. Los grupos hidroxilo del PP se forman por la extracción de un hidrógeno (del carbono terciario presente en cada unidad de repetición del polímero) que conduce a la formación de un macroradical que posteriormente reacciona con un segundo radical hidroxilo, dando lugar a la introducción de grupos hidroxilo en la superficie del PP. Esta activación es importante porque la cantidad de grupos hidroxilo obtenidos durante el proceso de activación influye fuertemente en el inicio de la unión del silano y, por lo tanto, en la formación de la película de sílice. Los grupos hidroxilo son esenciales en la formación de fuertes enlaces covalentes con los grupos silanol de la sílice del recubrimiento. A continuación, se depositó un recubrimiento de capa de sílice e inmovilizó covalentemente con molécula bioactiva funcionalizada con APTES como los llevados a cabo en los procesos descritos en los ejemplos Ejemplo 2.2 y 2.3, dando lugar a las superficies PP-SiO2yfinalm ente PP-SiO2-Van. Ejemplo 3. Cuantificación de la funcionalización con las moléculas bioactivas - SS-SiO?-Van. Para cuantificar la funcionalización de la superficie SS-SiO2-Van, se realizó un ensayo colorimétrico de superficie. Para este propósito, se usó ninhidrina como agente de prueba colorimétrica. Generalmente, la ninhidrina se usa en ensayos colorimétricos para el reconocimiento de grupos amina, en estos ensayos se observa un cambio de color de amarillo a púrpura intenso solo en el caso de la presencia de grupos amino en la solución. El color púrpura intenso, conocido como violeta de Ruhemann, se produce cuando dos moléculas del compuesto ninhidrina (2, 2-dihidroxiindano-1, 3-diona) reaccionan con una amina primaria, una amina secundaria o un aminoácido. Considerando esto, el ensayo de ninhidrina se desarrolló sumergiendo placas de SS, SS-OH, SS-SiO2 y SS-SiO2-Van en la solución de ninhidrina y las placas se dejaron en contacto con la solución durante 10 min a 80 °C. Después de este tiempo, se observó que solo las placas de SS-SiO2 -Van se tornaron de color púrpura, lo que confirma el proceso de uncionalización de la vainillina en la superficie. Después de eso, las placas de SS-SiO2-Van se sumergieron en 5 mi de etanol y se sonicaron durante varias horas para separar el complejo Van-ninhidrina de la superficie. Cuando se liberó todo el color de las placas SS debido a la ninhidrina unida, se cuantificó el contenido de Van-ninhidrina del disolvente de etanol midiendo su absorbancia a 400 nm. Previamente se preparó una curva de calibración con el complejo Van-ninhidrina obtenido al hacer reaccionar la ninhidrina con el derivado Van-APTES en etanol (de 0, 9 a 10, 5 mg/mL) y se utilizó para la cuantificación. La misma metodología se realizó para las superficies desnudas y de control: placas SS (superficie desnuda) , placas SS-OH y SS-SiO2 (superficies de control) . El resultado obtenido fue de 0, 95 ±0, 1 mg/cm2 de funcionalización sobre cada superficie de acero SS-SiO2-Van. Para las placas de SS, SS-OH y SS-SiO2 el resultado obtenido fue de 0 mg/cm2. Ejemplo 4. Evaluación de la viabilidad microbiana - SS-SiOp-Van v PP-SiOp-Van. La actividad antimicrobiana de los recubrimientos de la invención, en particular los del ejemplo 2 (SS-SiO2-Van) , frente a los microrganismos se evaluó mediante ensayos in-vitro con S. epidermidis. La evaluación de la viabilidad microbiana se realizó en medio líquido, para permitir el contacto entre las bacterias y las superficies funcionalizadas y no funcionalizadas durante la incubación, seguido de placas para enumerar las unidades formadoras de colonias (UFC) viables restantes. Se compararon materiales recubiertos con el recubrimiento de la invención con materiales como el acero inoxidable (SS) , acero inoxidable activado (SS-OH) y acero inoxidable recubierto con sílice (SS-SiO2) , estos fueron considerados como controles negativos. La eficacia antimicrobiana se realizó en medio líquido, en solución de fosfato (PBS) . Se prepararon diluciones inoculadas con S. epidermidis en PBS para obtener una concentración de 104 células/mL. Un matraz que contenía las superficies SS-SiO2-Van funcionalizadas, se inoculó con 1 mL de suspensión de S. epidermidis para obtener una concentración final de 103 células/mL. Las placas de SS, SS-OH y SS-SiO2 se trataron siguiendo el mismo procedimiento que SS-SiO2-Van. Finalmente, todas las muestras se incubaron con agitación orbital (120 rpm) a 37 °C durante 24 h. Para contabilizar las células viables, se tomaron alícuotas de 100 l de cada suspensión de muestra (SS, SS-OH, SS-SiO2 y SS-SiC>2-Van) y se distribuyeron en placas de agar soja triptona (TSA, por sus siglas en inglés) . Después de la incubación de la placa a 37 °C durante 24 h, se contaron las colonias y los resultados obtenidos se expresaron como porcentaje de log UFC/mL. Todos los tratamientos se probaron por triplicado. Las superficies SS-SiO2-Van mostraron un efecto antimicrobiano contra S. epidermidis, lo que llevó a la eliminación total del microorganismo después de 24 h de tratamiento en comparación con las superficies no tratadas (SS, SS-OH y SS-SiO2) . Los resultados pueden observarse en la figura 1. Adicionalmente, se comprobó la robustez de la actividad antimicrobiana con sucesivos ciclos. Se evaluó el efecto antimicrobiano de las mismas placas ya utilizadas para confirmar la presencia de la molécula antimicrobiana (Van-APTES) en las superficies. La eficacia de la actividad antimicrobiana (Figura 2) se mantuvo en los dos ensayos siguientes (Ensayo II y Ensayo III) y se obtuvo una reducción total de la viabilidad bacteriana después de un tratamiento de 72 horas. Sin embargo, se observó una disminución en la actividad antimicrobiana de los materiales SS-SiO2-Van en los siguientes ciclos de prueba. Así, la eficacia de las placas alcanzó un 80% en el caso del Ensayo IV y un 40% en el Ensayo V (Figura 2) tras 72 horas de incubación en presencia de bacterias. A pesar de esta disminución, la actividad antimicrobiana de las placas es notable. La actividad antimicrobiana de los recubrimientos de la invención, en particular los del ejemplo 2.4 (PP-SiO2-Van) , frente a los microrganismos se evaluó mediante ensayos invitro con Escherichia coli, lo que llevó a la eliminación total del microorganismo después de 24 h de tratamiento en comparación con las superficies no tratadas (PP, PP-OH y PP-SiO2) . Los resultados pueden observarse en la figura 3. Los resultados mostraron que las superficies de polipropileno funcionalizadas con un CAEs, como es la Vainillina, redujeron la viabilidad bacteriana de un 100% (Figura 3) . Ejemplo 5. Comprobación de la adhesión microbiana- SS-SiO2-Van. Los ensayos de adhesión bacteriana con SS-SiO2-Van se realizaron en medio líquido, caldo de triptona y soja (TSB, por sus siglas en inglés Tr y ptic Soy Broth) . Se prepararon diluciones de S. epidermidis en TSB para obtener una concentración de 104 células/mL. Un matraz que contenía las placas SS-SiO2-Van funcionalizadas se inoculó con 1 mL de suspensión de S. epidermidis para obtener una concentración final de 103 células/mL. Finalmente, todas las muestras se incubaron a 370C durante 24 h. Las placas de SS, SS-OH y SS-SiO2 también se sumergieron en una suspensión bacteriana similar como control. Después de la incubación, las bacterias no adheridas se eliminaron lavando suavemente las placas con una solución de fosfato (PBS) estéril (pH 7, 4) . Cada placa con bacterias adheridas se colocó en un matraz que contenía 3 mi de PBS estéril y se sonicó durante 5 min. Las soluciones sonicadas, que contenían las bacterias recuperadas, se diluyeron en serie y se distribuyeron 100 L de cada dilución en placas de Tr y ptic Soy Agar (TSA) . Las placas se incubaron durante la noche a 37 °C y el número de colonias se contó al día siguiente. La viabilidad de las bacterias se expresó como % de UFC. Todos los tratamientos se ensayaron por triplicado. Los resultados en la figura 4 mostraron que las superficies SS-SiO2 -Van pudieron inhibir el 75 % de la formación de biopelículas en comparación con las placas SS, SS-OH y SS-S iO2.
Publicaciones:
ES2956957 (04/01/2024) - A1 Solicitud de patente con informe sobre el estado de la técnica
Eventos:
En fecha 14/07/2023 se realizó Registro Instancia de Solicitud
En fecha 14/07/2023 se realizó Admisión a Trámite
En fecha 14/07/2023 se realizó Aceptación Tramitación CAP
En fecha 14/07/2023 se realizó 1001P_Comunicación Admisión a Trámite
En fecha 17/07/2023 se realizó Superado examen de oficio
En fecha 19/12/2023 se realizó Realizado IET
En fecha 22/12/2023 se realizó 1109P_Comunicación Traslado del IET
En fecha 04/01/2024 se realizó Publicación Solicitud
En fecha 04/01/2024 se realizó Publicación Folleto Solicitud con IET (A1)
En fecha 28/03/2024 se realizó 5215P_Observaciones del solicitante al IET, Opinión Escrita y/o alegaciones a observaciones de terceros
En fecha 08/04/2024 se realizó Validación petición y/o pago de examen sustantivo conforme
Pagos:
14/07/2023 - Pago Tasas IET
Fuente de la información
Parte de la información aquí publicada es pública puesto que ha sido obtenida de la Oficina de Propiedad Industrial de los diferentes países el 08/05/2024 y por lo tanto puede ser que la información no esté actualizada.Parte de la información aquí mostrada ha sido calculada por nuestro sistema informático y puede no ser veraz.
Privacidad
Si considera que al información aquí publicada afecta a su privacidad y desea que eliminemos la información aquí publicada envíe un email a info@patentes-y-marcas.com o rellene el formulario que encontrará aquí.Información sobre el registro de patente nacional por Recubrimientos antimicrobianos con el número P202330594
El registro de patente nacional por Recubrimientos antimicrobianos con el número P202330594 fue solicitada el 14/07/2023. Se trata de un registro en España por lo que este registro no ofrece protección en el resto de países. El registro Recubrimientos antimicrobianos con el número P202330594 fue solicitada por UNIVERSITAT POLITÈCNICA DE VALÈNCIA mediante los servicios del agente Jorge Isern Jara. El registro [modality] por Recubrimientos antimicrobianos con el número P202330594 está clasificado como C09D 183/08,A01N 25/34,A01N 25/10,C08G 77/38,C08G 85/00,C23C 18/12,C23C 22/83,A61L 29/08,A61L 31/08 según la clasificación internacional de patentes.
Otras invenciones solicitadas en la clasificación internacional de patentes C09D 183/08,A01N 25/34,A01N 25/10,C08G 77/38,C08G 85/00,C23C 18/12,C23C 22/83,A61L 29/08,A61L 31/08.
Es posible conocer invenciones similares al campo de la técnica se refiere. El registro de patente nacional por Recubrimientos antimicrobianos con el número P202330594 está clasificado con la clasificación C09D 183/08,A01N 25/34,A01N 25/10,C08G 77/38,C08G 85/00,C23C 18/12,C23C 22/83,A61L 29/08,A61L 31/08 por lo que si se desea conocer más registros con la clasificación C09D 183/08,A01N 25/34,A01N 25/10,C08G 77/38,C08G 85/00,C23C 18/12,C23C 22/83,A61L 29/08,A61L 31/08 clicar aquí.Otras invenciones solicitadas a través del representante JORGE ISERN JARA
Es posible conocer todas las invenciones solicitadas a través del agente JORGE ISERN JARA entre las que se encuentra el registro patente nacional por Recubrimientos antimicrobianos con el número P202330594. Si se desean conocer más invenciones solicitadas a través del agente JORGE ISERN JARA clicar aquí.Patentes en España
Es posible conocer todas las invenciones publicadas en España entre las que se encuentra el registro patente nacional por Recubrimientos antimicrobianos. Nuestro portal www.patentes-y-marcas.com ofrece acceso a las publicaciones de patentes en España. Conocer las patentes registradas en un país es importante para saber las posibilidades de fabricar, vender o explotar una invención en España.Patentes registradas en la clase C
Es posible conocer todas las patentes registradas en la clase C (QUIMICA; METALURGIA) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C09
Es posible conocer todas las patentes registradas en la clase C09 (COLORANTES; PINTURAS; PULIMENTOS; RESINAS NATURALES; ADHESIVOS; COMPOSICIONES NO PREVISTAS EN OTRO L) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C09D
Es posible conocer todas las patentes registradas en la clase C09D (COMPOSICIONES DE REVESTIMIENTO, p. ej. PINTURAS, BARNICES, LACAS; EMPLASTES; PRODUCTOS QUIMICOS PARA) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A
Es posible conocer todas las patentes registradas en la clase A (NECESIDADES CORRIENTES DE LA VIDA) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A01
Es posible conocer todas las patentes registradas en la clase A01 (AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A01N
Es posible conocer todas las patentes registradas en la clase A01N (CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C08
Es posible conocer todas las patentes registradas en la clase C08 (COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C08G
Es posible conocer todas las patentes registradas en la clase C08G (COMPUESTOS MACROMOLECULARES OBTENIDOS POR REACCIONES DISTINTAS A AQUELLAS EN LAS QUE INTERVIENEN SOL) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C23
Es posible conocer todas las patentes registradas en la clase C23 (REVESTIMIENTO DE MATERIALES METALICOS; REVESTIMIENTO DE MATERIALES CON MATERIALES METALICOS; TRATAMI) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase C23C
Es posible conocer todas las patentes registradas en la clase C23C (REVESTIMIENTO DE MATERIALES METALICOS; REVESTIMIENTO DE MATERIALES CON MATERIALES METALICOS; TRATAMI) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61
Es posible conocer todas las patentes registradas en la clase A61 (CIENCIAS MEDICAS O VETERINARIAS; HIGIENE) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.Patentes registradas en la clase A61L
Es posible conocer todas las patentes registradas en la clase A61L (PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZ) entre las que se encuentra la patente Recubrimientos antimicrobianos con el número P202330594. Conocer las patentes registradas en una clase es importante para saber las posibilidades de registrar una patente en esa misma clase.
¿Tienes alguna duda?
Escribe tu consulta y te responderemos rápida y gratuitamente.


 P202330576
P202330576